Puryna

|
|
|
|

|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
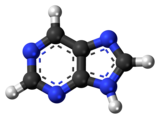
9H - puryna
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.004.020 |
| KEGG | |
| Siatka | Puryna |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C5H4N4 _ _ _ _ _ | |
| Masa cząsteczkowa | 120,115 g·mol -1 |
| Temperatura topnienia | 214 ° C (417 ° F; 487 K) |
| 500 g/L (temperatura pokojowa) | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Puryna jest heterocyklicznym aromatycznym związkiem organicznym , który składa się z dwóch połączonych ze sobą pierścieni ( pirymidyny i imidazolu ). Jest rozpuszczalny w wodzie . Puryna daje również swoją nazwę szerszej klasie cząsteczek , purynom , które obejmują podstawione puryny i ich tautomery . Są to najczęściej występujące azot w przyrodzie.
Źródła dietetyczne
Puryny występują w dużym stężeniu w mięsie i produktach mięsnych, zwłaszcza w narządach wewnętrznych, takich jak wątroba i nerki . Ogólnie rzecz biorąc, diety roślinne mają niską zawartość puryn. Rośliny i glony o wysokiej zawartości puryn obejmują niektóre rośliny strączkowe ( soczewicę i groszek czarny ) oraz spirulinę . Przykłady źródeł o wysokiej zawartości puryn obejmują: cukierki , anchois , sardynki , wątrobę, nerki wołowe , mózgi , ekstrakty mięsne (np. Oxo , Bovril ), śledź , makrela , przegrzebki , dziczyzna , drożdże ( piwo , ekstrakt drożdżowy , drożdże odżywcze ) i sos .
Umiarkowaną ilość puryn zawiera również czerwone mięso, wołowina , wieprzowina , drób , ryby i owoce morza , szparagi , kalafior , szpinak , grzyby , zielony groszek , soczewica , suszony groszek, fasola , płatki owsiane , otręby pszenne , kiełki pszenicy i jagody. .
Biochemia
Puryny i pirymidyny tworzą dwie grupy zasad azotowych , w tym dwie grupy zasad nukleotydowych . Zasady purynowe to guanina (G) i adenina (A), które tworzą odpowiednie nukleozydy- deoksyrybonukleozydy ( deoksyguanozyna i deoksyadenozyna ) z ugrupowaniem dezoksyrybozy i rybonukleozydy ( guanozyna , adenozyna) ) z ugrupowaniem rybozy. Te nukleozydy z kwasem fosforowym tworzą odpowiednie nukleotydy (dezoksyguanylan, deoksyadenyl i guanylan, adenylan), które są budulcem DNA i RNA . Zasady purynowe odgrywają również istotną rolę w wielu procesach metabolicznych i sygnalizacyjnych w obrębie związków monofosforanu guanozyny (GMP) i monofosforanu adenozyny (AMP).
Aby przeprowadzić te podstawowe procesy komórkowe, komórka potrzebuje zarówno puryn, jak i pirymidyn , i to w podobnych ilościach. Zarówno puryna, jak i pirymidyna działają samohamująco i aktywująco . Kiedy powstają puryny, hamują one enzymy wymagane do tworzenia większej ilości puryn. To samohamowanie występuje, ponieważ aktywują one również enzymy potrzebne do tworzenia pirymidyn. Pirymidyna jednocześnie w podobny sposób samohamuje i aktywuje purynę. Z tego powodu w komórce przez cały czas znajduje się prawie taka sama ilość obu substancji.
Nieruchomości
Puryna jest zarówno bardzo słabym kwasem ( pK a 8,93), jak i jeszcze słabszą zasadą ( pK a 2,39). W przypadku rozpuszczenia w czystej wodzie pH jest w połowie między tymi dwiema wartościami pKa.
Puryna jest aromatyczna , ma cztery tautomery , z których każdy ma wiązanie wodorowe z innym z czterech atomów azotu. Są one identyfikowane jako 1-H, 3-H, 7-H i 9-H (patrz rysunek numerowanego pierścienia). Powszechna postać krystaliczna faworyzuje tautomer 7-H, podczas gdy w rozpuszczalnikach polarnych przeważają zarówno tautomery 9-H, jak i 7-H. Podstawniki pierścieni i interakcje z innymi cząsteczkami mogą przesunąć równowagę tych tautomerów.
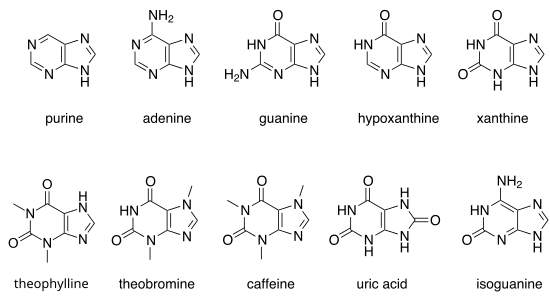
Godne uwagi puryny
Istnieje wiele naturalnie występujących puryn. Należą do nich nukleozasady adenina ( 2 ) i guanina ( 3 ). W DNA zasady te tworzą wiązania wodorowe odpowiednio z ich komplementarnymi pirymidynami , tyminą i cytozyną . Nazywa się to komplementarnym parowaniem zasad. W RNA dopełnieniem adeniny jest uracyl zamiast tyminy.
Inne godne uwagi puryny to hipoksantyna , ksantyna , teofilina , teobromina , kofeina , kwas moczowy i izoguanina .
Funkcje

Oprócz kluczowych ról puryn (adeniny i guaniny) w DNA i RNA, puryny są również istotnymi składnikami wielu innych ważnych biomolekuł, takich jak ATP , GTP , cykliczny AMP , NADH i koenzym A. Sama puryna ( 1 ) nie została znaleziona w naturze, ale można ją wytworzyć w drodze syntezy organicznej .
Mogą również działać bezpośrednio jako neuroprzekaźniki , działając na receptory purynergiczne . Adenozyna aktywuje receptory adenozyny .
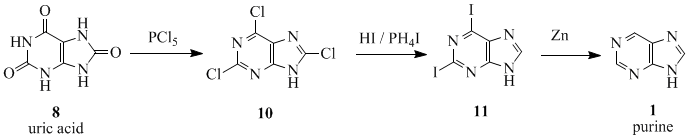
Historia
Termin puryna ( czysty mocz ) został wymyślony przez niemieckiego chemika Emila Fischera w 1884 roku. Po raz pierwszy zsyntetyzował go w 1898 roku. Materiałem wyjściowym do sekwencji reakcji był kwas moczowy ( 8 ), który został wyizolowany z kamieni nerkowych przez Carl Wilhelm Scheele w 1776 r. Kwas moczowy (8) poddano reakcji z PCl 5 otrzymując 2,6,8-trichloropurynę ( 10 ), którą przekształcono za pomocą HI i PH 4 I dać 2,6-dijodopurynę ( 11 ). Produkt zredukowano do puryny ( 1 ) stosując pył cynkowy .
Metabolizm
Wiele organizmów ma szlaki metaboliczne umożliwiające syntezę i rozkład puryn.
Puryny są biologicznie syntetyzowane jako nukleozydy (zasady przyłączone do rybozy ).
Nagromadzenie zmodyfikowanych nukleotydów purynowych zaburza różne procesy komórkowe, zwłaszcza te z udziałem DNA i RNA . Aby być żywotnymi, organizmy posiadają szereg fosfohydrolaz dezoksypurynowych, które hydrolizują te pochodne purynowe, usuwając je z aktywnych pul NTP i dNTP . Deaminacja zasad purynowych może skutkować akumulacją takich nukleotydów jak ITP , dITP, XTP i dXTP.
Defekty enzymów kontrolujących produkcję i rozkład puryn mogą poważnie zmienić sekwencje DNA komórki, co może wyjaśniać, dlaczego ludzie, którzy są nosicielami pewnych genetycznych wariantów enzymów metabolicznych puryn, są bardziej narażeni na niektóre rodzaje raka .
Biosynteza puryn w trzech domenach życia
Organizmy we wszystkich trzech domenach życia, eukarionty , bakterie i archeony , są zdolne do przeprowadzania de novo biosyntezy puryn . Ta zdolność odzwierciedla niezbędność puryn do życia. Biochemiczny szlak syntezy jest bardzo podobny u eukariontów i gatunków bakterii, ale jest bardziej zmienny u gatunków archeonów. Stwierdzono, że prawie kompletny lub kompletny zestaw genów wymaganych do biosyntezy puryn występuje u 58 z 65 badanych gatunków archeonów. Jednak zidentyfikowano również siedem gatunków archeonów z całkowicie lub prawie całkowicie nieobecnymi genami kodującymi purynę. Najwyraźniej gatunki archeologiczne niezdolne do syntezy puryn są w stanie pozyskiwać egzogenne puryny do wzrostu, a zatem są analogiczne do mutantów purynowych eukariontów, np. mutantów purynowych grzyba Ascomycete Neurospora crassa , które również wymagają egzogennych puryn do wzrostu.
Związek z dną moczanową
Wyższy poziom spożycia mięsa i owoców morza wiąże się ze zwiększonym ryzykiem dny moczanowej , podczas gdy wyższy poziom spożycia produktów mlecznych wiąże się ze zmniejszonym ryzykiem. Umiarkowane spożycie warzyw lub białka bogatych w purynę nie wiąże się ze zwiększonym ryzykiem dny moczanowej. Podobne wyniki uzyskano w przypadku ryzyka hiperurykemii .
Synteza laboratoryjna
Oprócz syntezy puryn in vivo w metabolizmie puryn , purynę można również wytworzyć sztucznie.
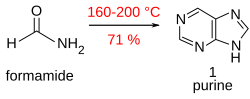
Purynę ( 1 ) otrzymuje się z dobrą wydajnością, gdy formamid ogrzewa się w otwartym naczyniu w temperaturze 170°C przez 28 godzin.
Ta niezwykła reakcja i inne im podobne zostały omówione w kontekście pochodzenia życia .
Opatentowana 20 sierpnia 1968 r. obecnie uznana metoda produkcji adeniny na skalę przemysłową jest zmodyfikowaną formą metody formamidowej. Ta metoda polega na podgrzaniu formamidu w temperaturze 120 stopni Celsjusza w zamkniętej kolbie przez 5 godzin w celu wytworzenia adeniny. Ilość reakcji jest znacznie zwiększona przy użyciu tlenochlorku fosforu (chlorku fosforu) lub pięciochlorku fosforu jako katalizatora kwasowego oraz światła słonecznego lub warunków ultrafioletowych. Po upływie 5 godzin i schłodzeniu roztworu formamid-tlenochlorek fosforu-adenina, do kolby zawierającej formamid i utworzoną adeninę wlewa się wodę. Następnie roztwór wodno-formamidowo-adeninowy przelewa się przez kolumnę filtracyjną z węglem aktywnym. Cząsteczki wody i formamidu, będąc małymi cząsteczkami, przejdą przez węgiel drzewny do kolby na odpady; duże cząsteczki adeniny będą jednak przyczepiać się lub „adsorbować” do węgla drzewnego z powodu sił van der waalsa, które oddziałują między adeniną a węglem w węglu drzewnym. Ponieważ węgiel drzewny ma dużą powierzchnię, jest w stanie wychwycić większość cząsteczek, które przechodzą przez niego o określonej wielkości (większej niż woda i formamid). Aby wyekstrahować adeninę z adeniny zaadsorbowanej na węglu drzewnym, na strukturę węgiel aktywny-adenina wlewa się gazowy amoniak rozpuszczony w wodzie (wodny amoniak), aby uwolnić adeninę do roztworu amoniak-woda. Roztwór zawierający wodę, amoniak i adeninę pozostawia się następnie do wyschnięcia na powietrzu, przy czym adenina traci rozpuszczalność z powodu utraty gazowego amoniaku, który wcześniej uczynił roztwór zasadowym i zdolnym do rozpuszczania adeniny, powodując w ten sposób jego krystalizację w czysty biały proszek które można przechowywać.
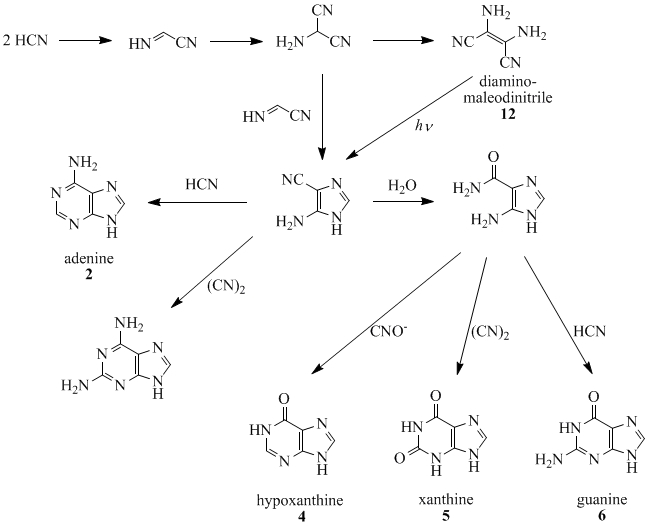
Oro, Orgel i współpracownicy wykazali, że cztery cząsteczki HCN tetrameryzują, tworząc diaminomaleodynitryl ( 12 ), który można przekształcić w prawie wszystkie naturalnie występujące puryny. Na przykład pięć cząsteczek HCN skrapla się w reakcji egzotermicznej, tworząc adeninę , zwłaszcza w obecności amoniaku.
Synteza puryn Traubego (1900) jest klasyczną reakcją (nazwaną na cześć Wilhelma Traubego ) między aminą -podstawioną pirymidyną a kwasem mrówkowym .
Prebiotyczna synteza rybonukleozydów purynowych
Aby zrozumieć, jak powstało życie , potrzebna jest wiedza o szlakach chemicznych, które umożliwiają tworzenie kluczowych elementów budulcowych życia w prawdopodobnych warunkach prebiotycznych . Nam i in. wykazali bezpośrednią kondensację nukleozasad purynowych i pirymidynowych z rybozą w celu uzyskania rybonukleozydów w wodnych mikrokropelkach, co jest kluczowym etapem prowadzącym do powstania RNA. Również wiarygodny prebiotyczny proces syntezy rybonukleozydów purynowych został przedstawiony przez Beckera i in.
Zobacz też
- Purinony
- Pirymidyna
- Proste pierścienie aromatyczne
- Przemiana
- Transwersja
- Dna moczanowa , zaburzenie metabolizmu puryn
- Adenina
- Guanina