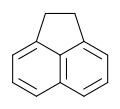
acenaften
|
|

|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
1,2-dihydroacenaftylen |
|
|
Systematyczna nazwa IUPAC
Tricyklo[6.3.1.0 4,12 ]dodeka-1(12),4,6,8,10-pentaen |
|
| Inne nazwy 1,8-etylenonaftalen peri -etylenonaftalen naftylenoetylen tricyklo[6.3.1.0 4,12 ]dodekapentaen |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.001.336 |
| Numer WE |
|
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS |
|
| UNII | |
| Numer ONZ | 3077 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 12 H 10 | |
| Masa cząsteczkowa | 154,212 g·mol -1 |
| Wygląd | Biały lub jasnożółty krystaliczny proszek |
| Gęstość | 1,024 g/ cm3 |
| Temperatura topnienia | 93,4 ° C (200,1 ° F; 366,5 K) |
| Temperatura wrzenia | 279 ° C (534 ° F; 552 K) |
| 0,4 mg/100 ml | |
| Rozpuszczalność w etanolu | niewielki |
| Rozpuszczalność w chloroformie | niewielki |
| Rozpuszczalność w benzenie | bardzo rozpuszczalny |
| Rozpuszczalność w kwasie octowym | rozpuszczalny |
| -.709·10-6 cm 3 / g | |
| Termochemia | |
|
Pojemność cieplna ( C )
|
190,4 J mol -1 K -1 |
|
Standardowa entropia molowa ( S ⦵ 298 ) |
188,9 J mol -1 K -1 |
|
Standardowa entalpia formowania (Δ f H ⦵ 298 ) |
70,3 kJ/mol |
| Zagrożenia | |
| NFPA 704 (ognisty diament) | |
| Punkt zapłonu | 135 ° C (275 ° F; 408 K) |
| > 450 ° C (842 ° F; 723 K) | |
| Karta charakterystyki (SDS) | ICSC 1674 |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Acenaften to wielopierścieniowy węglowodór aromatyczny (WWA) składający się z naftalenu z mostkiem etylenowym łączącym pozycje 1 i 8. Jest to bezbarwne ciało stałe. Smoła węglowa zawiera około 0,3% tego związku.
Produkcja i reakcje
Acenaften został po raz pierwszy przygotowany ze smoły węglowej przez Marcellina Berthelota . Później Berthelot i Bardy zsyntetyzowali związek przez cyklizację α-etylonaftalenu. Na skalę przemysłową wciąż otrzymuje się go ze smoły węglowej wraz z jego pochodną acenaftylenem (i wieloma innymi związkami).
Podobnie jak inne areny , acenaften tworzy kompleksy z centrami metali o niskiej wartościowości. Jednym z przykładów jest (η6 - acenaften)Mn(CO) 3 ] + .
Używa
Stosowany jest na dużą skalę do otrzymywania bezwodnika dikarboksylowego naftalenu, który jest prekursorem barwników i rozjaśniaczy optycznych . Bezwodnik dikarboksylowy naftalenu jest prekursorem dibezwodnika perylenotetrakarboksylowego , prekursorem kilku komercyjnych pigmentów i barwników .

