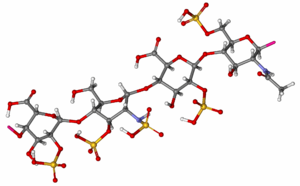
Enoksaparyna sodowa
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Lovenox, Clexane, Xaparin i inne |
| leki biopodobne | Arovi, Inclunox, Inclunox HP, Inhixa, Noromby, Noromby HP, Redesca, Redesca HP, Thorinane |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a696006 |
| Dane licencyjne |
|
| Kategoria ciąży |
|
Drogi podania |
Podskórnie , dożylnie |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Okres półtrwania w fazie eliminacji | 4,5 godziny |
| Identyfikatory | |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| Bank Leków | |
| ChemSpider |
|
| UNII | |
| KEGG | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA | 100.029.698 |
| Dane chemiczne i fizyczne | |
| Formuła | ( C 26H 40N 2O 36S 5 ) rz _ _ |
| Masa cząsteczkowa | 4500 g/mol (średnio) |
|
| |
Enoksaparyna sodowa , sprzedawana między innymi pod marką Lovenox , jest lekiem przeciwzakrzepowym (rozrzedzającym krew). Jest stosowany w leczeniu i profilaktyce zakrzepicy żył głębokich (ZŻG) i zatorowości płucnej (ZP), w tym w czasie ciąży i po niektórych rodzajach zabiegów chirurgicznych. Jest również stosowany u osób z ostrym zespołem wieńcowym (ACS) i zawałem serca . Podaje się go we wstrzyknięciu tuż pod skórę lub do żyły . Jest również stosowany podczas hemodializy .
Częste działania niepożądane obejmują krwawienie, gorączkę i obrzęk nóg . Krwawienie może być poważne, zwłaszcza u osób poddawanych nakłuciu lędźwiowemu . Stosowanie w czasie ciąży wydaje się być bezpieczne dla dziecka. Enoksaparyna należy do rodziny leków heparyny drobnocząsteczkowej .
Enoksaparyna została po raz pierwszy wyprodukowana w 1981 roku i zatwierdzona do użytku medycznego w 1993 roku. Znajduje się na Liście Podstawowych Leków Światowej Organizacji Zdrowia . Enoksaparyna jest sprzedawana pod kilkoma markami i jest dostępna jako lek generyczny . Enoksaparyna jest wytwarzana z heparyny . W 2020 roku był to 350. najczęściej przepisywany lek w Stanach Zjednoczonych, z ponad 500 tysiącami recept.
Zastosowania medyczne
- Leczenie niestabilnej dławicy piersiowej (UA) i zawału mięśnia sercowego bez załamka Q (NQMI), podawane jednocześnie z aspiryną
- Profilaktyka ZŻG i zatorowości płucnej u chorych obłożnie chorych
- Profilaktyka ZŻG w operacjach endoprotezoplastyki stawu kolanowego
- Profilaktyka ZŻG w operacjach endoprotezoplastyki stawu biodrowego
- Profilaktyka ZŻG w chirurgii jamy brzusznej
- Leczenie DVT z lub bez zatorowości płucnej
- Leczenie szpitalnego pacjenta z zakrzepicą żył głębokich z zawałem mięśnia sercowego z uniesieniem odcinka ST (STEMI)
- Leczenie pomostowe dla osób z INR poniżej zakresu terapeutycznego
Monitorowanie
Enoksaparyna ma przewidywalne wchłanianie, biodostępność i dystrybucję, dlatego zwykle nie prowadzi się monitorowania. Istnieją jednak przypadki, w których monitorowanie może być korzystne dla szczególnych populacji, na przykład osób z niewydolnością nerek lub osób otyłych. W takim przypadku można zmierzyć jednostki anty-Xa i odpowiednio dostosować dawkowanie.
Środek odwracający
Siarczan protaminy jest mniej skuteczny w odwracaniu enoksaparyny w porównaniu z heparyną , z maksymalną neutralizacją około 60% efektu anty-Xa.
Ciąża
- Enoksaparyna jest lekiem FDA kategorii ciąży B, co oznacza, że enoksaparyna nie powinna szkodzić nienarodzonemu dziecku, gdy jest stosowana w czasie ciąży. To stwierdzenie jest oparte na badaniach rozrodczości z udziałem ciężarnych szczurów i królików. nie wad wrodzonych ani toksycznego wpływu enoksaparyny na nienarodzony płód. Jednak reakcja człowieka na enoksaparynę może różnić się od reakcji małego zwierzęcia, dlatego enoksaparynę należy stosować w czasie ciąży tylko w przypadku zdecydowanej potrzeby.
- Enoksaparyna nie przenika przez łożysko, dlatego jest mało prawdopodobne, aby nienarodzone dziecko było narażone na jej działanie.
- Kobiety stosujące enoksaparynę w czasie ciąży zgłaszały przypadki zgonów płodów, ale nie jest jasne, czy enoksaparyna spowodowała te zgony.
- Kobieta w ciąży przyjmująca enoksaparynę powinna być regularnie monitorowana pod kątem krwawień i/lub „nadmiernej antykoagulacji”, zwłaszcza gdy zbliża się termin porodu. Ryzyko krwotoku podczas porodu jest większe, jeśli dana osoba nadal stosuje enoksaparynę, co może zagrozić życiu dziecka i (lub) matki.
- Wielodawkowe fiolki markowej enoksaparyny (Lovenox) zawierają 15 mg alkoholu benzylowego na 1 ml jako środek konserwujący. Wcześniaki, którym podawano duże ilości alkoholu benzylowego (99–405 mg/kg mc./dobę) doświadczały „zespołu sapania”.
- Chociaż enoksaparynę stosuje się w celu zapobiegania zakrzepom krwi, sama ciąża może zwiększyć ryzyko zakrzepów u kobiety.
Skutki uboczne
Niezbyt często (<1%)
- U osób z niestabilną dusznicą bolesną lub zawałem mięśnia sercowego bez załamka Q: Migotanie
- przedsionków , niewydolność serca , obrzęk płuc, zapalenie płuc : ≥ 0,5%v
Często (>1%)
- Małopłytkowość , tj. może być związana z trombocytopenią wywołaną przez heparynę (0,5-5,0% osób leczonych przez co najmniej pięć dni)
- aminotransferaz w surowicy : 5,9%-6,1%
- U osób poddawanych zabiegom chirurgicznym w obrębie jamy brzusznej lub jelita grubego:
- Krwawienie, niedokrwistość, wybroczyny : ≥ 2%
- U osób poddawanych alloplastyce stawu biodrowego lub kolanowego:
- Gorączka, nudności, niedokrwistość , obrzęki, obrzęki obwodowe: ≥ 2%
- U osób z poważnymi ograniczeniami ruchowymi podczas ostrej choroby:
- Duszność , małopłytkowość, splątanie, biegunka, nudności: ≥ 2%
- U osób leczonych z powodu zakrzepicy żył głębokich:
- krwotok w miejscu wstrzyknięcia, ból w miejscu wstrzyknięcia, krwiomocz : ≥ 2%
Częstotliwość w trakcie badania
- Reakcje miejscowe: miejscowe podrażnienie, ból, krwiak , wybroczyny, rumień
- Krwawienie
- Hiperkaliemia
- zapalenie transamin
- Krwotok
Ostrzeżenie w pudełku
FDA wydała zmianę ostrzeżenia pudełkowego dotyczącego enoksaparyny w październiku 2013 r. Wersja ta zaleca zachowanie ostrożności podczas zakładania i usuwania cewników rdzeniowych u osób przyjmujących enoksaparynę w celu nakłucia lędźwiowego lub znieczulenia neuroosiowego . Konieczne może być opóźnienie podania leków przeciwzakrzepowych u tych osób w celu zmniejszenia ryzyka wystąpienia krwiaków podpajęczynówkowych lub nadtwardówkowych, które mogą objawiać się trwałym lub długotrwałym porażeniem . Osoby z grupy ryzyka wystąpienia krwiaków mogą zgłaszać się z założonymi na stałe cewnikami zewnątrzoponowymi, jednoczesnym stosowaniem leków nasilających stany krwawienia, takich jak niesteroidowe leki przeciwzapalne (NLPZ) , lub przebytymi w przeszłości nakłuciami zewnątrzoponowymi lub rdzeniowymi, urazami kręgosłupa lub deformacjami kręgosłupa . FDA zaleca monitorowanie osób z grupy ryzyka pod kątem krwawień i zmian neurologicznych.
Farmakologia
Mechanizm akcji
Enoksaparyna wiąże się i wzmacnia antytrombinę (krążący antykoagulant), tworząc kompleks, który nieodwracalnie inaktywuje czynnik krzepnięcia Xa . Wykazuje mniejszą aktywność wobec czynnika IIa (trombiny) w porównaniu z heparyną niefrakcjonowaną (HNF) ze względu na małą masę cząsteczkową.
Farmakokinetyka
Wchłanianie: Biodostępność (wstrzyknięcie podskórne) ~ 100%
Dystrybucja: Objętość dystrybucji (aktywność przeciw czynnikowi Xa) = 4,3 litra
Metabolizm: Enoksaparyna jest metabolizowana w wątrobie do związków o małej masie cząsteczkowej na drodze odsiarczania i depolimeryzacji.
Eliminacja: Okres półtrwania pojedynczej dawki enoksaparyny we wstrzyknięciu podskórnym wynosi 4,5 godziny. Około 10–40% aktywnych i nieaktywnych fragmentów z pojedynczej dawki jest wydalane przez nerki. U osób z zaburzeniami czynności nerek konieczne jest dostosowanie dawki w zależności od czynności nerek.
Klasa narkotykowa
Enoksaparyna należy do klasy leków znanych jako heparyny drobnocząsteczkowe. Inne leki z tej klasy to dalteparyna , fondaparynuks i tinzaparyna .
leki biopodobne
We wrześniu 2016 roku Inhixa i Thorinane zostały dopuszczone do użytku w Unii Europejskiej. Thorinane został wycofany z rynku w październiku 2019 roku.
W marcu 2017 r. Enoxaparin BECAT, Laboratorios ROVI (Hiszpania) uzyskał pozwolenie na dopuszczenie do obrotu w dwudziestu sześciu krajach Europy. Produkt jest już dostępny w Europie.
W październiku 2020 r. Noromby i Noromby HP zostały dopuszczone do użytku medycznego w Kanadzie.
W listopadzie 2020 r. i Inclunox HP zostały dopuszczone do użytku medycznego w Kanadzie.
W grudniu 2020 r. Redesca i Redesca HP zostały dopuszczone do użytku medycznego w Kanadzie.
Linki zewnętrzne
- „Enoksaparyna sodowa” . Portal informacyjny o lekach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.