Ester progestagenu

Ester progestagenu jest estrem progestagenu lub progestagenu ( syntetycznego progestagenu ) . Progestagenem jest progesteron , endogenny hormon płciowy . Estryfikację często stosuje się w celu poprawy farmakokinetyki steroidów , w tym biodostępności po podaniu doustnym , lipofilowości i okresu półtrwania w fazie eliminacji . Ponadto z wstrzyknięciem domięśniowym estry steroidów są często wchłaniane do organizmu wolniej, co pozwala na rzadsze ich podawanie. Wiele (choć nie wszystkie) estrów steroidów działa jako proleki .
Estryfikacja jest szczególnie istotna w przypadku progesteronu, ponieważ sam progesteron wykazuje bardzo słabą farmakokinetykę po podaniu doustnym i dlatego jest nieskuteczny przy przyjmowaniu doustnym. Niemodyfikowany, ma okres półtrwania w fazie eliminacji wynoszący zaledwie 5 minut i jest prawie całkowicie inaktywowany przez wątrobę podczas metabolizmu pierwszego przejścia . Mikronizacja umożliwiła jednak skuteczność progesteronu po podaniu doustnym, chociaż doustny mikronizowany progesteron został opracowany dopiero w ostatnich latach.
Przykłady ważnych estrów progestagenu obejmują pochodne 17α -hydroksyprogesteronu , octan medroksyprogesteronu , octan megestrolu , octan cyproteronu i kapronian hydroksyprogesteronu , pochodna 19-norprogesteronu octan nomegestrolu oraz pochodne 19-nortestosteronu octan noretysteronu i enantan noretysteronu .
Estry progestagenu
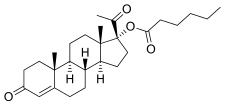
Estrogeny odkryto w 1929 r., a od 1936 r. wprowadzono do użytku klinicznego różne estry estradiolu , takie jak benzoesan estradiolu i dipropionian estradiolu . Mniej więcej w tym czasie wprowadzono także estry testosteronu , takie jak propionian testosteronu i fenylooctan testosteronu . W przeciwieństwie do estradiolu i testosteronu , progesteron okazał się trudniejszy do estryfikacji. W rzeczywistości estryfikacja polega na zastąpieniu grupy hydroksylowej z grupą alkoksylową i w przeciwieństwie do estradiolu i testosteronu, progesteron nie posiada żadnych grup hydroksylowych, więc w rzeczywistości chemiczna estryfikacja samego progesteronu nie jest możliwa. Pierwsze estry progestagenu wprowadzono dopiero w połowie lat pięćdziesiątych XX wieku i były to raczej estry 17α-hydroksyprogesteronu (który w przeciwieństwie do progesteronu ma grupę hydroksylową dostępną do estryfikacji), a nie progesteronu; obejmowały kapronian 17α-hydroksyprogesteronu (Delalutin, Proluton) i octan 17α-hydroksyprogesteronu (Prodroks). Poniższy cytat de Médicis Sajous i in. (1961) szczegółowo opisuje rozwój estrów progestagenu:

W ciągu kilku lat Upjohn zainwestował wiele dziesiątek tysięcy dolarów w wysiłki w celu znalezienia łatwo wchłaniającego się, aktywnego po podaniu doustnym estru progesteronu. Wysiłek zakończył się ograniczonym sukcesem. Znaleziono jeden obiecujący ester, [octan 17α-hydroksyprogesteronu], sprzedawany jako Prodox. Doustnie był bardziej aktywny niż inne preparaty progesteronu dostępne wówczas na rynku, ale po podaniu doustnym nie był tak aktywny, jak oczekiwano. [ potrzebne źródło ] Aby otrzymać lek progestagenowy o pożądanych właściwościach, konieczna okazała się zmiana samej cząsteczki progesteronu. Począwszy od około 1957 roku chemicy zajmujący się sterydami w Upjohn przygotowali serię progesteronów modyfikowanych na różne sposoby, które, jak stwierdzono, zwielokrotniają działanie kortyzonu i hydrokortyzonu. Jedna z modyfikacji — opracowana przez zespół pod kierunkiem dr Johna C. Babcocka — polegała na przyłączeniu atomu węgla i trzech atomów wodoru – grupy metylowej – do węgla 6 w pierwszym pierścieniu jądra steroidu progesteronowego. Podobna modyfikacja była kluczowym krokiem w tworzeniu Medrolu, przeciwzapalnego steroidu typu kortyzonu firmy Upjohn o dużej sile działania. Nowym środkiem progestagennym był [octan 6α-metylo-17α-hydroksyprogesteronu] lub [octan medroksyprogesteronu], który Upjohn zastrzegł znak towarowy Provera. Okazało się, że jest to najsilniejszy lek progestagenny, jaki dotychczas odkryto – setki razy skuteczniejszy po podaniu doustnym niż progesteron i około pięćdziesiąt razy bardziej aktywny po wstrzyknięciu podskórnym. Provera została wprowadzona na rynek w 1959 roku.
Octan medroksyprogesteronu (Provera) wszedł do użytku klinicznego i stał się szeroko rozpowszechniony na rynku, w dużej mierze zastępując estry 17α-hydroksyprogesteronu. Następnie opracowano i wprowadzono różne analogi octanu medroksyprogesteronu, takie jak octan chlormadinonu , octan cyproteronu i octan megestrolu . Wprowadzono także estry progestagenowe innych grup progestyn , w tym pochodne 19-norprogesteronu kapronian gestonoronu , octan segesteronu (nestoron) , octan nomegestrolu i norgestomet (11β-metylo-17α-acetoksy-19-norprogesteron) oraz pochodne 19-nortestosteronu : dioctan etynodiolu , octan noretysteronu , enantan noretysteronu i octan chingestanolu .
Chociaż estry steroidowych androgenów i estrogenów są na ogół same w sobie nieaktywne i działają jako proleki, to samo nie dotyczy wielu estrów progestagenu. Na przykład estry pochodnych 17α-hydroksyprogesteronu, takie jak kapronian hydroksyprogesteronu, octan medroksyprogesteronu i octan cyproteronu, same są bardzo aktywne (w rzeczywistości są znacznie bardziej aktywne niż ich formy nieestryfikowane) i nie są prolekami, tworząc niewiele lub nie tworząc żadnego z nich ich związki macierzyste (w przypadku podanych przykładów hydroksyprogesteron , medroksyprogesteron i cyproteron odpowiednio). Z drugiej strony, estry pochodnych 19-nortestosteronu, takie jak dioctan etynodiolu, octan noretysteronu, enantan noretysteronu i octan kwingestanolu, są prolekami.
Etery progestagenu


Chociaż progesteron nie podlega estryfikacji, posiada grupy ketonowe w pozycjach C3 i C20, dzięki czemu można go eteryfikować ; to znaczy, możliwe są etery progesteronu. Quingestrone (Enol-Luteovis) to eter progesteronu (w szczególności eter 3-cyklopentylowy progesteronu), który został wprowadzony do obrotu we Włoszech jako doustny środek antykoncepcyjny . Quingestron jest odmianą progesteronu o ulepszonej farmakokinetyce, w tym większej sile działania, aktywności po podaniu doustnym, większej lipofilowości i dłuższym okresie półtrwania. Dwa inne progestageny, pentagestron (nigdy nie sprzedawany) i octan pentagestronu (Gestovis, Gestovister) to etery 3-cyklopentyloenolu, odpowiednio, 17α-hydroksyprogesteronu i octanu 17α-hydroksyprogesteronu, podczas gdy eter 3-acetylo-enolu progesteronu (nigdy nie sprzedawany) to 3-acetylenol eter progesteronu.
Chociaż początkowo sądzono, że etery progesteronu, takie jak kwingestron, są prolekami progesteronu, później odkryto, że tak nie jest i zamiast tego kwingestron wydaje się przekształcać bezpośrednio w odpowiednie alkohole, a nie w ketony . Alkohole te są metabolitami progesteronu , takimi jak pregnanolony i pregnanodiole , a ponieważ niektóre z tych metabolitów, na przykład 3β-dihydroprogesteron , mają silne działanie progestagenowe, może to wyjaśniać skuteczność kliniczną eterów progestagenu, takich jak kwingestron, jako progestagenów.
Oksmy progestagenu
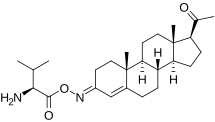
koniugaty oksymów C3 i C20 progesteronu, takie jak karboksymetylooksym progesteronu (3-( O -karboksymetylo)oksym progesteronu; P4-3-CMO), P1-185 (progesteron 3- O- ( L -walina) -E -oksym), EIDD-1723 (progesteron (20E ) -20-[ O -[(fosfonooksy)metylo]oksym] sól sodowa), EIDD-036 (20-oksym progesteronu) i VOLT-02 (struktura chemiczna nieujawniona) , zostały opracowane jako rozpuszczalne w wodzie proleki progesteronu i neurosteroidów, chociaż żaden z nich nie zakończył badań klinicznych ani nie został jeszcze wprowadzony na rynek.
Niektóre progestyny 19-nortestosteronu, w tym dostępne na rynku progestyny norgestimat i norelgestromin oraz niedopuszczony do obrotu progestagen oksym octanu noretysteronu , są oksymami C3, chociaż same mają silne działanie progestagenne i niekoniecznie są prolekami odpowiednich ketonów .
Zobacz też
- Lista estrów progestagenu
- Ester steroidowy
- Ester estrogenu
- Ester androgenu
- Lista estrów steroidowych
- Lista progestagenów
Linki zewnętrzne
-
 Media związane z estrami progestagenu w Wikimedia Commons
Media związane z estrami progestagenu w Wikimedia Commons