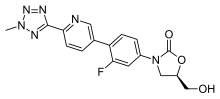
Tedyzolid
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Sivextro |
| Inne nazwy | TR-700 |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a614038 |
Drogi podania |
Doustnie , dożylnie |
| Kod ATC | |
| Status prawny | |
| Status prawny |
|
| Dane farmakokinetyczne | |
| Biodostępność | 91% |
| Wiązanie białek | 70–90% |
| Okres półtrwania w fazie eliminacji | 12 godzin |
| Wydalanie | Kał |
| Identyfikatory | |
| |
| Numer CAS |
|
| Identyfikator klienta PubChem | |
| Bank Leków | |
| ChemSpider | |
| UNII |
|
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA | 100.249.430 |
| Dane chemiczne i fizyczne | |
| Formuła | C 17 H 15 F N 6 O 3 |
| Masa cząsteczkowa | 370,344 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
Tedyzolid (dawniej torezolid , nazwa handlowa Sivextro ) jest antybiotykiem z grupy oksazolidynonów . Fosforan tedyzolidu jest prolekiem w postaci estru fosforanowego substancji czynnej tedyzolidu. Został opracowany przez Cubist Pharmaceuticals po przejęciu Trius Therapeutics (autor: Dong-A Pharmaceuticals) i jest sprzedawany do leczenia ostrych bakteryjnych infekcji skóry i struktur skóry (znanych również jako powikłane infekcje skóry i struktury skóry (cSSSI)) .
Najczęstsze działania niepożądane to nudności (mdłości), ból głowy, biegunka i wymioty. Te działania niepożądane miały na ogół łagodne lub umiarkowane nasilenie.
Tedyzolid został dopuszczony do użytku medycznego w Stanach Zjednoczonych w czerwcu 2014 r., a do użytku medycznego w Unii Europejskiej w marcu 2015 r.
Zastosowania medyczne
Tedyzolid został zatwierdzony przez Amerykańską Agencję ds. Żywności i Leków (FDA) w dniu 20 czerwca 2014 r. jako wskazanie do leczenia ostrych bakteryjnych zakażeń skóry i struktur skóry (ABSSSI) wywołanych przez niektóre wrażliwe bakterie, w tym Staphylococcus aureus (w tym oporne na metycylinę szczepy, MRSA i szczepy wrażliwe na metycylinę), różne gatunki Streptococcus ( S. pyogenes , S. agalactiae i grupa S. anginosus , w tym S. anginosus , S. intermedius i S. constellatus ) oraz Enterococcus faecalis . Tedyzolid jest pochodną oksazolidynonu drugiej generacji , która jest od 4 do 16 razy silniejsza przeciwko gronkowcom i enterokokom w porównaniu z linezolidem . Zalecana dawka w leczeniu wynosi 200 mg raz na dobę przez łącznie sześć dni, doustnie (z posiłkiem lub bez) lub we wstrzyknięciu dożylnym (jeśli pacjent ma więcej niż 18 lat).
W Unii Europejskiej tedyzolid jest wskazany w leczeniu ostrych bakteryjnych zakażeń skóry i struktur skóry (ABSSSI) u dorosłych.
Mechanizm akcji
Fosforan tedyzolidu (TR-701) jest prolekiem aktywowanym przez fosfatazy osocza lub jelit do tedyzolidu (TR-700) po podaniu leku doustnie lub dożylnie. Po aktywacji tedyzolid wywiera działanie bakteriostatyczne na drobnoustroje poprzez hamowanie syntezy białek poprzez wiązanie się z 50S rybosomu (w miejscu akceptorowym) bakterii.
Badania kliniczne
Tedyzolid udowodnił swoją niegorszość w stosunku do linezolidu w dwóch badaniach III fazy, znanych jako badania ESTABLISH.
Tedizolid jest drugim lekiem zatwierdzonym przez FDA na mocy nowego prawa federalnego Generating Antibiotic Incentives Now (znanego jako ustawa GAIN). Nowe antybiotyki produkowane zgodnie z tą nową ustawą zostaną zaprojektowane jako kwalifikowany produkt na choroby zakaźne (QIDP), co umożliwi przyspieszoną ocenę przez FDA i dodatkowe pięć lat wyłączności rynkowej.
Niekorzystne skutki
Najczęstszymi działaniami niepożądanymi stwierdzonymi w badaniach klinicznych były nudności, ból głowy, biegunka, wymioty i zawroty głowy. Stwierdzono również, że tedyzolid ma wpływ na hematologię (na krew), co wykazano w fazy I, w których pacjenci narażeni na dawki dłuższe niż 6 dni wykazywali możliwy wpływ dawki i czasu trwania na parametry hematologiczne. Jego bezpieczeństwo u pacjentów ze zmniejszoną liczbą białych krwinek nie zostało ustalone. neuropatii obwodowej i nerwu wzrokowego , podobnie jak inni członkowie grupy oksazolidynonów.
Linki zewnętrzne
- „Tedyzolid” . Portal informacyjny o lekach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Fosforan tedyzolidu” . Portal informacyjny o lekach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Wstrzyknięcie tedyzolidu: informacje o lekach MedlinePlus” . MedlinePlus .
