neomycyna
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Neo-rx |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a682274 |
Drogi podania |
Miejscowy , doustny |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | Nic |
| Wiązanie białek | Nie dotyczy |
| Metabolizm | Nie dotyczy |
| Okres półtrwania w fazie eliminacji | 2 do 3 godzin |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| Bank Leków | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Karta informacyjna ECHA | 100.014.333 |
| Dane chemiczne i fizyczne | |
| Formuła | C 23 H 46 N 6 O 13 |
| Masa cząsteczkowa | 614,650 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
Neomycyna jest antybiotykiem aminoglikozydowym , który wykazuje działanie bakteriobójcze na Gram-ujemne bakterie tlenowe i niektóre bakterie beztlenowe, u których nie rozwinęła się jeszcze oporność. Na ogół nie jest skuteczny wobec Gram-dodatnich i beztlenowych pałeczek Gram-ujemnych. Neomycyna występuje w preparatach doustnych i miejscowych, w tym w kremach, maściach i kroplach do oczu. Neomycyna należy do grupy antybiotyków aminoglikozydowych , które zawierają dwa lub więcej aminocukrów połączonych wiązaniami glikozydowymi .
Neomycyna została odkryta w 1949 roku przez mikrobiologa Selmana Waksmana i jego ucznia Huberta Lechevaliera z Rutgers University . Neomycyna została dopuszczona do użytku medycznego w 1952 r. Uniwersytet Rutgers uzyskał patent na neomycynę w 1957 r.
Odkrycie
Neomycyna została odkryta w 1949 roku przez mikrobiologa Selmana Waksmana i jego ucznia Huberta Lechevaliera z Rutgers University . Jest naturalnie wytwarzany przez bakterie Streptomyces fradiae . Synteza wymaga określonych warunków odżywczych w stacjonarnych lub zanurzonych warunkach tlenowych. Związek jest następnie izolowany i oczyszczany z bakterii.
Zastosowania medyczne
Neomycyna jest zwykle stosowana jako preparat miejscowy , taki jak Neosporin ( neomycyna/polimyksyna B/bacytracyna ). Antybiotyk można również podawać doustnie, w takim przypadku zwykle łączy się go z innymi antybiotykami. Neomycyna nie wchłania się z przewodu pokarmowego i była stosowana jako środek zapobiegawczy w przypadku encefalopatii wątrobowej i hipercholesterolemii . Zabijając bakterie w przewodzie pokarmowym, neomycyna utrzymuje niski poziom amoniaku i zapobiega encefalopatii wątrobowej, zwłaszcza przed operacjami żołądkowo-jelitowymi .
Waksman i Lechevalier pierwotnie zauważyli, że neomycyna była aktywna przeciwko bakteriom opornym na streptomycynę, jak również Mycobacterium tuberculosis , czynnikowi wywołującemu gruźlicę . Neomycynę stosowano również w leczeniu przerostu bakteryjnego jelita cienkiego . Neomycyny nie podaje się we wstrzyknięciach, ponieważ jest wyjątkowo nefrotoksyczna (uszkadzająca czynność nerek), nawet w porównaniu z innymi aminoglikozydami . Wyjątkiem jest sytuacja, gdy neomycyna jest zawarta w małych ilościach jako środek konserwujący w niektórych szczepionkach – zwykle 25 μg na dawkę.
Widmo
Podobnie jak inne aminoglikozydy, neomycyna wykazuje doskonałą aktywność wobec bakterii Gram-ujemnych i jest częściowo skuteczna wobec bakterii Gram-dodatnich . Jest stosunkowo toksyczny dla ludzi, a reakcje alergiczne są odnotowywane jako częsta reakcja niepożądana (patrz: nadwrażliwość ). Lekarze czasami zalecają stosowanie maści antybiotykowych bez neomycyny, takich jak Polysporin . Poniżej przedstawiono na minimalne stężenie hamujące (MIC) dla kilku bakterii Gram-ujemnych o znaczeniu medycznym.
- Enterobacter cloacae : >16 μg/ml
- Escherichia coli : 1 μg/ml
- Proteus vulgaris : 0,25 μg/ml
Skutki uboczne
W latach 2005–2006 neomycyna była piątym najczęściej występującym alergenem w wynikach testów płatkowych (10,0%). Jest również znanym kwasu gamma -aminomasłowego GABA i może być odpowiedzialny za drgawki i psychozy. Podobnie jak inne aminoglikozydy, wykazano, że neomycyna jest ototoksyczna , powodując szum w uszach , utratę słuchu i problemy z układem przedsionkowym u niewielkiej liczby pacjentów. Pacjenci z istniejącym szumem w uszach lub niedosłuchem czuciowo-nerwowym powinni porozmawiać z lekarzem o ryzyku i skutkach ubocznych przed przyjęciem tego leku.
Biologia molekularna
Działalność
Działanie przeciwbakteryjne neomycyny wynika z jej wiązania z podjednostką 30S rybosomu prokariotycznego , gdzie hamuje prokariotyczną translację mRNA.
Neomycyna wykazuje również wysokie powinowactwo wiązania z 4,5-bisfosforanem fosfatydyloinozytolu (PIP2), fosfolipidowym składnikiem błon komórkowych.
Opór
Oporność na neomycynę jest nadawana przez jeden z dwóch genów kinazy kanamycyny . Geny nadające oporność na neomycynę są zwykle zawarte w plazmidach DNA stosowanych do ustanowienia stabilnych linii komórkowych ssaków wykazujących ekspresję sklonowanych białek w hodowli. Wiele dostępnych w handlu plazmidów do ekspresji białek zawiera neo -oporności jako marker selekcyjny .
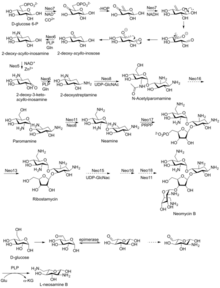
Szlak biosyntetyczny
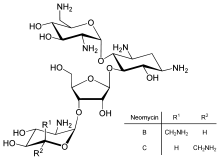
Neomycynę po raz pierwszy wyizolowano ze Streptomyces fradiae i Streptomyces albogriseus w 1949 r. (NBRC 12773). Neomycyna jest mieszaniną neomycyny B (framycetyny); i jej epimer neomycyna C, ten ostatni składnik stanowi około 5–15% mieszaniny. Jest związkiem zasadowym, który jest najbardziej aktywny przy odczynie zasadowym. Jest również termostabilny i rozpuszczalny w wodzie (nierozpuszczalny w rozpuszczalnikach organicznych). Neomycyna ma dobrą aktywność przeciwko Gram-dodatnim i Gram-ujemnym , ale jest ototoksyczna . Jego stosowanie jest więc ograniczone do doustnego leczenia infekcji jelitowych.
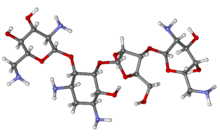
Neomycyna B składa się z czterech połączonych ugrupowań: D -neozaminy, 2-deoksystreptaminy (2-DOS), D -rybozy i L -neozaminy.
Neomycyna A, zwana także neaminą, zawiera D -neozaminę i 2-deoksystreptaminę. Za biosyntezę neamin odpowiada sześć genów: gen DOIS (btrC, neo7); L-glutamina: gen aminotransferazy DOI (btrS, neo6); przypuszczalny gen glikozylotransferazy (btrM, neo8); przypuszczalny gen aminotransferazy (podobny do glutaminianu-1-semialdehydu 2,1-aminomutazy) (btrB, neo18); domniemany gen dehydrogenazy alkoholowej (btrE, neo5); i inny domniemany gen dehydrogenazy (podobny do dehydrogenazy chorynowej i pokrewnych flawoprotein) (btrQ, neo11). Deacetylaza działająca w celu usunięcia grupy acetylowej z ugrupowań N-acetyloglukozaminy aminoglikozydu półprodukty (Neo16) pozostają do wyjaśnienia (sekwencja podobna do BtrD).
Następnie następuje przyłączenie D -rybozy poprzez rybozylację neaminy przy użyciu 5-fosforybozylo-1-difosforanu (PRPP) jako donora rybozylu (BtrL, BtrP); gen glikozylotransferazy (potencjalne homologi RibF, LivF, Parf) (Neo15).
Neosamina B ( L -neosamina B) jest najprawdopodobniej biosyntetyzowana w taki sam sposób jak neosamina C ( D -niosamina) w biosyntezie neaminy, ale z dodatkowym etapem epimeryzacji wymaganym w celu uwzględnienia obecności epimerycznej neosaminy B w neomycynie B.
Neomycyna C może ulegać syntezie enzymatycznej z rybostamycyny.
Kompozycja
Standardowa neomycyna składa się z kilku pokrewnych związków, w tym neomycyny A (neaminy), neomycyny B (framycetyny), neomycyny C i kilku mniejszych związków występujących w znacznie mniejszych ilościach. Neomycyna B jest najbardziej aktywnym składnikiem neomycyny, następnie neomycyna C i neomycyna A. Neomycyna A jest nieaktywnym produktem degradacji izomerów C i B. Ilości tych składników w neomycynie różnią się od partii do partii, w zależności od producenta i procesu produkcyjnego.
Wiązanie DNA
Aminoglikozydy, takie jak neomycyna, są znane ze swojej zdolności do wiązania się z dupleksem RNA z wysokim powinowactwem. Stała asocjacji neomycyny z RNA w miejscu A mieści się w 109 M -1 . Jednak ponad 50 lat po jego odkryciu jego właściwości wiązania DNA były nadal nieznane. Wykazano, że neomycyna indukuje stabilizację termiczną potrójnego DNA, mając jednocześnie niewielki lub prawie żaden wpływ na stabilizację dupleksu B-DNA. Wykazano również, że neomycyna wiąże się ze strukturami, które przyjmują strukturę w kształcie litery A, a jednym z nich jest tripleks DNA. Neomycyna obejmuje również tworzenie hybrydowego tripleksu DNA:RNA.