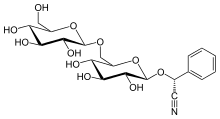
amigdalina
|
|

|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
(2R ) -[(6- O -β- D -glukopiranozylo-β- D -glukopiranozylo)oksy]fenyloacetonitryl
|
|
|
Preferowana nazwa IUPAC
(2R ) -fenylo{[(2R , 3R , 4S , 5S , 6R ) -3,4,5-trihydroksy-6-({[( 2R , 3R , 4S , 5S ,6 R )-3,4,5-trihydroksy-6-(hydroksymetylo)oksan-2-ylo]oksy}metylo)oksan-2-ylo]oksy}acetonitryl |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 66856 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.045.372 |
| Numer WE |
|
| Siatka | amigdalina |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 20 H 27 N O 11 | |
| Masa cząsteczkowa | 457.429 |
| Temperatura topnienia | 223-226 ° C (świeci) |
| H2O: 0,1 g/ml gorący, klarowny do bardzo lekko mętnego, bezbarwny | |
| Zagrożenia | |
| Oznakowanie GHS : | |

|
|
| Ostrzeżenie | |
| H302 | |
| P264 , P270 , P301+P312 , P330 , P501 | |
| NFPA 704 (ognisty diament) | |
| Karta charakterystyki (SDS) | A6005 |
| Związki pokrewne | |
|
Związki pokrewne
|
Vicianin , letril , prunasin , sambunigrin |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Amigdalina (ze starogreckiego : ἀμυγδαλή amygdalē „migdał”) jest naturalnie występującym związkiem chemicznym występującym w wielu roślinach, zwłaszcza w nasionach (jądrach) moreli , gorzkich migdałów , jabłek , brzoskwiń , wiśni i śliwek .
Amigdalina jest klasyfikowana jako glikozyd cyjanogenny , ponieważ każda cząsteczka amigdaliny zawiera grupę nitrylową , która może zostać uwolniona jako toksyczny anion cyjankowy pod działaniem beta-glukozydazy . Jedzenie amigdaliny spowoduje uwolnienie cyjanku w ludzkim ciele i może prowadzić do zatrucia cyjankiem .
Od wczesnych lat pięćdziesiątych zarówno amigdalina, jak i pochodna chemiczna o nazwie letril były promowane jako alternatywne metody leczenia raka , często pod błędną nazwą witaminy B17 ( ani amigdalina, ani letril nie są witaminami ). Badania naukowe wykazały, że są one nie tylko nieskuteczne klinicznie w leczeniu raka, ale także potencjalnie toksyczne lub śmiertelne, gdy są przyjmowane doustnie z powodu zatrucia cyjankiem . Promocja letrilu w leczeniu raka została opisana w literaturze medycznej jako kanoniczny przykład znachorstwa i jako „najsprytniejsza, najbardziej wyrafinowana iz pewnością najbardziej dochodowa promocja znachorów raka w historii medycyny”.
Chemia
Amigdalina jest cyjanogennym glikozydem pochodzącym z aromatycznego aminokwasu fenyloalaniny . Amigdalina i prunazyna są powszechne wśród roślin z rodziny Rosaceae , zwłaszcza rodzaju Prunus , Poaceae (trawy), Fabaceae (rośliny strączkowe) oraz w innych roślinach jadalnych, w tym w siemieniu lnianym i manioku . W obrębie tych roślin amigdalina i enzymy niezbędne do jej hydrolizy są magazynowane w oddzielnych miejscach i mieszają się dopiero w wyniku uszkodzenia tkanek. Zapewnia to naturalny system obronny.
Amigdalina zawarta jest w pestkach owoców pestkowych , takich jak migdały , morela (14 g/kg), brzoskwinia (6,8 g/kg) i śliwka (4–17,5 g/kg w zależności od odmiany), a także w nasionach jabłka (3 g/kg). Benzaldehyd uwalniany z amigdaliny zapewnia gorzki smak. Ze względu na różnicę w genie recesywnym zwanym słodkim jądrem [Sk] , mniej amigdaliny jest obecne w niegorzkich (lub słodkich) migdałach niż w gorzkich migdałach . W jednym badaniu stężenie amigdaliny z gorzkich migdałów wahało się od 33 do 54 g/kg w zależności od odmiany; odmiany półgorzkie średnio 1 g/kg, a odmiany słodkie średnio 0,063 g/kg ze znaczną zmiennością w zależności od odmiany i regionu uprawy.
W przypadku jednej metody izolowania amigdaliny pestki są usuwane z owoców i rozbijane w celu uzyskania jąder, które są suszone na słońcu lub w piecach. Jądra gotuje się w etanolu ; po odparowaniu roztworu i dodaniu eteru dietylowego amigdalina wytrąca się w postaci drobnych białych kryształków. Naturalna amigdalina ma konfigurację ( R ) na chiralnym centrum fenylowym. W łagodnych warunkach zasadowych to stereogeniczne centrum izomeryzuje; ( S )-epimer nazywa się neoamygdaliną . Chociaż zsyntetyzowana wersja amigdaliny jest ( R )-epimerem, centrum stereogeniczne przyłączone do grup nitrylowych i fenylowych łatwo epimeryzuje, jeśli producent nie przechowuje związku prawidłowo.
Amigdalina jest hydrolizowana przez β-glukozydazę jelitową (emulsynę) i beta-glukozydazę amigdaliny (amygdalazę), dając gentiobiozę i L - mandelonitryl . Gentiobioza jest dalej hydrolizowana, dając glukozę , podczas gdy mandelonitryl ( cyjanohydryna benzaldehydu ) rozkłada się , dając benzaldehyd i cyjanowodór . Cyjanowodór w wystarczających ilościach ( dopuszczalne dzienne spożycie : ~0,6 mg) powoduje zatrucie cyjankiem, którego śmiertelna dawka doustna wynosi 0,6–1,5 mg/kg masy ciała.
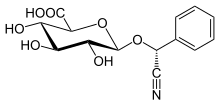
letril
|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
(2S , 3S , 4S , 5R , 6R ) -6-[( R )-cyjano(fenylo)metoksy]-3,4,5-trihydroksyoksano-2-karboksylowy
|
|
| Inne nazwy
L -mandelonitryl-β- D -glukuronid, witamina B 17
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA | 100.045.372 |
|
Identyfikator klienta PubChem
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C14H15NO7 _ _ _ _ _ _ | |
| Masa cząsteczkowa | 309.2714 |
| Temperatura topnienia | 214 do 216 ° C (417 do 421 ° F; 487 do 489 K) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Letril (opatentowany w 1961 r.) jest prostszą półsyntetyczną pochodną amigdaliny. Letril jest syntetyzowany z amigdaliny na drodze hydrolizy. Zwykle preferowanym źródłem komercyjnym są pestki moreli ( Prunus armeniaca ). Nazwa pochodzi od osobnych słów „ lewoskrętny ” i „ mandelonitryl ”. Laevorotatory opisuje stereochemię cząsteczki, podczas gdy mandelonitryl odnosi się do części cząsteczki, z której cyjanek jest uwalniany w wyniku rozkładu. Tabletka letrilu 500 mg może zawierać od 2,5 do 25 mg cyjanowodoru.
Podobnie jak amigdalina, letril ulega hydrolizie w dwunastnicy (odczyn alkaliczny) i jelicie (enzymatycznie) do kwasu D - glukuronowego i L - mandelonitrylu ; ten ostatni hydrolizuje do benzaldehydu i cyjanowodoru, który w wystarczających ilościach powoduje zatrucie cyjankiem .
Twierdzenia dotyczące letrilu opierały się na trzech różnych hipotezach: Pierwsza hipoteza sugerowała, że komórki nowotworowe zawierają obfite beta-glukozydazy, które uwalniają HCN z letrilu poprzez hydrolizę. Normalne komórki były podobno nienaruszone, ponieważ zawierały niskie stężenia beta-glukozydaz i wysokie stężenia rodanu , który przekształca HCN w mniej toksyczny tiocyjanian . Później jednak wykazano, że zarówno komórki rakowe, jak i zdrowe zawierają jedynie śladowe ilości beta-glukozydaz i podobne ilości rodanu.
Drugi sugerował, że po spożyciu amigdalina była hydrolizowana do mandelonitrylu , transportowana w stanie nienaruszonym do wątroby i przekształcana w kompleks beta-glukuronidu, który następnie był przenoszony do komórek nowotworowych, hydrolizowany przez beta-glukuronidazy w celu uwolnienia mandelonitrylu, a następnie HCN. Jednak mandelonitryl dysocjuje do benzaldehydu i cyjanowodoru i nie może być stabilizowany przez glikozylację.
Wreszcie trzeci stwierdził, że letril jest odkrytą witaminą B-17, a ponadto sugeruje, że rak jest wynikiem „niedoboru B-17”. Postulowano, że regularne podawanie w diecie tej formy letrilu faktycznie zapobiegłoby wszystkim zachorowaniom na raka. Nie ma dowodów potwierdzających to przypuszczenie w postaci procesu fizjologicznego, wymagań żywieniowych lub identyfikacji jakiegokolwiek zespołu niedoboru. Termin „witamina B-17” nie jest uznawany przez Komitet ds. Nomenklatury Amerykańskiego Instytutu Witamin Żywienia. Ernst T. Krebs (nie mylić z Hansem Adolfem Krebsem , odkrywcą cyklu kwasu cytrynowego ) oznaczył letril jako witaminę, aby sklasyfikować go raczej jako suplement diety niż środek farmaceutyczny.
Historia letrilu
Wczesne użycie
Amigdalina została po raz pierwszy wyizolowana w 1830 roku z nasion gorzkich migdałów ( Prunus dulcis ) przez Pierre-Jean Robiquet i Antoine Boutron-Charlard. Liebig i Wöhler odkryli trzy produkty hydrolizy amigdaliny: cukier, benzaldehyd i kwas pruski (cyjanowodór, HCN). Późniejsze badania wykazały, że kwas siarkowy hydrolizuje go do D -glukozy , benzaldehydu i kwasu pruskiego; podczas gdy kwas solny daje kwas migdałowy , D -glukozę i amoniak .
W 1845 r. amigdalinę stosowano jako lek na raka w Rosji, aw latach 20. XX wieku w Stanach Zjednoczonych, ale uznano ją za zbyt trującą. W latach pięćdziesiątych rzekomo nietoksyczna, syntetyczna postać została opatentowana do stosowania jako środek konserwujący mięso, a później sprzedawana jako letril do leczenia raka.
Amerykańska Agencja ds. Żywności i Leków zakazała międzystanowego transportu amigdaliny i letrilu w 1977 r. Następnie 27 stanów USA zalegalizowało stosowanie amigdaliny w tych stanach.
Kolejne wyniki
W kontrolowanym, zaślepionym badaniu z 1977 roku letril nie wykazywał większej aktywności niż placebo.
Następnie letril przetestowano na 14 układach nowotworowych bez dowodów na skuteczność. Memorial Sloan-Kettering Cancer Center (MSKCC) stwierdziło, że „letril nie wykazał żadnych korzystnych skutków”. Błędy we wcześniejszym komunikacie prasowym MSKCC zostały podkreślone przez grupę zwolenników letrilu kierowaną przez Ralpha Mossa , byłego urzędnika MSKCC ds. Błędy te uznano za nieistotne z naukowego punktu widzenia, ale Nicholas Wade w Science stwierdził, że „nawet pozory odejścia od ścisłej obiektywności są niefortunne”. Wyniki tych badań zostały opublikowane razem.
Przegląd systematyczny z 2015 roku przeprowadzony przez Cochrane Collaboration wykazał:
Twierdzenia, że letril lub amigdalina mają korzystny wpływ na pacjentów z rakiem, nie są obecnie poparte solidnymi danymi klinicznymi. Istnieje znaczne ryzyko poważnych działań niepożądanych zatrucia cyjankiem po letrilu lub amigdalinie, zwłaszcza po spożyciu doustnym. Stosunek korzyści do ryzyka stosowania letrilu lub amigdaliny w leczeniu raka jest zatem jednoznacznie ujemny.
Autorzy zalecili również, ze względów etycznych i naukowych, aby nie przeprowadzać dalszych badań klinicznych nad letrilem lub amigdaliną.
Ze względu na brak dowodów letril nie został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków ani Komisję Europejską .
Amerykańskie Narodowe Instytuty Zdrowia osobno oceniły dowody i doszły do wniosku, że badania kliniczne amigdaliny wykazały niewielki lub żaden wpływ na raka. Na przykład badanie przeprowadzone w 1982 roku przez Mayo Clinic na 175 pacjentach wykazało, że rozmiar guza zwiększył się u wszystkich pacjentów z wyjątkiem jednego. Autorzy stwierdzili, że „niebezpieczeństwa związane z terapią amigdaliną zostały potwierdzone u kilku pacjentów przez objawy toksyczności cyjanku lub poziomy cyjanku we krwi zbliżające się do śmiertelnego zakresu”.
W badaniu stwierdzono: „Pacjentów narażonych na ten środek należy poinstruować o niebezpieczeństwie zatrucia cyjankiem, a ich poziom cyjanku we krwi powinien być dokładnie monitorowany. Amigdalina (letril) jest toksycznym lekiem, który nie jest skuteczny w leczeniu raka”.
Ponadto „nie zgłoszono żadnych kontrolowanych badań klinicznych (badań porównujących grupy pacjentów otrzymujących nowe leczenie z grupami, które tego nie robią) letrilu”.
Skutkiem ubocznym leczenia letrilem są objawy zatrucia cyjankiem. Objawy te obejmują: nudności i wymioty, ból głowy, zawroty głowy, wiśniowy kolor skóry, uszkodzenie wątroby, nienormalnie niskie ciśnienie krwi, opadającą górną powiekę, problemy z chodzeniem z powodu uszkodzonych nerwów, gorączkę, splątanie, śpiączkę i śmierć.
Europejskiej Agencji Bezpieczeństwa Żywności ds. Zanieczyszczeń w Łańcuchu Żywnościowym zbadał potencjalną toksyczność amigdaliny w pestkach moreli . Panel stwierdził: „Jeśli konsumenci zastosują się do zaleceń stron internetowych promujących spożywanie pestek moreli, ich narażenie na cyjanek znacznie przekroczy” dawkę, która ma być toksyczna. Panel poinformował również, że ostra toksyczność cyjanku wystąpiła u dorosłych, którzy spożyli 20 lub więcej ziaren, au dzieci „pięć lub więcej ziaren wydaje się być toksycznych”.
Rzecznictwo i legalność letrilu
Zwolennicy letrilu twierdzą, że istnieje spisek między amerykańską Agencją ds. Żywności i Leków , przemysłem farmaceutycznym i środowiskiem medycznym, w tym Amerykańskim Stowarzyszeniem Medycznym i Amerykańskim Towarzystwem ds.
Zwolennicy stosowania letrilu zmienili również uzasadnienie jego stosowania, najpierw jako lek na raka, potem jako witaminę, następnie jako część „holistycznego” schematu żywieniowego lub jako lek na ból nowotworowy, między innymi żaden z które mają jakiekolwiek istotne dowody potwierdzające jego użycie.
Pomimo braku dowodów na jego stosowanie, letril zyskał znaczną popularność ze względu na jego szeroką promocję jako „bezbolesnego” leczenia raka jako alternatywy dla operacji i chemioterapii , które mają znaczące skutki uboczne. Stosowanie letrilu doprowadziło do wielu zgonów. Represje FDA i AMA, rozpoczęte w latach 70. XX wieku, skutecznie podniosły ceny na czarnym rynku, odegrały rolę w narracji spiskowej i umożliwiły pozbawionym skrupułów spekulantom wspieranie wielomilionowych imperiów przemytniczych.
Niektórzy amerykańscy pacjenci z rakiem udali się do Meksyku na leczenie tą substancją, na przykład w szpitalu Oasis of Hope w Tijuanie . Aktor Steve McQueen zmarł w Meksyku po operacji usunięcia guza żołądka, po wcześniejszym długotrwałym leczeniu międzybłoniaka opłucnej (raka związanego z narażeniem na działanie azbestu) pod opieką Williama D. Kelleya , dentysty i ortodonty bez licencji, który twierdził, że opracowali leczenie raka obejmujące enzymy trzustkowe, 50 witamin i minerałów dziennie, częste mycie ciała, lewatywy i specjalną dietę, a także letril.
Zwolennicy letrilu w Stanach Zjednoczonych to Dean Burk , były główny chemik laboratorium cytochemicznego National Cancer Institute , oraz krajowy mistrz w siłowaniu się na rękę Jason Vale, który fałszywie twierdził, że jego rak nerki i trzustki został wyleczony przez jedzenie pestek moreli . Vale został skazany w 2004 roku między innymi za oszukańcze marketing letrilu jako lekarstwa na raka. Sąd stwierdził również, że Vale zarobił co najmniej 500 000 dolarów na oszukańczej sprzedaży letrilu.
W latach siedemdziesiątych sprawy sądowe w kilku stanach zakwestionowały uprawnienia FDA do ograniczania dostępu do leków potencjalnie ratujących życie. Ponad dwadzieścia stanów uchwaliło prawa legalizujące stosowanie letrilu. Po jednogłośnym orzeczeniu Sądu Najwyższego w sprawie Stany Zjednoczone przeciwko Rutherford , w którym ustalono, że transport międzystanowy związku jest nielegalny, użycie drastycznie spadło. Amerykańska Agencja ds. Żywności i Leków nadal domaga się kar więzienia dla sprzedawców sprzedających letril do leczenia raka, nazywając go „wysoce toksycznym produktem, który nie wykazał żadnego wpływu na leczenie raka”.
W kulturze popularnej
Odcinek Law & Order Second Opinion opowiada o doradcy żywieniowym o imieniu „Doctor” Hass , który podaje pacjentom letril jako lek na raka piersi jako alternatywę dla mastektomii.
