Dur brzuszny
| Dur brzuszny | |
|---|---|
| Inne nazwy | Gorączka jelitowa, powolna gorączka |
 | |
| Czynnik sprawczy: odmiana serologiczna Salmonella enterica Typhi (pokazana pod mikroskopem z barwieniem wici) | |
| Specjalność |
Choroba zakaźna |
| Objawy | Gorączka, która zaczyna się od niskiej i wzrasta z każdym dniem, prawdopodobnie osiągając nawet 40,5 °C Ból głowy, osłabienie i zmęczenie, bóle mięśni, pocenie się, suchy kaszel, utrata apetytu, utrata masy ciała, ból brzucha, biegunka lub zaparcie, wysypka , obrzęk żołądka (powiększona wątroba lub śledziona) |
| Zwykły początek | 1-2 tygodnie po spożyciu |
| Czas trwania | Zwykle 7–10 dni po rozpoczęciu antybiotykoterapii. Dłużej, jeśli występują powikłania lub lekooporność. |
| Powoduje | Zakażenie przewodu pokarmowego Salmonella enterica serovar Typhi |
| Czynniki ryzyka | Mieszkać lub podróżować do obszarów, w których występuje dur brzuszny, Pracować jako mikrobiolog kliniczny zajmujący się bakteriami Salmonella typhi, Mieć bliski kontakt z osobą zarażoną lub niedawno zarażoną durem brzusznym, Pić wodę zanieczyszczoną ściekami, która zawiera Salmonella typhi |
| Zapobieganie | Można zapobiegać szczepionką. Osoby podróżujące do regionów o większej częstości występowania duru brzusznego są zwykle zachęcane do zaszczepienia się przed podróżą. |
| Leczenie | Antybiotyki, nawodnienie, w skrajnych przypadkach operacja. Kwarantanna, aby uniknąć narażenia innych (nie jest to powszechnie stosowane w dzisiejszych czasach). |
| Rokowanie | Prawdopodobny powrót do zdrowia bez komplikacji, jeśli odpowiednie antybiotyki zostaną podane i wcześnie zdiagnozowane. Jeśli infekujący szczep jest oporny na wiele leków lub w znacznym stopniu oporny na leki, rokowanie jest trudniejsze do określenia. Wśród nieleczonych ostrych przypadków 10% wydala bakterie przez trzy miesiące po początkowym wystąpieniu objawów, a 2–5% stanie się przewlekłymi nosicielami duru brzusznego. Niektórzy nosiciele są diagnozowani na podstawie pozytywnej próbki tkanki. Przewlekli nosiciele są z definicji bezobjawowi. |
Dur brzuszny , znany również jako dur brzuszny , jest chorobą wywoływaną przez bakterie Salmonella serotypu Typhi. Objawy wahają się od łagodnych do ciężkich i zwykle rozpoczynają się od sześciu do 30 dni po ekspozycji. przez kilka dni pojawia się stopniowa wysoka gorączka . Często towarzyszy temu osłabienie, ból brzucha , zaparcia , bóle głowy i łagodne wymioty. U niektórych osób pojawia się wysypka skórna z różowymi plamami . W ciężkich przypadkach ludzie mogą odczuwać dezorientację. Bez leczenia objawy mogą trwać tygodnie lub miesiące. Biegunka może być ciężka, ale występuje rzadko. Inni ludzie mogą przenosić bakterię bez wpływu na nią, ale nadal mogą rozprzestrzeniać chorobę. Dur brzuszny jest rodzajem jelitowej , wraz z durem rzekomym . Uważa się, że S. enterica Typhi infekuje i replikuje się tylko u ludzi.
Dur brzuszny jest wywoływany przez bakterię Salmonella enterica subsp. enterica serotyp Typhi rosnący w jelitach , kępkach Peyersa , krezkowych węzłach chłonnych , śledzionie , wątrobie , pęcherzyku żółciowym , szpiku kostnym i krwi . Tyfus rozprzestrzenia się poprzez jedzenie lub picie pokarmu lub wody zanieczyszczonej kałem zakażonej osoby. Czynniki ryzyka obejmują ograniczony dostęp do czystej wody pitnej i złe warunki sanitarne . Ci, którzy nie byli jeszcze narażeni na kontakt z patogenem i spożywają skażoną wodę pitną lub żywność, są najbardziej narażeni na wystąpienie objawów. Tylko ludzie mogą zostać zarażeni; nie są znane rezerwuary zwierząt.
Diagnoza polega na wyhodowaniu i identyfikacji S. enterica Typhi z próbek pobranych od pacjentów lub wykryciu odpowiedzi immunologicznej na patogen z próbek krwi . Niedawno nowe postępy w gromadzeniu i analizie danych na dużą skalę pozwoliły naukowcom opracować lepszą diagnostykę, taką jak wykrywanie zmieniających się ilości małych cząsteczek we krwi, które mogą konkretnie wskazywać na dur brzuszny. Narzędzia diagnostyczne w regionach, w których dur brzuszny jest najbardziej rozpowszechniony, mają dość ograniczoną dokładność i specyficzność, a czas potrzebny do postawienia właściwej diagnozy, rosnące rozprzestrzenianie się oporności na antybiotyki i koszty testów są również trudnościami dla niedofinansowanych systemów opieki zdrowotnej.
Szczepionka przeciw durowi brzusznemu może zapobiec około 40% do 90% przypadków w ciągu pierwszych dwóch lat. Szczepionka może działać przez okres do siedmiu lat. Dla osób z grupy wysokiego ryzyka lub osób podróżujących do obszarów, gdzie choroba jest powszechna, zaleca się szczepienie. Inne wysiłki mające na celu zapobieganie tej chorobie obejmują zapewnienie czystej wody pitnej , dobrych warunków sanitarnych i mycia rąk . Do czasu potwierdzenia zakażenia osoba zarażona nie powinna przygotowywać posiłków dla innych. Dur brzuszny leczy się antybiotykami, takimi jak azytromycyna , fluorochinolony lub cefalosporyny trzeciej generacji . Rozwija się oporność na te antybiotyki, co utrudnia leczenie.
W 2015 roku zgłoszono 12,5 miliona nowych przypadków duru brzusznego. Choroba występuje najczęściej w Indiach. Dzieci są najczęściej dotknięte. Tyfus zmniejszył się w krajach rozwiniętych w latach czterdziestych XX wieku w wyniku poprawy warunków sanitarnych i stosowania antybiotyków. Każdego roku w Stanach Zjednoczonych odnotowuje się około 400 przypadków, a około 6000 osób choruje na tyfus. W 2015 r. spowodowało to około 149 000 zgonów na całym świecie – w porównaniu ze 181 000 w 1990 r. Bez leczenia ryzyko zgonu może sięgać nawet 20%. Po leczeniu wynosi od 1% do 4%.
Tyfus to inna choroba. Ze względu na podobne objawy nie zostały one uznane za odrębne choroby aż do XIX wieku. „Tyfus” oznacza „przypominający tyfus”.
Symptomy i objawy
Klasycznie postęp nieleczonego duru brzusznego ma trzy odrębne etapy, z których każdy trwa około tygodnia. W trakcie tych etapów pacjent staje się wyczerpany i wychudzony.
- W pierwszym tygodniu temperatura ciała powoli wzrasta i obserwuje się wahania gorączki ze względną bradykardią ( objaw Fageta ), złym samopoczuciem , bólem głowy i kaszlem. W jednej czwartej przypadków obserwuje się krwawienie z nosa ( krwawienie z nosa), możliwy jest również ból brzucha. Zmniejszenie liczby krążących krwinek białych ( leukopenia ) występuje z eozynopenią i względną limfocytozą ; posiewy krwi są pozytywne dla S. enterica subsp. enterica odmiana serologiczna Typhi. Test Widala jest zazwyczaj ujemna.
- W drugim tygodniu osoba jest często zbyt zmęczona, aby wstać, z wysoką gorączką na poziomie około 40 ° C (104 ° F) i bradykardią (dysocjacja sfigmotermiczna lub objaw Fageta), klasycznie z dykrotyczną falą tętna . Może wystąpić delirium , gdy pacjent jest często spokojny, ale czasami staje się pobudzony. To delirium nadało durowi brzusznemu przydomek „nerwowa gorączka”. Plamy róży pojawiają się na dolnej części klatki piersiowej i brzuchu u około jednej trzeciej pacjentów. Rhonchi (odgłosy grzechotania oddechu) są słyszalne u podstawy płuc. Brzuch jest rozdęty i bolesny w prawym dolnym kwadrancie, gdzie słychać dudnienie. Na tym etapie może wystąpić biegunka, ale często występują również zaparcia. Śledziona i wątroba są powiększone ( hepatosplenomegalia ) i tkliwość, a aktywność aminotransferaz wątrobowych jest podwyższona. Test Widala jest silnie dodatni, z obecnością przeciwciał antyO i antyH. Posiewy krwi są czasami nadal pozytywne.
- W trzecim tygodniu duru brzusznego może wystąpić szereg powikłań:
- Gorączka jest nadal bardzo wysoka i waha się bardzo niewiele w ciągu 24 godzin. Następuje odwodnienie wraz z niedożywieniem, a pacjent ma majaczenie. U jednej trzeciej osób dotkniętych chorobą rozwija się wysypka plamkowa na tułowiu.
- Występuje krwotok jelitowy z powodu krwawienia w zatkanych kępkach Peyera ; może to być bardzo poważne, ale zwykle nie jest śmiertelne.
- Perforacja jelita w dystalnej części jelita krętego jest bardzo poważnym powikłaniem, często śmiertelnym. Może przebiegać bez niepokojących objawów do czasu wystąpienia posocznicy lub rozlanego zapalenia otrzewnej .
- Choroby układu oddechowego, takie jak zapalenie płuc i ostre zapalenie oskrzeli
- Zapalenie mózgu
- Objawy neuropsychiatryczne (opisywane jako „mamrotanie delirium” lub „czuwanie w śpiączce”), z skubaniem pościeli lub wyimaginowanych przedmiotów.
- Ropnie z przerzutami, zapalenie pęcherzyka żółciowego , zapalenie wsierdzia i zapalenie kości .
- Czasami obserwuje się małą liczbę płytek krwi ( małopłytkowość ).
Powoduje

Bakteria
Gram -ujemna bakteria wywołująca dur brzuszny to Salmonella enterica subsp. enterica odmiana serologiczna Typhi. W oparciu o schemat podtypów MLST, dwa główne typy sekwencji S. Typhi to ST1 i ST2, które są szeroko rozpowszechnione na całym świecie. Globalna analiza filogeograficzna wykazała dominację haplotypu 58 (H58), który prawdopodobnie powstał w Indiach pod koniec lat 80. XX wieku i obecnie rozprzestrzenia się na całym świecie z wielolekoopornością. Bardziej szczegółowy schemat genotypowania został zgłoszony w 2016 roku i jest obecnie szeroko stosowany. Ten schemat przeklasyfikował nomenklaturę H58 do genotypu 4.3.1.
Przenoszenie
W przeciwieństwie do innych szczepów Salmonelli , nie są znane żadne zwierzęta będące nosicielami duru brzusznego. Jedynymi znanymi nosicielami bakterii są ludzie. S. enterica subsp. enterica serovar Typhi jest przenoszona drogą fekalno-oralną od osób zakażonych oraz od bezobjawowych nosicieli bakterii. Bezobjawowym nosicielem jest osoba, która rok po ostrym stadium infekcji nadal wydala bakterie duru brzusznego z kałem.
Diagnoza
Diagnozę stawia się na podstawie dowolnego posiewu krwi , szpiku kostnego lub kału oraz testu Widala (wykazanie obecności przeciwciał przeciwko antygenom Salmonella O-somatyczny i H-flagellar). W krajach epidemicznych i mniej zamożnych, po wykluczeniu malarii , czerwonki lub zapalenia płuc , zazwyczaj podejmuje się próbę terapeutyczną z chloramfenikolem w oczekiwaniu na wyniki testu Widala oraz posiewów krwi i kału.
Test Widala
Test Widala służy do identyfikacji specyficznych przeciwciał w surowicy osób chorych na dur brzuszny za pomocą interakcji antygen-przeciwciało. [ potrzebne źródło ]
W tym teście surowica jest mieszana z martwą zawiesiną bakteryjną salmonelli ze specyficznymi antygenami. Jeśli surowica pacjenta zawiera przeciwciała przeciwko tym antygenom, przyczepiają się one do nich, tworząc grudki. Jeśli zbrylanie nie występuje, test jest negatywny. Test Widala jest czasochłonny i podatny na znaczące fałszywe alarmy. Może być również fałszywie ujemny u osób niedawno zakażonych. Ale w przeciwieństwie do testu Typhidot, test Widala określa ilościowo próbkę za pomocą mian .
Szybkie testy diagnostyczne
Szybkie testy diagnostyczne, takie jak Tubex, Typhidot i Test-It, wykazały umiarkowaną dokładność diagnostyczną.
tyfidot
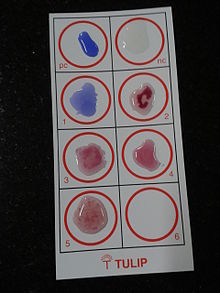
Typhidot opiera się na obecności swoistych przeciwciał IgM i IgG przeciwko specyficznemu antygenowi 50 Kd OMP. Test ten przeprowadza się na membranie z azotanu celulozy, do której przyczepione jest określone S. typhi jako utrwalone linie testowe. Oddzielnie identyfikuje przeciwciała IgM i IgG. IgM wskazuje na niedawną infekcję; IgG oznacza zdalną infekcję.
Podkładka do próbek tego zestawu zawiera koloidalne złoto-anty-ludzka IgG lub złoto-anty-ludzka IgM. Jeśli próbka zawiera przeciwciała IgG i IgM przeciwko tym antygenom, zareagują one i zmienią kolor na czerwony. Test dur brzuszny staje się dodatni w ciągu 2-3 dni od zakażenia.
Dwa kolorowe paski wskazują na pozytywny wynik testu. Pojedynczy prążek kontrolny wskazuje na wynik negatywny. Pojedyncza pierwsza stała linia lub całkowity brak prążka wskazuje na nieważny test. Największym ograniczeniem Typhidota jest to, że nie jest ilościowy, tylko pozytywny lub negatywny.
Próba tubeksowa
Test Tubex zawiera dwa rodzaje cząstek: brązowe cząstki magnetyczne pokryte antygenem i niebieskie cząsteczki wskaźnikowe pokryte przeciwciałem O9. Podczas testu, jeśli w surowicy obecne są przeciwciała, przyłączą się one do brązowych cząstek magnetycznych i opadną na podstawę, podczas gdy niebieskie cząsteczki wskaźnika pozostaną w roztworze, dając niebieski kolor, co oznacza, że wynik testu jest pozytywny. [ potrzebne źródło ]
Jeśli w surowicy nie ma przeciwciał, niebieskie cząsteczki przyczepiają się do brązowych cząstek i osadzają się na dnie, tworząc bezbarwny roztwór, co oznacza, że wynik testu jest ujemny.
Zapobieganie

Warunki sanitarne i higiena są ważne, aby zapobiegać durowi brzusznemu. Może rozprzestrzeniać się tylko w środowiskach, w których odchody ludzkie mogą mieć kontakt z żywnością lub wodą pitną. Ostrożne przygotowywanie posiłków i mycie rąk są kluczowe dla zapobiegania durowi brzusznemu. Uprzemysłowienie w znacznym stopniu przyczyniło się do wyeliminowania duru brzusznego, ponieważ wyeliminowało zagrożenia dla zdrowia publicznego związane z umieszczaniem na ulicach publicznych odchodów końskich, które doprowadziły do powstania dużej liczby much, które są wektorami wielu patogenów, w tym Salmonella spp . Według statystyk amerykańskiego Centrum Kontroli i Prewencji Chorób , ok chlorowanie wody pitnej doprowadziło do dramatycznego spadku przenoszenia duru brzusznego.
Szczepionka
Dwie szczepionki przeciw durowi brzusznemu są zarejestrowane do stosowania w zapobieganiu durowi brzusznemu: żywa, doustna szczepionka Ty21a (sprzedawana jako Vivotif przez Crucell Switzerland AG) oraz polisacharydowa szczepionka przeciw durowi brzusznemu do wstrzykiwania (sprzedawana jako Typhim Vi przez Sanofi Pasteur i Typpherix przez GlaxoSmithKline ). Oba są skuteczne i zalecane dla osób podróżujących do obszarów, w których dur brzuszny jest endemiczny. Dawki przypominające są zalecane co pięć lat w przypadku szczepionki doustnej i co dwa lata w przypadku szczepionki do wstrzykiwań. Starsza, zabita szczepionka pełnokomórkowa jest nadal stosowana w krajach, w których nowsze preparaty nie są dostępne, ale ta szczepionka nie jest już zalecana do stosowania, ponieważ ma więcej skutków ubocznych (głównie ból i stan zapalny w miejscu wstrzyknięcia).
Aby pomóc zmniejszyć wskaźniki zachorowalności na dur brzuszny w krajach rozwijających się , Światowa Organizacja Zdrowia (WHO) zatwierdziła program szczepień rozpoczynający się w 1999 r. Szczepienia okazały się skuteczne w kontrolowaniu epidemii na obszarach o wysokiej zachorowalności, a także są bardzo opłacalne: ceny są zwykle niższe niż 1 USD za dawkę. Ponieważ cena jest niska, społeczności dotknięte ubóstwem chętniej korzystają ze szczepień. Chociaż programy szczepień przeciwko durowi brzusznemu okazały się skuteczne, same nie mogą wyeliminować duru brzusznego. Łączenie szczepionek z działaniami na rzecz zdrowia publicznego jest jedynym sprawdzonym sposobem kontrolowania tej choroby.
Od lat 90. WHO zaleca dwie szczepionki przeciw durowi brzusznemu. Szczepionkę ViPS podaje się we wstrzyknięciu, a Ty21a w kapsułkach. Zaleca się szczepienie szczepionką ViPS tylko dla osób powyżej drugiego roku życia i wymaga ponownego szczepienia po 2–3 latach ze skutecznością 55–72%. Szczepionka Ty21a jest zalecana dla osób w wieku pięciu lat i starszych, trwająca 5–7 lat ze skutecznością 51–67%. Obie szczepionki okazały się bezpieczne i skuteczne w zwalczaniu epidemii w wielu regionach.
Dostępna jest również wersja szczepionki skojarzonej ze szczepionką przeciwko wirusowemu zapaleniu wątroby typu A.
Wyniki badania fazy 3 skoniugowanej szczepionki przeciw durowi brzusznemu (TCV) w grudniu 2019 r. wykazały o 81% mniej przypadków wśród dzieci.
Leczenie
Doustna terapia nawadniająca
Ponowne odkrycie doustnej terapii nawadniającej w latach 60. XX wieku zapewniło prosty sposób zapobiegania wielu zgonom z powodu chorób biegunkowych w ogóle.
Antybiotyki
Jeśli oporność jest rzadka, leczeniem z wyboru jest fluorochinolon, taki jak cyprofloksacyna . W przeciwnym razie pierwszym wyborem jest cefalosporyna trzeciej generacji, taka jak ceftriakson lub cefotaksym . Cefiksym jest odpowiednią alternatywą doustną.
Prawidłowo leczona dur brzuszny w większości przypadków nie jest śmiertelna. Antybiotyki, takie jak ampicylina , chloramfenikol, trimetoprim-sulfametoksazol , amoksycylina i ciprofloksacyna były powszechnie stosowane w leczeniu. Leczenie antybiotykami zmniejsza śmiertelność przypadków do około 1%.
Bez leczenia u niektórych pacjentów rozwija się utrzymująca się gorączka, bradykardia, hepatosplenomegalia, objawy brzuszne i czasami zapalenie płuc. U pacjentów o białej skórze różowe plamy, które bledną pod naciskiem, pojawiają się na skórze tułowia nawet w 20% przypadków. W trzecim tygodniu u nieleczonych przypadków mogą wystąpić powikłania żołądkowo-jelitowe i mózgowe, które w 10–20% przypadków mogą zakończyć się zgonem. Najwyższe wskaźniki śmiertelności odnotowano u dzieci poniżej 4 roku życia. Około 2–5% osób, które zachorowały na dur brzuszny, staje się przewlekłymi nosicielami, ponieważ bakterie utrzymują się w drogach żółciowych po ustąpieniu objawów.
Chirurgia
Operacja jest zwykle wskazana, jeśli wystąpi perforacja jelit . Jedno z badań wykazało 30-dniową śmiertelność na poziomie 9% (8/88), a zakażenia miejsca operowanego na poziomie 67% (59/88), przy czym obciążenie chorobami ponoszą głównie kraje o niskich zasobach.
W leczeniu chirurgicznym większość chirurgów preferuje proste zamknięcie perforacji z drenażem otrzewnej . Resekcja jelita cienkiego jest wskazana u pacjentów z wieloma perforacjami. Jeśli leczenie antybiotykami nie eliminuje wątrobowo-żółciowego , należy usunąć pęcherzyk żółciowy . Cholecystektomia jest czasami skuteczna, zwłaszcza u pacjentów z kamicą żółciową , ale nie zawsze jest skuteczna w eliminacji stanu nosicielstwa z powodu utrzymującego się zakażenia wątroby .
Opór
Ponieważ oporność na ampicylinę, chloramfenikol, trimetoprim-sulfametoksazol i streptomycynę jest obecnie powszechna, środki te nie są już stosowane jako leczenie pierwszego rzutu duru brzusznego. Tyfus oporny na te czynniki jest znany jako dur wielolekooporny.
Oporność na cyprofloksacynę jest coraz większym problemem, zwłaszcza na subkontynencie indyjskim i w Azji Południowo-Wschodniej . Wiele ośrodków przechodzi z ciprofloksacyny na ceftriakson jako pierwszą linię leczenia podejrzenia duru brzusznego pochodzącego z Ameryki Południowej, Indii, Pakistanu, Bangladeszu, Tajlandii lub Wietnamu. Sugerowano również, że azytromycyna jest lepsza w leczeniu opornego duru brzusznego niż leki fluorochinolonowe i ceftriakson. Azytromycynę można przyjmować doustnie i jest tańsza niż ceftriakson podawany we wstrzyknięciu.
Odrębny problem dotyczy badań laboratoryjnych pod kątem zmniejszonej wrażliwości na ciprofloksacynę; obecne zalecenia są takie, że izolaty powinny być badane jednocześnie pod kątem ciprofloksacyny (CIP) i kwasu nalidyksowego (NAL), że izolaty wrażliwe zarówno na CIP, jak i NAL powinny być zgłaszane jako „wrażliwe na cyprofloksacynę” oraz że izolaty wrażliwe na CIP, ale nie na NAL należy zgłaszać jako „zmniejszoną wrażliwość na cyprofloksacynę”. Jednak analiza 271 izolatów wykazała, że około 18% izolatów o zmniejszonej wrażliwości na fluorochinolony , klasę, do której należy CIP ( MIC 0,125–1,0 mg/L), nie zostałyby wykryte tą metodą.
Epidemiologia
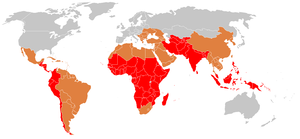
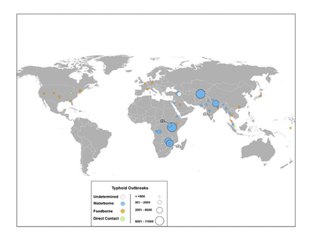
W 2000 roku dur brzuszny spowodował około 21,7 miliona zachorowań i 217 000 zgonów. Występuje najczęściej u dzieci i młodych dorosłych w wieku od 5 do 19 lat. W 2013 roku spowodowało to około 161 000 zgonów - w porównaniu z 181 000 w 1990 roku. Niemowlęta, dzieci i młodzież w południowo-środkowej i południowo-wschodniej Azji mają najwyższe wskaźniki duru brzusznego. Ogniska są również często zgłaszane w Afryce Subsaharyjskiej i Azji Południowo-Wschodniej. W 2000 roku ponad 90% zachorowań i zgonów z powodu duru brzusznego miało miejsce w Azji. W Stanach Zjednoczonych każdego roku występuje około 400 przypadków, z których 75% nabywa się podczas podróży międzynarodowych.
Przed erą antybiotyków śmiertelność z powodu duru brzusznego wynosiła 10–20%. Dziś, przy szybkim leczeniu, jest to mniej niż 1%, ale u 3–5% zakażonych osób rozwija się przewlekła infekcja pęcherzyka żółciowego. Ponieważ S. enterica subsp. enterica serovar Typhi jest ograniczony do ludzi, ci przewlekli nosiciele stają się kluczowym rezerwuarem, który może utrzymywać się przez dziesięciolecia w celu dalszego rozprzestrzeniania się choroby, dodatkowo komplikując jej identyfikację i leczenie. Ostatnio badanie S. enterica subsp. enterica serowar Typhi związany z dużą epidemią i nosicielem na poziomie genomu dostarcza nowych informacji na temat patogenezy patogenu.
W krajach uprzemysłowionych poprawa warunków sanitarnych i obchodzenia się z żywnością zmniejszyła liczbę przypadków duru brzusznego. Kraje rozwijające się mają najwyższe wskaźniki. Obszary te nie mają dostępu do czystej wody, odpowiednich systemów sanitarnych i odpowiednich placówek opieki zdrowotnej. Na tych obszarach taki dostęp do podstawowych potrzeb w zakresie zdrowia publicznego nie jest spodziewany w najbliższej przyszłości.
W latach 2004–2005 wybuch epidemii w Demokratycznej Republice Konga spowodował ponad 42 000 przypadków i 214 zgonów. Od listopada 2016 r. w Pakistanie wybuchła epidemia duru brzusznego o dużej odporności na leki (XDR).
W Europie raport oparty na danych za 2017 r. uzyskanych z Europejskiego Systemu Nadzoru (TESSy) dotyczących rozmieszczenia potwierdzonych przypadków duru brzusznego i duru rzekomego wykazał, że 22 kraje UE/EOG zgłosiły łącznie 1098 przypadków, z czego 90,9% stanowiły podróże spokrewnione, nabyte głównie podczas podróży do Azji Południowej .
Historia
Wczesne opisy
Zaraza ateńska podczas wojny peloponeskiej była najprawdopodobniej wybuchem duru brzusznego. Podczas wojny Ateńczycy wycofali się do otoczonego murami miasta, aby uniknąć ataku Spartan . Ten masowy napływ ludzi do skoncentrowanej przestrzeni przeciążył infrastrukturę wodociągową i kanalizacyjną, prawdopodobnie prowadząc do niehigienicznych warunków, ponieważ słodka woda stała się trudniejsza do zdobycia, a odpady stały się trudniejsze do zbierania i usuwania poza mury miasta. W 2006 roku badanie szczątków miejsca masowego pochówku z Aten z okresu zarazy (ok. 430 pne) wykazało, że wykryto fragmenty DNA podobne do współczesnego DNA S. Typhi, podczas gdy Yersinia pestis ( dżuma), Rickettsia prowazekii (tyfus), Mycobacterium tuberculosis , wirusa ospy krowiej i Bartonella henselae nie wykryto w żadnej z badanych szczątków.
Możliwe, że cesarz rzymski August Cezar miał ropień wątroby lub dur brzuszny i przeżył, stosując kąpiele lodowe i zimne okłady jako środek leczenia gorączki. Znajduje się tam pomnik greckiego lekarza Antoniusza Musy , który leczył gorączkę.
Definicja i dowód transmisji
Francuskim lekarzom Pierre-Fidele Bretonneau i Pierre-Charles-Alexandre Louis przypisuje się opisanie duru brzusznego jako specyficznej choroby, unikalnej dla tyfusu . Obaj lekarze przeprowadzili sekcje zwłok osób, które zmarły w Paryżu z powodu gorączki – i wskazali, że wielu miało zmiany w kępkach Peyera co korelowało z wyraźnymi objawami przed śmiercią. Brytyjscy medycy byli sceptyczni co do rozróżnienia między tyfusem a tyfusem, ponieważ oba były wówczas endemiczne w Wielkiej Brytanii. Jednak we Francji krążył w populacji tylko tyfus. Pierre-Charlles-Alexandre Louis przeprowadził również studia przypadków i analizy statystyczne, aby wykazać, że tyfus jest zaraźliwy - i że osoby, które już chorowały, wydawały się być chronione. Później kilku amerykańskich lekarzy potwierdziło te odkrycia, a następnie Sir William Jenner przekonał pozostałych sceptyków, że dur brzuszny jest specyficzną chorobą, którą można rozpoznać po zmianach w kępkach Peyera, badając sześćdziesiąt sześć sekcji zwłok pacjentów z gorączką i dochodząc do wniosku, że objawy bólów głowy, biegunki, wysypki i bólu brzucha występowały tylko u pacjentów, którzy wówczas mieli jelita uszkodzenia po śmierci; co utrwaliło związek choroby z przewodem pokarmowym i dało pierwszą wskazówkę co do drogi przenoszenia.
W 1847 roku William Budd dowiedział się o epidemii duru brzusznego w Clifton i stwierdził, że wszyscy 13 z 34 mieszkańców, którzy zachorowali na tę chorobę, czerpali wodę pitną z tej samej studni. Warto zauważyć, że ta obserwacja miała miejsce dwa lata przed odkryciem przez Johna Snow drogi zanieczyszczonej wody jako przyczyny wybuchu cholery . Budd został później urzędnikiem ds. Zdrowia w Bristolu i zapewnił zaopatrzenie w czystą wodę oraz udokumentował dalsze dowody duru brzusznego jako choroby przenoszonej przez wodę przez całą swoją karierę.
Przyczyna
Polski naukowiec Tadeusz Browicz opisał krótką pałeczkę w narządach i kale ofiar duru brzusznego w 1874 r. Browicz był w stanie wyizolować i wyhodować prątki, ale nie posunął się tak daleko, by insynuować lub udowodnić, że spowodowały chorobę.
W kwietniu 1880 roku, trzy miesiące przed publikacją Ebertha, Edwin Klebs opisał krótkie i nitkowate prątki w kępkach Peyera u ofiar duru brzusznego. Spekulowano o roli bakterii w chorobie, ale nie została ona potwierdzona.
W 1880 roku Karl Joseph Eberth opisał Bacillus, który, jak podejrzewał, był przyczyną duru brzusznego. Eberthowi przypisuje się definitywne odkrycie bakterii poprzez pomyślne wyizolowanie tej samej bakterii od 18 z 40 ofiar duru brzusznego i nieodkrycie bakterii obecnej u jakichkolwiek „kontrolnych” ofiar innych chorób. W 1884 roku patolog Georg Theodor August Gaffky (1850–1918) potwierdził odkrycia Ebertha. Gaffky wyizolował tę samą bakterię co Eberth ze śledziony ofiary duru brzusznego i był w stanie wyhodować bakterię na podłożu stałym. Organizmowi nadano takie nazwy, jak Bacillus Ebertha, Eberthella Typhi i Gaffky-Eberth Bacillus. Obecnie bakteria wywołująca dur brzuszny nosi naukową nazwę Salmonella enterica serovar Typhi.
Chlorowanie wody
Większość krajów rozwiniętych odnotowała spadek zachorowań na dur brzuszny w pierwszej połowie XX wieku z powodu szczepień i postępów w zakresie warunków sanitarnych i higieny publicznej. W 1893 roku podjęto próby chlorowania wody w Hamburgu w Niemczech, aw 1897 roku Maidstone w Anglii było pierwszym miastem, w którym chlorowano całą wodę. W 1905 roku, po wybuchu duru brzusznego, miasto Lincoln w Anglii wprowadziło stałe chlorowanie wody. Pierwsza stała dezynfekcja wody pitnej w USA została przeprowadzona w 1908 roku w Jersey City w stanie New Jersey , zaopatrzenie w wodę. Uznanie za decyzję o budowie instalacji chlorowania przypisuje się Johnowi L. Lealowi . Obiekt chlorowania został zaprojektowany przez George'a W. Fullera .
Wybuchy w podróżujących grupach wojskowych doprowadziły do powstania torby Lyster w 1915 roku; worek z kranem, który można zawiesić na drzewie lub słupie, napełniony wodą i wyposażony w tabletkę chlorującą do wrzucenia do wody. Torba Lyster była niezbędna dla przetrwania amerykańskich żołnierzy podczas wojny w Wietnamie .
Transmisja bezpośrednia i nośniki
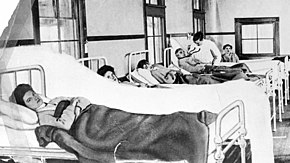
Było kilka przypadków, w których dostawcy mleka rozprzestrzeniali tyfus w społecznościach, którym służyli. Chociaż tyfus nie rozprzestrzenia się przez samo mleko, było kilka przykładów dystrybutorów mleka w wielu lokalizacjach, którzy podlewali swoje mleko zanieczyszczoną wodą lub myli szklane butelki, w których umieszczono mleko zanieczyszczoną wodą. Boston miał dwa takie przypadki na przełomie XIX i XX wieku. W 1899 r. odnotowano 24 przypadki duru brzusznego u jednego mleczarza, którego żona zmarła na tyfus tydzień przed wybuchem epidemii. W 1908 roku JJ Fallon, który był również mleczarzem, zmarł na tyfus. Po jego śmierci i potwierdzeniu diagnozy duru brzusznego miasto przeprowadziło dochodzenie w sprawie objawów i przypadków duru brzusznego na jego trasie i znalazło dowody na znaczną epidemię. Miesiąc po pierwszym zgłoszeniu epidemii, Boston Globe opublikował krótkie oświadczenie, w którym ogłosił koniec epidemii, stwierdzając, że „[a] na Jamaica Plain nastąpił niewielki wzrost, łącznie 272 przypadki. W całym mieście jest łącznie 348 przypadków”. Podczas tej epidemii zgłoszono co najmniej jedną śmierć: pani Sophia S. Engstrom, lat 46. Tyfus nadal pustoszył dzielnicę Jamaica Plain , w szczególności przez cały 1908 r., A kilka innych osób zmarło z powodu duru brzusznego, chociaż te przypadki były nie są bezpośrednio związane z epidemią. W tamtym czasie dzielnica Jamaica Plain była domem dla wielu imigrantów z klasy robotniczej i biednych, głównie z Irlandia .
Najbardziej znaną nosicielką duru brzusznego, ale bynajmniej nie najbardziej niszczycielską, była Mary Mallon , znana jako Tyfus Maria. Chociaż w tamtym czasie znane były inne przypadki przenoszenia duru brzusznego z człowieka na człowieka, koncepcja bezobjawowego nosiciela, który był w stanie przenosić chorobę, była jedynie hipotezą i nie została jeszcze zidentyfikowana ani udowodniona. Mary Mallon stała się pierwszym znanym przykładem bezobjawowego nosiciela choroby zakaźnej, czyniąc dur brzuszny pierwszą znaną chorobą przenoszoną przez bezobjawowych gospodarzy. Przypadki i zgony spowodowane przez Mallona dotyczyły głównie rodzin z wyższych sfer w Nowym Jorku. W czasie, gdy Mallon był osobistym kucharzem dla rodzin z wyższych sfer, Nowy Jork zgłaszał rocznie od 3000 do 4500 przypadków duru brzusznego. Latem 1906 r. na dur brzuszny zachorowały dwie córki zamożnej rodziny i pracujące w ich domu służące. Po zbadaniu źródeł wody w domu i wykluczeniu zanieczyszczenia wody, rodzina zatrudniła inżyniera budownictwa Jerzego Sopera przeprowadzić dochodzenie w sprawie możliwego źródła duru brzusznego w domu. Soper opisał siebie jako „wojownika epidemii”. Jego dochodzenie wykluczyło wiele źródeł pożywienia i doprowadziło go do pytania, czy kucharz zatrudniony przez rodzinę tuż przed wybuchem epidemii w ich gospodarstwie domowym, Mallon, był źródłem. Ponieważ już wyjechała i podjęła pracę gdzie indziej, zaczął ją śledzić w celu uzyskania próbki kału. Kiedy w końcu mógł osobiście spotkać Mallon, opisał ją, mówiąc: „Mary miała dobrą figurę i można by ją nazwać wysportowaną, gdyby nie była trochę za ciężka”. W opowiadaniach o pościgu Sopera za Mallonem, wydaje się, że jego jedynym wyrzutem sumienia jest to, że nie przypisano mu wystarczającego uznania za jego nieustanne poszukiwanie i publikację jej danych osobowych, stwierdzając, że media „okradają mnie z jakiejkolwiek zasługi odkrycia pierwszego nosiciela duru brzusznego znalezionego w Ameryce”. Ostatecznie podejrzewano, że Mallon spowodował 51 przypadków i 3 zgony.
W 1924 roku miasto Portland w stanie Oregon doświadczyło wybuchu duru brzusznego, na który złożyło się 26 przypadków i 5 zgonów, wszystkie zgony z powodu krwotoku jelitowego . Stwierdzono, że wszystkie przypadki były spowodowane przez jednego pracownika gospodarstwa mlecznego, który wydalał duże ilości patogenu duru brzusznego w swoim moczu. Błędne rozpoznanie choroby, spowodowane niedokładnymi wynikami testu Widala, opóźnioną identyfikacją nosiciela i właściwym leczeniem. Ostatecznie potrzeba było czterech próbek różnych wydzielin od wszystkich pracowników mleczarni, aby skutecznie zidentyfikować nosiciela. Po odkryciu, pracownik mleczarni został przymusowo poddany kwarantannie przez siedem tygodni i pobierano regularne próbki, przez większość czasu próbki kału nie dające duru brzusznego i często mocz dający patogen. Zgłoszono, że nosiciel ma 72 lata i wydaje się być w doskonałym zdrowiu bez żadnych objawów. Leczenie farmaceutyczne zmniejszyło ilość wydzielanych bakterii, jednak infekcja nigdy nie została całkowicie usunięta z moczu, a nosiciel został uwolniony „z rozkazem, aby nigdy więcej nie zajmować się żywnością przeznaczoną do spożycia przez ludzi”. W momencie zwolnienia autorzy zauważyli, że „od ponad pięćdziesięciu lat utrzymuje się głównie z dojenia krów i niewiele wie o innych formach pracy, należy się spodziewać, że konieczna będzie ścisła obserwacja, aby upewnić się, że nie nie angażować się ponownie w ten zawód”.
Ogólnie rzecz biorąc, na początku XX wieku medycyna zaczęła identyfikować nosicieli choroby i dowody na jej przenoszenie niezależnie od zanieczyszczenia wody. W Amerykańskim Stowarzyszeniu Medycznym z 1933 r publikacji, leczenie bezobjawowych nosicieli najlepiej podsumowuje zdanie otwierające „Nosiciele prątków duru brzusznego są zagrożeniem”. W tej samej publikacji podano pierwsze oficjalne szacunki dotyczące nosicieli duru brzusznego: od 2 do 5% wszystkich chorych na dur brzuszny, z podziałem na nosicieli tymczasowych i przewlekłych. Autorzy szacują ponadto, że na każdego nosiciela płci męskiej przypada od czterech do pięciu przewlekłych nosicielek płci żeńskiej, chociaż nie przedstawili żadnych danych wyjaśniających to twierdzenie o różnicy między płciami w odsetku nosicieli duru brzusznego. Jeśli chodzi o leczenie, autorzy sugerują: „Po rozpoznaniu nosiciele muszą zostać poinstruowani, jak usuwać odchody, a także jak ważna jest higiena osobista. Należy im zabronić dotykania żywności lub napojów przeznaczonych dla innych osób oraz ich przemieszczania się i miejsce pobytu należy zgłosić inspektorom sanitarnym”.
Obecnie nosiciele duru brzusznego występują na całym świecie, ale największa liczba bezobjawowych zakażeń występuje prawdopodobnie w krajach Azji Południowej i Południowo-Wschodniej oraz w krajach Subsaharyjskich. Departament zdrowia publicznego hrabstwa Los Angeles śledzi nosicieli duru brzusznego i co roku zgłasza liczbę nosicieli zidentyfikowanych w hrabstwie; w latach 2006-2016 wykrywano 0-4 nowych przypadków nosicieli duru brzusznego rocznie. Należy zgłaszać przypadki duru brzusznego w ciągu jednego dnia roboczego od identyfikacji. Od 2018 r. Nosiciele chronicznego duru brzusznego muszą podpisać „Umowę przewoźnika” i są zobowiązani do przeprowadzania testów na obecność duru brzusznego dwa razy w roku, najlepiej co 6 miesięcy. Przewoźnicy mogą zostać zwolnieni z umów po spełnieniu warunków „zwolnienia”, na podstawie realizacji spersonalizowanego planu leczenia opracowanego z personelem medycznym. Wymagania dotyczące uwolnienia nosiciela kału lub pęcherzyka żółciowego: 6 kolejnych negatywnych próbek kału i moczu dostarczonych w odstępach 1 miesiąca lub dłuższych, rozpoczynających się co najmniej 7 dni po zakończeniu terapii. Wymagania dotyczące zwolnienia nosiciela moczu lub nerki: 6 kolejnych negatywnych próbek moczu dostarczonych w odstępach 1 miesiąca lub dłuższych, rozpoczynających się co najmniej 7 dni po zakończeniu terapii. Od 2016 roku stosunek liczby kobiet do mężczyzn wśród nosicieli w hrabstwie Los Angeles wynosił 3: 1.
Ze względu na charakter przypadków bezobjawowych pozostaje wiele pytań dotyczących tego, jak ludzie są w stanie tolerować infekcję przez długi czas, jak identyfikować takie przypadki i jakie są skuteczne opcje leczenia. Naukowcy pracują obecnie nad zrozumieniem bezobjawowego zakażenia Salmonelli , badając infekcje u zwierząt laboratoryjnych, co ostatecznie doprowadzi do ulepszonych opcji zapobiegania i leczenia nosicieli duru brzusznego. W 2002 roku dr John Gunn opisał zdolność Salmonella sp. do tworzenia biofilmów na kamieniach żółciowych u myszy, dostarczając modelu do badania przewozu w pęcherzyku żółciowym. Dr Denise Monack i dr Stanley Falkow opisali mysi model bezobjawowej infekcji jelitowej i ogólnoustrojowej w 2004 r., a następnie dr Monack wykazał, że subpopulacja superrozsiewaczy jest odpowiedzialna za większość transmisji do nowych gospodarzy, po 80/20 zasady przenoszenia chorób i że mikroflora jelitowa prawdopodobnie odgrywa rolę w przenoszeniu. Mysi model dr Monacka umożliwia długotrwałe nosicielstwo salmonelli w krezkowych węzłach chłonnych , śledzionie i wątroba .
Rozwój szczepionki

Brytyjski bakteriolog Almroth Edward Wright jako pierwszy opracował skuteczną szczepionkę przeciw durowi brzusznemu w Army Medical School w Netley , Hampshire . Został wprowadzony w 1896 roku i z powodzeniem używany przez Brytyjczyków podczas drugiej wojny burskiej w Afryce Południowej. W tym czasie dur brzuszny często zabijał więcej żołnierzy na wojnie, niż zginęło w walce wroga. Wright dalej rozwijał swoją szczepionkę w nowo otwartym dziale badawczym St Mary's Hospital Medical School w Londynie od 1902 roku, gdzie ustalił metodę pomiaru substancji ochronnych ( opsonina ) w ludzkiej krwi. Wersja Wrighta szczepionki przeciw durowi brzusznemu została wyprodukowana przez hodowanie bakterii w bulionie w temperaturze ciała , a następnie podgrzanie bakterii do 60 ° C w celu „dezaktywacji termicznej” patogenu, zabicia go, przy jednoczesnym zachowaniu nienaruszonych antygenów powierzchniowych. Zabite ciepłem bakterie zostały następnie wstrzyknięte pacjentowi. Aby wykazać skuteczność szczepionki, Wright zebrał próbki surowicy od pacjentów kilka tygodni po szczepieniu i przetestował zdolność ich surowicy do aglutynacji żywe bakterie duru brzusznego. Wynik „pozytywny” był reprezentowany przez zbrylanie się bakterii, co wskazywało, że organizm wytwarzał surowicę odpornościową (obecnie nazywaną przeciwciałami ) przeciwko patogenowi.
Powołując się na przykład drugiej wojny burskiej, podczas której wielu żołnierzy zmarło z powodu łatwych do uniknięcia chorób, Wright przekonał armię brytyjską , że należy wyprodukować 10 milionów dawek szczepionek dla żołnierzy wysyłanych na front zachodni , ratując w ten sposób nawet pół miliona istnień ludzkich podczas I wojny światowej . Armia brytyjska była jedynym bojownikiem w momencie wybuchu wojny, którego żołnierze byli w pełni uodpornieni na bakterię. Po raz pierwszy ich straty spowodowane walką przewyższyły straty spowodowane chorobami.
W 1909 r. Frederick F. Russell , lekarz armii amerykańskiej , przyjął szczepionkę Wrighta na dur brzuszny do użytku w armii, a dwa lata później jego program szczepień stał się pierwszym, w ramach którego zaszczepiono całą armię. Wyeliminował dur brzuszny jako istotną przyczynę zachorowalności i śmiertelności w armii amerykańskiej. Szczepienia przeciwko durowi brzusznemu członków armii amerykańskiej stały się obowiązkowe w 1911 r. Przed szczepionką wskaźnik zachorowań na dur brzuszny w wojsku wynosił 14 000 lub więcej na 100 000 żołnierzy. Do I wojny światowej wskaźnik zachorowań na tyfus u żołnierzy amerykańskich wynosił 37 na 100 000.
W czasie drugiej wojny światowej armia Stanów Zjednoczonych zezwoliła na stosowanie trójwalentnej szczepionki – zawierającej inaktywowane termicznie patogeny duru brzusznego, Paratyphi A i Paratyphi B.
W 1934 r. odkrycie antygenu otoczkowego Vi przez Arthura Felixa i pannę SR Margaret Pitt umożliwiło opracowanie bezpieczniejszej szczepionki z antygenem Vi – która jest obecnie szeroko stosowana. Arthur Felix i Margaret Pitt również wyizolowali szczep Ty2, który stał się szczepem macierzystym Ty21a , szczepu używanego obecnie jako żywa atenuowana szczepionka przeciwko durowi brzusznemu.
Antybiotyki i odporność
Chloramfenikol został wyizolowany ze Streptomyces przez dr Davida Gotlieba w latach czterdziestych XX wieku. W 1948 roku amerykańscy lekarze wojskowi przetestowali jego skuteczność w leczeniu chorych na dur brzuszny w Kuala Lumpur , Malezja. Osoby, które otrzymały pełny cykl leczenia, ustąpiły z infekcji, podczas gdy u pacjentów, którym podano niższą dawkę, doszło do nawrotu. Bezobjawowi nosiciele nadal wydalali prątki pomimo leczenia chloramfenikolem – tylko chorzy pacjenci uzyskali poprawę po zastosowaniu chloramfenikolu. Oporność na chloramfenikol stała się powszechna w Azji Południowo-Wschodniej w latach pięćdziesiątych XX wieku, a obecnie chloramfenikol jest stosowany tylko w ostateczności ze względu na częste występowanie oporności.
Terminologia
Choroba była określana różnymi nazwami, często związanymi z objawami, takimi jak gorączka żołądkowa, gorączka jelitowa, dur brzuszny, dziecięca gorączka remisyjna, gorączka powolna, gorączka nerwowa, gorączka pitogenna, gorączka drenażowa i niska gorączka.
Znani ludzie
- Cesarz Rzymu August (podejrzewany na podstawie zapisów historycznych, ale niepotwierdzony), przeżył.
- Albert, książę małżonek , mąż królowej Wielkiej Brytanii Wiktorii , zmarł w 24 dni po pierwszej wzmiance o „poczuciu się okropnie chorym”. Zmarł 14 grudnia 1861 po utracie apetytu, bezsenności, gorączce, dreszczach, obfitym poceniu się, wymiotach, wysypce, urojeniach, niemożności rozpoznania członków rodziny, nasilającej się wysypce na brzuchu, zmianie koloru języka, wreszcie w stanie skrajnego zmęczenia . Lekarz prowadzący William Jenner , ówczesny ekspert od tyfusu, zdiagnozował go.
- Edward VII z Wielkiej Brytanii, syn królowej Wiktorii , będąc jeszcze księciem Walii, miał prawie śmiertelny przypadek duru brzusznego.
- Car Rosji Mikołaj II przeżył, choroba trwała ok. 1900–1901. [ źródło opublikowane samodzielnie ]
- William Henry Harrison , dziewiąty prezydent Stanów Zjednoczonych Ameryki , zmarł 32 dni po zakończeniu swojej kadencji, w 1841 roku. Jest to najkrótsza kadencja sprawowana przez prezydenta Stanów Zjednoczonych.
- Wilbur Wright , współtwórca samolotu wraz z bratem Orvillem, zmarł na tyfus 32 lata przed Orvillem.
- Stephen A. Douglas , przeciwnik polityczny Abrahama Lincolna w 1858 i 1860 roku, zmarł na tyfus 3 czerwca 1861 roku.
- Ignacio Zaragoza , meksykański generał i polityk, zmarł w wieku 33 lat na tyfus 8 września 1862 roku.
- William Wallace Lincoln , syn prezydenta USA Abrahama i Mary Todd Lincoln, zmarł na tyfus w 1862 roku.
- Księżniczka Leopoldina z Brazylii , córka cesarza Piotra II , zmarła na tyfus w 1871 roku.
- Martha Bulloch Roosevelt , matka prezydenta Theodore'a Roosevelta i babka ze strony ojca Eleanor Roosevelt , zmarła na tyfus w 1884 roku.
- Mary Mallon , „Tyfusowa Mary” – więcej informacji można znaleźć w sekcji historii, „nosiciele”.
- Leland Stanford Jr. , syn amerykańskiego potentata i polityka A. Lelanda Stanforda i eponim Leland Stanford Junior University , zmarł na dur brzuszny w 1884 roku w wieku 15 lat.
- Troje z pięciorga dzieci Ludwika Pasteura zmarło na tyfus.
- Gerard Manley Hopkins , angielski poeta, zmarł na tyfus w 1889 roku.
- Lizzie van Zyl , południowoafrykańska więźniarka obozu koncentracyjnego Bloemfontein podczas drugiej wojny burskiej , zmarła na tyfus w 1901 roku.
- Dr HJH „Tup” Scott , kapitan australijskiej drużyny krykieta z 1886 roku, która podróżowała po Anglii, zmarł na tyfus w 1910 roku.
- Arnold Bennett , angielski powieściopisarz, zmarł w 1932 roku na tyfus, dwa miesiące po wypiciu szklanki wody w paryskim hotelu, aby udowodnić, że jest bezpieczna.
- Hakaru Hashimoto , japoński naukowiec medyczny, zmarł na tyfus w 1934 roku.
ogniska
- Plaga ateńska (podejrzewana)
- Wybuch „gorączki płonącej” wśród rdzennych Amerykanów . W latach 1607-1624 85% populacji nad rzeką James zmarło z powodu epidemii tyfusu. Światowa Organizacja Zdrowia szacuje, że w tym czasie liczba ofiar śmiertelnych wyniosła ponad 6000.
- Maidstone , Kent w latach 1897–1898: zarejestrowano 1847 pacjentów z durem brzusznym. Ta epidemia jest godna uwagi, ponieważ po raz pierwszy zastosowano szczepionkę przeciw durowi brzusznemu podczas epidemii cywilnej. Almotha Edwarda Wrighta została zaoferowana 200 pracownikom służby zdrowia, a spośród 84 osób, które otrzymały szczepionkę, żadna nie zachorowała na dur brzuszny, podczas gdy 4, które nie zostały zaszczepione, zachorowały.
- Armia amerykańska w wojnie hiszpańsko-amerykańskiej : dane rządowe szacują, że ponad 21 000 żołnierzy miało tyfus, w wyniku czego zginęło 2200 osób.
- W 1902 roku goście na bankietach burmistrzów w Southampton i Winchester w Anglii zachorowali, a czterech zmarło, w tym dziekan Winchester , po spożyciu ostryg. Infekcja była spowodowana ostrygami pochodzącymi z Emsworth , gdzie ławice ostryg zostały skażone nieoczyszczonymi ściekami.
- Dzielnica Jamaica Plain , Boston w 1908 r. - powiązana z dostawą mleka. Więcej informacji można znaleźć w sekcji historii, „przewoźnicy”.
- Epidemia wśród nowojorczyków z wyższej klasy, którzy zatrudniali Mary Mallon – 51 przypadków i 3 zgony w latach 1907-1915.
- Aberdeen , Szkocja, latem 1964 r. – pochodzenie od skażonej wołowiny w puszkach pochodzącej z Argentyny, sprzedawanej na rynkach. Ponad 500 pacjentów zostało poddanych kwarantannie w szpitalu przez co najmniej cztery tygodnie, a epidemia została powstrzymana bez zgonów.
- Duszanbe , Tadżykistan, w latach 1996–1997: 10 677 zgłoszonych przypadków, 108 zgonów
- Kinszasa , Demokratyczna Republika Konga, w 2004 r.: 43 000 przypadków i ponad 200 zgonów. Prospektywne badanie próbek pobranych w tym samym regionie w latach 2007-2011 wykazało, że około jedna trzecia próbek pobranych od pacjentów była oporna na wiele antybiotyków.
- Kampala , Uganda w 2015 r.: zgłoszono 10 230 przypadków
Zobacz też
- Pogorączkowe zapalenie siatkówki
Dalsza lektura
- Światowa Organizacja Zdrowia, Newsroom (31 stycznia 2018). „Tyfus: arkusz informacyjny” . Źródło 27 czerwca 2021 r .
- Kanadyjska Agencja Zdrowia Publicznego (2010). „Karty charakterystyki patogenu: Substancje zakaźne – Salmonella enterica spp” . Źródło 28 czerwca 2021 r .
- Centra Kontroli i Zapobiegania Chorobom (30 marca 2021 r.). „Dur brzuszny i dur rzekomy: informacje dla pracowników służby zdrowia” . Źródło 27 czerwca 2021 r .
- Narodowa Służba Zdrowia (18 czerwca 2018). „Dur brzuszny: przegląd” . Źródło 27 czerwca 2021 r .
- Adler R, Mara E (2016). Dur brzuszny: historia . Jefferson, Karolina Północna: McFarland & Company Inc. ISBN 978-0-7864-9781-2 .
-
GBD 2017 Tyfus i paratyfus, współpracownicy (kwiecień 2019). „Globalne obciążenie durem brzusznym i paratyfusem: systematyczna analiza na potrzeby badania Global Burden of Disease Study 2017” . Nazwa naukowego czasopisma medycznego. Choroby Zakaźne . 19 (4): 369–381. doi : 10.1016/S1473-3099(18)30685-6 . PMC 6437314 . PMID 30792131 .
{{ cite journal }}:|first1=ma nazwę ogólną ( pomoc )