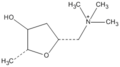
muskaryna
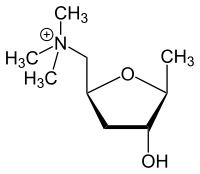
|
|

|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
2,5-Anhydro-1,4,6-trideoksy-6-(trimetyloamonio) -D - rybo -heksitol
|
|
|
Preferowana nazwa IUPAC
1-[(2S , 4R , 5S ) -4-hydroksy-5-metyloksolan-2-ylo]-N , N , N - trimetylometanoaminium |
|
| Inne nazwy
L -(+)-muskaryna, muskaryna, (2S , 4R , 5S ) -(4-hydroksy-5-metylo-tetrahydrofuran-2-ylometylo)-trimetylo-amoniowy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.005.541 |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C9H20NO2 + _ _ _ _ _ | |
| Masa cząsteczkowa | 174,26 g/mol |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Muskaryna , L -(+)-muskaryna lub muskaryna jest naturalnym produktem występującym w niektórych grzybach , szczególnie w gatunkach Inocybe i Clitocybe , takich jak śmiertelna C. dealbata . Stwierdzono również, że grzyby z rodzajów Entoloma i Mycena zawierają poziomy muskaryny, które mogą być niebezpieczne w przypadku spożycia. Muskarynę znaleziono w nieszkodliwych śladowych ilościach w borowikach , Hygrocybe , Lactarius i Russula . Śladowe stężenia muskaryny występują również w Amanita muscaria , chociaż farmakologicznie bardziej istotnym związkiem z tego grzyba jest alkaloid przypominający lek Z, muscimol . Owocniki A. muscaria zawierają zmienną dawkę muskaryny, zwykle około 0,0003% świeżej masy. Jest to bardzo niskie, a objawy toksyczności występują bardzo rzadko. Inocybe i Clitocybe zawierają muskarynę w stężeniu do 1,6%.
Muskaryna jest nieselektywnym agonistą muskarynowych receptorów acetylocholiny .
Historia
Nazwa muskaryna pochodzi od nazwy Amanita muscaria , z której została po raz pierwszy wyizolowana przez niemieckich chemików Oswalda Schmiedeberga i Richarda Koppe z Uniwersytetu w Dorpacie , którzy opisali swoje odkrycia w 1869 roku. Specyficzna nazwa grzyba z kolei pochodzi od łacińskiego musca oznaczającego latać, ponieważ grzyb był często używany do wabienia i łapania much, stąd jego potoczna nazwa „muchomor”.
Muskaryna była pierwszą badaną substancją parasympatykomimetyczną i powoduje głęboką aktywację obwodowego przywspółczulnego układu nerwowego , która może zakończyć się zapaścią krążeniową i śmiercią. Będąc czwartorzędową solą amoniową , muskaryna jest gorzej wchłaniana z przewodu pokarmowego niż aminy trzeciorzędowe i nie przekracza bariery krew-mózg . Agoniści muskarynowi aktywują receptory muskarynowe, podczas gdy agoniści nikotynowi aktywują receptory nikotynowe. Oba są cholinomimetykami o działaniu bezpośrednim; wytwarzają swoje efekty poprzez wiązanie i aktywację receptorów cholinergicznych. Ostateczny dowód struktury został przedstawiony przez Franza Jellinka i współpracowników w 1957 roku za pomocą analizy dyfrakcji rentgenowskiej ; Jellinek dalej opisał trójwymiarową strukturę cząsteczki przy użyciu chlorku muskaryny. Te nowe odkrycia zapoczątkowały badania nad farmakologią muskaryny i substancji podobnych do muskaryn, które są strukturalnie spokrewnione z acetylocholiną .
Struktura i reaktywność
Muskaryna naśladuje funkcję naturalnego neuroprzekaźnika acetylocholiny w muskarynowej części cholinergicznego układu nerwowego, pomimo mniej elastycznej struktury ze względu na pięcioczłonowy pierścień w szkielecie molekularnym. Z wyjątkiem podwójnego wiązania tlenu, cała struktura acetylocholiny jest obecna w prawej dolnej części muskaryny (patrz rysunek 3 poniżej dla porównania obu struktur).
Istnieją dwie lustrzane formy muskaryny, nazwane: 2S-muskaryna i 2R-muskaryna.
Wydajna synteza (+)-muskaryny
Poniższy schemat przedstawia bardzo wydajny sposób syntezy (+)-muskaryny według naukowców Chana i Li w kanadyjskim czasopiśmie Chemistry w 1992 roku. Mleczan S-(-)-etylu (2) (Rysunek 4) ulega konwersji do eteru 2,6-dichlorobenzylowego (3). Redukcja wodorkiem diizobutyloglinu (DIBAL) eteru 2,6-dichlorobenzylowego daje aldehyd (4). Traktowanie surowego aldehydu bromkiem allilu i proszkiem cynku w wodzie z NH4Cl jako katalizatorem dało w wyniku mieszaninę anty:syn 5a i 5b. Traktowanie 5a jodem w CH3 CN w temperaturze 0°C daje cyklizowany produkt 6a. Na koniec traktowanie związku 6a nadmiarem trimetyloaminy w etanolu dało (+)-muskarynę (2S,4R,5S). Podobna sekwencja reakcji z 5b dała (+)-epimuskarynę (7).
Inne syntezy
Można go syntetyzować na różne sposoby z zupełnie różnych substancji, zwłaszcza z 2,5-dimetylo-3-karboksymetylofluranu.
Farmakologia
Farmakodynamika
Muskaryna naśladuje działanie neuroprzekaźnika acetylocholiny poprzez agonizację muskarynowych receptorów acetylocholiny . Receptory te zostały nazwane na cześć muskaryny, aby odróżnić je od innych acetylocholiny ( receptorów nikotynowych ), które są stosunkowo niereagujące na muskarynę. Istnieje pięć różnych typów muskarynowych M4 receptorów M3 : M1 , M2 i , , M5 . Większość tkanek wyraża mieszaninę podtypów. M2 i M3 pośredniczą w odpowiedziach muskarynowych w obwodowych tkankach autonomicznych . Podtypy M1 i M4 występują liczniej w mózgu i zwojach autonomicznych . Receptory o numerach nieparzystych, M1 , M3 i M5 , oddziałują z białkami Gq stymulując hydrolizę fosfoinozytydu i uwalnianie wewnątrzkomórkowego wapnia. I odwrotnie, receptory o numerach parzystych, M 2 i M 4 oddziałują z białkami G i hamując cyklazę adenylową, co skutkuje zmniejszeniem wewnątrzkomórkowego stężenia cyklicznego monofosforanu adenozyny (cAMP). Większość agonistów receptorów muskarynowych nie jest selektywna względem podtypów.
Receptory muskarynowe sygnalizują również innymi szlakami, na przykład poprzez modulację kanałów potasowych przez kompleks G beta-gamma . Pozwala to muskarynie modulować pobudliwość komórkową poprzez potencjał błonowy .
Metabolizm
Istnieje niewiele badań dotyczących metabolizmu muskaryny w organizmie człowieka, co sugeruje, że związek ten nie jest metabolizowany przez ludzi. Chociaż przeprowadzono szeroko zakrojone badania w dziedzinie metabolizmu acetylocholiny przez acetylocholinoesterazę , muskaryna nie jest metabolizowana przez ten enzym, co częściowo wyjaśnia potencjalną toksyczność związku. Muskaryna jest łatwo rozpuszczalna w wodzie. Najbardziej prawdopodobnym sposobem opuszczenia krwi przez muskarynę jest klirens nerkowy; ostatecznie opuści ciało w moczu.
Zastosowania medyczne
Agoniści muskarynowi są stosowani jako leki w leczeniu jaskry , pooperacyjnej niedrożności jelit , wrodzonego rozszerzenia okrężnicy , zatrzymania moczu i kserostomii . Muskaryna jest przeciwwskazana u osób z chorobami, które czynią je podatnymi na stymulację przywspółczulną, u osób z astmą lub POChP lub u osób z chorobą wrzodową . Również osoby z niedrożnością przewodu pokarmowego lub dróg moczowych nie przepisuje się muskaryny, ponieważ nasila ona niedrożność, powodując wzrost ciśnienia, który może prowadzić do perforacji.
Skuteczność
Ponieważ muskaryna działa na muskarynowy receptor acetylocholiny , najlepsze porównanie można wykonać z acetylocholiną, która normalnie działa na ten receptor. Czysta muskaryna w porównaniu z czystą acetylocholiną jest w większości przypadków uważana za silniejszą, jej działanie jest zawsze wolniejsze, ale trwalsze niż acetylocholina. Możliwym wyjaśnieniem tego długotrwałego zachowania może być to, że muskaryna nie ulega hydrolizie przez acetylocholinoesterazę w szczelinie synaptycznej.
Toksykologia
Zatrucie muskaryną charakteryzuje się zwężeniem źrenic , niewyraźnym widzeniem, zwiększonym wydzielaniem śliny , nadmiernym poceniem się , łzawieniem , wydzieliną oskrzelową, skurczem oskrzeli, bradykardią , skurczami brzucha, zwiększonym wydzielaniem kwasu żołądkowego, biegunką i wielomoczem . Jeśli muskaryna dotrze do mózgu, może wywołać drżenie , konwulsje i hipotermię . Komory serca zawierają receptory muskarynowe które pośredniczą w zmniejszaniu siły skurczów, prowadząc do obniżenia ciśnienia krwi. Jeśli muskaryna jest podawana dożylnie, może wywołać ostrą niewydolność krążenia z zatrzymaniem akcji serca . Objawy zatrucia grzybami bogatymi w muskarynę, zwłaszcza Inocybe , są bardzo typowe: objawy zaczynają się wcześnie, po kwadransie do dwóch godzin, z bólem głowy, nudnościami, wymiotami i zwężeniem gardła . Następnie pojawia się ślinotok, łzawienie i rozproszone pocenie się, połączone ze zwężeniem źrenic, zaburzone akomodacja i ograniczone widzenie. Kolka żołądkowa i jelitowa prowadzi do biegunki i bolesnego parcia na mocz. Skurcz oskrzeli prowadzi do ataków astmy i ciężkiej duszności , a bradykardia połączona z wyraźnym niedociśnieniem i rozszerzeniem naczyń powoduje wstrząs krążeniowy . Śmierć po 8 do 9 godzinach odnotowano w około 5% przypadków, ale można jej całkowicie uniknąć poprzez szybkie podanie antycholinergicznych dożylnie lub domięśniowo .
Antidotum
Leki przeciwmuskarynowe , takie jak atropina , mogą być stosowane jako antidotum na muskarynę. Atropina, podobnie jak muskaryna, jest alkaloidem, ale w przeciwieństwie do muskaryny jest antagonistą receptorów muskarynowych. Tym samym hamuje działanie acetylocholiny. Antagoniści receptora muskarynowego rozszerzają źrenicę i rozluźniają mięsień rzęskowy, są stosowane w leczeniu zapalenia błony naczyniowej oka i są związane z jaskrą. Są również stosowane w leczeniu nietrzymania moczu i chorób charakteryzujących się nadmierną motoryką jelit, takich jak zespół jelita drażliwego . Często nazywa się antagonistami muskarynowymi leki parasympatykolityczne , ponieważ mają takie same działanie jak środki blokujące pozazwojowe nerwy przywspółczulne.