Borelioza
| Borelioza | |
|---|---|
| Inne nazwy | Borelioza z Lyme |
 | |
| Dorosły kleszcz jelenia (większość przypadków boreliozy jest powodowana przez nimfy, a nie przez dorosłe kleszcze) | |
| Specjalność | Choroba zakaźna |
| Objawy | Rozszerzający się obszar zaczerwienienia w miejscu ukąszenia przez kleszcza , gorączka , ból głowy , zmęczenie |
| Komplikacje | Porażenie nerwu twarzowego , zapalenie stawów , zapalenie opon mózgowych , Zaburzenia rytmu serca |
| Zwykły początek | Tydzień po ugryzieniu |
| Powoduje | Borrelia przenoszona przez kleszcze |
| Metoda diagnostyczna | Na podstawie objawów, ekspozycji na kleszcze, badań krwi |
| Zapobieganie | Zapobieganie ukąszeniom kleszczy (odzież kończyn, DEET ), doksycyklina |
| Lek | Doksycyklina , amoksycylina , ceftriakson , cefuroksym |
| Częstotliwość | ~ 476 000 rocznie w USA (prawdopodobnie przeszacowanie), 200 000 rocznie w Europie |
Choroba z Lyme , znana również jako borelioza z Lyme , jest chorobą przenoszoną przez wektory, wywoływaną przez bakterię Borrelia , która jest przenoszona przez kleszcze z rodzaju Ixodes . Najczęstszym objawem infekcji jest rozszerzająca się czerwona wysypka , znana jako rumień wędrujący (EM), która pojawia się w miejscu ukąszenia kleszcza około tydzień później. Wysypka zwykle nie swędzi ani nie boli. Około 70–80% zakażonych osób ma wysypkę. Wczesna diagnoza może być trudna. Inne wczesne objawy mogą obejmować gorączkę, bóle głowy i zmęczenie . Nieleczone objawy mogą obejmować utratę zdolności poruszania się po jednej lub obu stronach twarzy , bóle stawów , silne bóle głowy ze sztywnością karku lub kołatanie serca . Miesiące lub lata później mogą wystąpić powtarzające się epizody bólu stawów i obrzęku. Od czasu do czasu mogą wystąpić bóle przeszywające lub mrowienie w rękach i nogach. Pomimo odpowiedniego leczenia, u około 10 do 20% osób dotkniętych chorobą występują bóle stawów, problemy z pamięcią i zmęczenie przez co najmniej sześć miesięcy.
Borelioza jest przenoszona na ludzi przez ukąszenia zakażonych kleszczy z rodzaju Ixodes . W Stanach Zjednoczonych kleszcze budzące niepokój są zwykle typu Ixodes scapularis i muszą być przyczepione przez co najmniej 36 godzin, zanim bakterie będą mogły się rozprzestrzenić. W Europie Ixodes ricinus mogą szybciej rozprzestrzeniać bakterie. W Ameryce Północnej bakterie Borrelia burgdorferi i B. mayonii powodują boreliozę. W Europie i Azji Borrelia afzelii , Borrelia garinii , B. spielmanii a cztery inne gatunki również powodują chorobę. Wydaje się, że choroba nie jest przenoszona między ludźmi, przez inne zwierzęta ani przez żywność. Diagnoza opiera się na połączeniu objawów, historii ekspozycji na kleszcze i ewentualnie badaniu swoistych przeciwciał we krwi. Badania krwi są często fałszywie ujemne we wczesnych stadiach choroby. Testowanie pojedynczych kleszczy zazwyczaj nie jest przydatne.
Zapobieganie obejmuje wysiłki mające na celu zapobieganie ukąszeniom przez kleszcze poprzez noszenie odzieży zakrywającej ramiona i nogi oraz stosowanie środków odstraszających owady na bazie DEET lub pikarydyny . Skuteczne może być również stosowanie pestycydów w celu zmniejszenia liczby kleszczy. Kleszcze można usunąć za pomocą pęsety . Jeśli usunięty kleszcz jest pełen krwi , można zastosować pojedynczą dawkę doksycykliny , aby zapobiec rozwojowi zakażenia, ale ogólnie nie jest to zalecane, ponieważ rozwój zakażenia występuje rzadko. Jeśli rozwinie się infekcja, skutecznych jest wiele antybiotyków, w tym doksycyklina, amoksycylina i cefuroksym . Standardowe leczenie trwa zazwyczaj dwa lub trzy tygodnie. U niektórych osób w wyniku leczenia pojawia się gorączka oraz bóle mięśni i stawów, które mogą utrzymywać się przez jeden lub dwa dni. U osób, u których występują uporczywe objawy, długotrwała antybiotykoterapia okazała się nieprzydatna.
Borelioza jest najczęstszą chorobą przenoszoną przez kleszcze na półkuli północnej . Do infekcji najczęściej dochodzi wiosną i wczesnym latem. Borelioza została po raz pierwszy zdiagnozowana jako odrębna choroba w 1975 roku w Lyme, Connecticut . Pierwotnie mylono go z młodzieńczym reumatoidalnym zapaleniem stawów . Zaangażowana bakteria została po raz pierwszy opisana w 1981 roku przez Willy'ego Burgdorfera . Przewlekłe objawy po leczeniu są znane jako „zespół boreliozy po leczeniu” (PTLDS). PTLDS różni się od przewlekłej boreliozy , termin, który nie jest już wspierany przez naukowców i używany na różne sposoby przez różne grupy. Niektórzy pracownicy służby zdrowia twierdzą, że PTLDS jest spowodowane uporczywą infekcją, ale uważa się to za nieprawdę, ponieważ po standardowym leczeniu nie można znaleźć dowodów na uporczywą infekcję.
nie są dostępne żadne szczepionki dla ludzi na boreliozę , chociaż badania trwają. Dostępnych jest wiele szczepionek do zapobiegania chorobie z Lyme u psów.
Symptomy i objawy

Borelioza może wpływać na kilka układów organizmu i powodować szeroki zakres objawów. Nie wszyscy chorzy na boreliozę mają wszystkie objawy, a wiele z nich nie jest specyficznych dla boreliozy, ale mogą wystąpić również w przypadku innych chorób.
Okres inkubacji od zakażenia do wystąpienia objawów wynosi zwykle od jednego do dwóch tygodni, ale może być znacznie krótszy (dni) lub znacznie dłuższy (miesiące lub lata). Objawy boreliozy najczęściej występują od maja do września na półkuli północnej, ponieważ za większość przypadków odpowiada faza nimfalna kleszcza. Bezobjawowa infekcja istnieje, ale występuje u mniej niż 7% zakażonych osób w Stanach Zjednoczonych. Zakażenie bezobjawowe może być znacznie częstsze wśród zakażonych w Europie.
Wczesna zlokalizowana infekcja
Wczesna miejscowa infekcja może wystąpić, gdy infekcja nie rozprzestrzeniła się jeszcze po całym ciele. Dotyczy to tylko miejsca, w którym infekcja po raz pierwszy zetknęła się ze skórą. Początkowym objawem około 80% infekcji z Lyme jest wędrujący (EM) w miejscu ukąszenia przez kleszcza, często w pobliżu fałdów skórnych, takich jak pacha , pachwina lub tył kolana , na tułowiu , pod paskami odzieży lub we włosach, uszach lub szyi dzieci. Większość osób zarażonych nie pamięta kleszcza ani ugryzienia. Wysypka pojawia się zwykle po jednym lub dwóch tygodniach (przedział 3–32 dni) po ukąszeniu i rozszerza się o 2–3 cm dziennie do średnicy 5–70 cm (mediana 16 cm). Wysypka jest zwykle okrągła lub owalna, czerwona lub niebieskawa i może mieć uniesiony lub ciemniejszy środek. W około 79% przypadków w Europie, ale tylko w 19% przypadków na endemicznych obszarach Stanów Zjednoczonych, wysypka stopniowo ustępuje od środka w kierunku brzegów, prawdopodobnie tworząc wzór „strzału w dziesiątkę”. Wysypka może być ciepła, ale zwykle nie swędzi, rzadko jest tkliwa lub bolesna, a jeśli nie jest leczona, ustępuje do czterech tygodni.
Wysypce EM często towarzyszą objawy choroby wirusopodobnej, w tym zmęczenie, ból głowy, bóle ciała, gorączka i dreszcze, ale zwykle nie występują nudności ani problemy z górnymi drogami oddechowymi. Objawy te mogą również pojawić się bez wysypki lub utrzymywać się po ustąpieniu wysypki. Lyme może przejść do późniejszych etapów bez tych objawów lub wysypki.
Osoby z wysoką gorączką utrzymującą się dłużej niż dwa dni lub u których inne objawy choroby wirusopodobnej nie ulegają poprawie pomimo antybiotykoterapii boreliozy lub które mają nieprawidłowo niski poziom białych lub czerwonych krwinek lub płytek we krwi, powinny zostać zbadane pod kątem możliwej koinfekcji z innymi chorobami przenoszonymi przez kleszcze, takimi jak erlichioza i babeszjoza .
Wczesna rozsiana infekcja
W ciągu dni lub tygodni od wystąpienia miejscowej infekcji bakterie Borrelia mogą rozprzestrzeniać się przez układ limfatyczny lub krwiobieg. W 10–20% nieleczonych przypadków wysypka EM rozwija się w miejscach na całym ciele, które nie mają związku z pierwotnym ukąszeniem kleszcza. Częste są również przejściowe bóle mięśni i stawów .
U około 10-15% nieleczonych osób borelioza powoduje problemy neurologiczne znane jako neuroborelioza . Wczesna neuroborelioza zwykle pojawia się 4–6 tygodni (zakres 1–12 tygodni) po ukąszeniu przez kleszcza i obejmuje pewną kombinację limfocytarnego zapalenia opon mózgowo-rdzeniowych, zapalenia nerwu czaszkowego, radikulopatii i/lub mononeuritis multiplex. Limfocytowe zapalenie opon mózgowo-rdzeniowych powoduje charakterystyczne zmiany w płynie mózgowo- rdzeniowym i może mu towarzyszyć przez kilka tygodni zmienny ból głowy oraz, rzadziej, zwykle łagodne objawy zapalenia opon mózgowo-rdzeniowych , takie jak niemożność pełnego zgięcia szyi i nietolerancja jasnego światła , ale zazwyczaj brak lub tylko bardzo niska gorączka. Po kilku miesiącach neuroborelioza może również dawać objawy otolaryngologiczne. Do 76,5% z nich występuje jako szum w uszach, najczęstszy objaw. Kolejnymi najczęstszymi objawami były zawroty głowy i zawroty głowy (53,7%) oraz utrata słuchu (16,7%). U dzieci częściowa utrata wzroku . Zapalenie nerwu czaszkowego to zapalenie nerwów czaszkowych . Kiedy z powodu boreliozy, najczęściej powoduje porażenie nerwu twarzowego , upośledzające mruganie, uśmiechanie się i żucie po jednej lub obu stronach twarzy. Może również powodować przerywane podwójne widzenie . Borelioza z Lyme to zapalenie korzeni nerwów rdzeniowych , które często powoduje ból , a rzadziej osłabienie , drętwienie lub zaburzenia czucia w obszarach ciała obsługiwanych przez nerwy połączone z dotkniętymi korzeniami , np. kończyny lub części tułowia. Ból jest często opisywany jako niepodobny do żadnego wcześniej odczuwanego, rozdzierający, migrujący, nasilający się w nocy, rzadko symetryczny i często towarzyszą mu skrajne zaburzenia snu. Mononeuritis multiplex to stan zapalny powodujący podobne objawy w jednym lub kilku niezwiązanych ze sobą nerwach obwodowych. Rzadko wczesna neuroborelioza może obejmować zapalenie mózgu lub rdzenia kręgowego , z objawami takimi jak splątanie, nieprawidłowy chód, ruchy gałek ocznych lub mowa , zaburzenia ruchu , zaburzenia planowania motorycznego lub drżenie .
W Ameryce Północnej porażenie nerwu twarzowego jest typowym objawem wczesnej neuroboreliozy, występującym u 5–10% nieleczonych osób, w około 75% przypadków towarzyszy mu limfocytarne zapalenie opon mózgowo-rdzeniowych. Radikulopatię z Lyme zgłasza się o połowę rzadziej, ale wiele przypadków może pozostać nierozpoznanych. U dorosłych Europejczyków najczęstszym objawem jest połączenie limfocytarnego zapalenia opon mózgowo-rdzeniowych i radikulopatii znanej jako zespół Bannwartha , któremu towarzyszy w 36-89% przypadków porażenie nerwu twarzowego. W tym zespole ból korzeniowy ma tendencję do rozpoczynania się w tym samym obszarze ciała, co początkowa rumienia wędrującego , jeśli taka wystąpiła, i poprzedza możliwe porażenie nerwu twarzowego i inne zaburzenia ruchu . W skrajnych przypadkach może dojść do trwałego upośledzenia funkcji motorycznych lub czuciowych kończyn dolnych. U dzieci europejskich najczęstszymi objawami są porażenie nerwu twarzowego (u 55%), inne zapalenie nerwu czaszkowego i limfocytarne zapalenie opon mózgowo-rdzeniowych (u 27%).
W około 4–10% nieleczonych przypadków w USA i 0,3–4% nieleczonych przypadków w Europie, zwykle między czerwcem a grudniem, około miesiąca (zakres 4 dni-7 miesięcy) po ukąszeniu przez kleszcza, infekcja może powodować serce powikłania znane jako zapalenie serca z Lyme . Objawy mogą obejmować kołatanie serca (u 69% osób), zawroty głowy , omdlenia , duszność i ból w klatce piersiowej . Mogą również występować inne objawy boreliozy, takie jak wysypka EM , bóle stawów , porażenie nerwu twarzowego , bóle głowy lub bóle korzeniowe . Jednak u niektórych osób zapalenie serca może być pierwszą manifestacją boreliozy. Zapalenie serca z Lyme u 19–87% osób niekorzystnie wpływa na układ przewodzenia elektrycznego serca, powodując blok przedsionkowo-komorowy , który często objawia się rytmem serca naprzemiennym w ciągu kilku minut od nienormalnie wolnego do nienormalnie szybkiego. U 10–15% osób borelioza powoduje mięśnia sercowego , takie jak kardiomegalia , dysfunkcja lewej komory lub zastoinowa niewydolność serca.
Inną chorobą skóry występującą w Europie, ale nie w Ameryce Północnej, jest chłoniak borelialny , purpurowa grudka, która rozwija się na płatku ucha, sutku lub mosznie .
Późno rozsiane zakażenie
Zapalenie stawów z Lyme występuje nawet u 60% nieleczonych osób, zwykle zaczynając około sześć miesięcy po zakażeniu. Zwykle dotyczy tylko jednego lub kilku stawów, często kolana lub ewentualnie biodra , innych dużych stawów lub stawu skroniowo-żuchwowego . Zwykle występuje wysięk i obrzęk w dużych stawach, ale tylko łagodny lub umiarkowany ból. Bez leczenia obrzęk i ból zwykle ustępują z czasem, ale okresowo powracają. Torbiele Bakera mogą tworzyć się i pękać.
We wczesnych badaniach nad boreliozą w USA opisano rzadką neuropatię obwodową , która obejmowała drętwienie, mrowienie lub pieczenie rozpoczynające się od stóp lub dłoni iz czasem prawdopodobnie poruszające się w górę kończyn. W późniejszej analizie, która wykazała słabą dokumentację tej manifestacji, eksperci zastanawiali się, czy w ogóle istnieje ona w Stanach Zjednoczonych, czy też jest po prostu bardzo rzadka.
Zespół neurologiczny zwany encefalopatią z Lyme jest związany z subtelnymi problemami z pamięcią i zdolnościami poznawczymi, bezsennością , ogólnym złym samopoczuciem i zmianami osobowości. Encefalopatia z Lyme jest kontrowersyjna w Stanach Zjednoczonych i nie została zgłoszona w Europie. Problemy takie jak depresja i fibromialgia są tak samo powszechne u osób z boreliozą, jak w populacji ogólnej. Nie ma przekonujących dowodów na to, że borelioza powoduje zaburzenia psychiczne, zaburzenia zachowania (np. ADHD ) lub zaburzenia rozwojowe (np. autyzm ).
Acrodermatitis chronica atrophicans (ACA) to przewlekła choroba skóry obserwowana głównie w Europie u osób starszych. ACA zaczyna się jako czerwonawo-niebieska plama przebarwionej skóry, często na grzbietach dłoni lub stóp. Zmiana powoli zanika w ciągu kilku tygodni lub miesięcy, a skóra staje się najpierw cienka i pomarszczona, a następnie, jeśli nie jest leczona, całkowicie sucha i pozbawiona włosów. ACA jest również związana z neuropatią obwodową.
Przyczyna

Boreliozę wywołują krętki , bakterie spiralne z rodzaju Borrelia . Krętki są otoczone peptydoglikanem i wici , wraz z błoną zewnętrzną podobną do bakterii Gram-ujemnych. Ze względu na podwójną błonę otoczki, Borrelia są często błędnie opisywane jako Gram-ujemne, pomimo znacznych różnic w składnikach ich otoczki w porównaniu z bakteriami Gram-ujemnymi. Gatunki Borrelia spokrewnione z Lyme są wspólnie określane jako Borrelia burgdorferi sensu lato i wykazują dużą różnorodność genetyczną .
B. burgdorferi sensu lato to kompleks gatunkowy składający się z 20 zaakceptowanych i trzech proponowanych genogatunków. Wiadomo, że osiem gatunków powoduje boreliozę: B. mayonii (występująca w Ameryce Północnej), B. burgdorferi sensu stricto (występująca w Ameryce Północnej i Europie), B. afzelii , B. garinii, B. spielmanii i B. lusitaniae (wszystkie znalezione w Eurazji ). Niektóre badania sugerowały również, że B. valaisiana może czasami zarażać ludzi, ale gatunek ten nie wydaje się być ważną przyczyną choroby.
Zaznacz cykl życia

Cykl życiowy kleszcza składa się z trzech etapów. Larwa, nimfa i postać dorosła. W fazie nimfy kleszcze najczęściej przenoszą boreliozę i są zwykle najbardziej aktywne późną wiosną i wczesnym latem w regionach o łagodnym klimacie. W fazie dorosłej przenoszenie boreliozy jest mniej powszechne ze względu na fakt, że dorosłe kleszcze mają mniejsze szanse na ukąszenie ludzi oraz ponieważ są one zwykle większe i dlatego można je łatwo zobaczyć i usunąć.
Przenoszenie
Borelioza jest klasyfikowana jako choroba odzwierzęca , ponieważ jest przenoszona na ludzi z naturalnego rezerwuaru małych ssaków i ptaków przez kleszcze , które żywią się obydwoma grupami żywicieli . Kleszcze twarde z rodzaju Ixodes są nosicielami boreliozy (również wektor Babesia ). Większość infekcji jest wywoływana przez kleszcze w stadium nimfalnym , ponieważ są bardzo małe i dlatego mogą żerować przez długi czas niewykryte. Kleszcze nimfy są na ogół wielkości maku, a czasami mają ciemną głowę i półprzezroczyste ciało. Lub kleszcze nimfalne mogą być ciemniejsze. (Młodsze larwy kleszczy są bardzo rzadko zarażone.) Chociaż jelenie są preferowanymi żywicielami dorosłych kleszczy jeleniowatych, a populacje kleszczy są znacznie mniejsze w przypadku braku jeleni, kleszcze na ogół nie zarażają się Borrelią od jeleni, zamiast tego pozyskują ją od zakażonych małych ssaki, takie jak mysz białonoga , a czasami ptaki. Obszary, w których borelioza jest powszechna, rozszerzają się.
W jelicie środkowym kleszcza białko A (OspA) powierzchni zewnętrznej Borrelii wiąże się z receptorem OspA kleszcza, znanym jako TROSPA . Kiedy kleszcz się żeruje, Borrelia obniża poziom OspA i zwiększa poziom OspC, innego białka powierzchniowego. Po migracji bakterii z jelita środkowego do gruczołów ślinowych, OspC wiąże się z Salp15, białkiem śliny kleszcza, które wydaje się mieć działanie immunosupresyjne, które nasila infekcję. Pomyślna infekcja gospodarza ssaka zależy od bakteryjnej ekspresji OspC.
Ukąszenia kleszczy często pozostają niezauważone ze względu na mały rozmiar kleszcza w fazie nimfalnej, a także wydzieliny kleszczy, które uniemożliwiają żywicielowi odczuwanie swędzenia lub bólu po ukąszeniu. Jednak transmisja jest dość rzadka, a tylko około 1,2 do 1,4 procent rozpoznanych ukąszeń kleszczy powoduje boreliozę.

W Europie głównym nosicielem jest Ixodes ricinus , zwany także kleszczem owczym lub kleszczem rycynowym . W Chinach Ixodes persulcatus (kleszcz tajga) jest prawdopodobnie najważniejszym wektorem. W Ameryce Północnej kleszcz czarnonogi lub kleszcz jeleni ( Ixodes scapularis ) jest głównym nosicielem na wschodnim wybrzeżu.
Samotny kleszcz ( Amblyomma americanum ), który występuje w południowo-wschodnich Stanach Zjednoczonych aż do Teksasu , raczej nie przenosi krętków boreliozy , chociaż może być powiązany z pokrewnym zespołem zwanym południową chorobą wysypkową związaną z kleszczami , która przypomina łagodną postać boreliozy.
Na zachodnim wybrzeżu Stanów Zjednoczonych głównym wektorem jest kleszcz czarnonogi ( Ixodes pacificus ). Skłonność tego gatunku kleszczy do żerowania głównie na gatunkach żywicieli, takich jak zachodnia jaszczurka płotowa , które są odporne na infekcję Borrelia , wydaje się zmniejszać przenoszenie boreliozy na Zachodzie.
może dojść do przeniesienia przez łożysko i podobnie jak w przypadku wielu innych chorób wywołanych przez krętki, w przypadku nieleczonej infekcji możliwe są niekorzystne skutki ciąży; szybkie leczenie antybiotykami zmniejsza lub eliminuje to ryzyko.
Nie ma naukowych dowodów potwierdzających przenoszenie boreliozy poprzez transfuzję krwi, kontakt seksualny lub mleko matki.
Koinfekcje przenoszone przez kleszcze
Kleszcze, które przenoszą B. burgdorferi na ludzi, mogą również przenosić i przenosić kilka innych drobnoustrojów, takich jak Babesia microti i Anaplasma phagocytophilum , które powodują odpowiednio choroby babeszjozy i ludzkiej anaplazmozy granulocytarnej (HGA). Wśród osób z wczesną boreliozą, w zależności od lokalizacji, 2–12% będzie miało również HGA, a 2–10% będzie miało babeszjozę. Kleszcze w niektórych regionach przenoszą również wirusy wywołujące kleszczowe zapalenie mózgu i chorobę wirusową Powassan . Koinfekcje boreliozy mogą nie wymagać dodatkowego leczenia, ponieważ mogą ustąpić samoistnie lub – jak w przypadku HGA – można je leczyć doksycykliną przepisywaną na boreliozę. Utrzymująca się gorączka lub zgodne nieprawidłowe wyniki badań laboratoryjnych mogą wskazywać na koinfekcję.
Patofizjologia
B. burgdorferi może rozprzestrzeniać się po całym ciele w trakcie choroby i została wykryta w skórze, sercu, stawach, obwodowym układzie nerwowym i ośrodkowym układzie nerwowym. B. Burgdorferi nie wytwarza toksyn. Dlatego wiele objawów boreliozy jest konsekwencją odpowiedzi immunologicznej na krętki w tych tkankach.
B. burgdorferi jest wstrzykiwana pod skórę przez ukąszenie zakażonego kleszcza Ixodes . Ślina kleszcza, która towarzyszy krętkowi wnikając w skórę podczas procesu żerowania, zawiera substancje zaburzające odpowiedź immunologiczną w miejscu ukąszenia. Zapewnia to środowisko ochronne, w którym krętek może wywołać infekcję. Krętki rozmnażają się i migrują na zewnątrz w skórze właściwej . Reakcja zapalna gospodarza na bakterie w skórze powoduje charakterystyczne okrągłe uszkodzenie EM. Neutrofile jednakże, które są niezbędne do usunięcia krętków ze skóry, nie pojawiają się w niezbędnej liczbie w rozwijającej się zmianie EM, ponieważ ślina kleszcza hamuje funkcję neutrofili. Pozwala to bakteriom przetrwać i ostatecznie rozprzestrzenić się po całym ciele.
Kilka dni lub tygodni po ukąszeniu przez kleszcza krętki rozprzestrzeniają się z krwią do stawów, serca, układu nerwowego i odległych miejsc na skórze, gdzie ich obecność powoduje różnorodne objawy rozsianej choroby. Rozprzestrzenianie się B. burgdorferi jest wspomagane przez przyłączenie plazminy proteazy gospodarza do powierzchni krętka.
Nieleczona bakteria może utrzymywać się w organizmie przez miesiące, a nawet lata, pomimo wytwarzania przeciwciał przeciwko B. burgdorferi przez układ odpornościowy. Krętki mogą uniknąć odpowiedzi immunologicznej poprzez zmniejszenie ekspresji białek powierzchniowych, które są celem przeciwciał, zmienność antygenową białka powierzchniowego VlsE, inaktywację kluczowych składników układu odpornościowego, takich jak dopełniacz , oraz ukrywanie się w macierzy pozakomórkowej , co może zakłócać funkcję układu odpornościowego. czynniki.
W mózgu B. burgdorferi może indukować astrocyty do astrogliozy (proliferacja, po której następuje apoptoza ), co może przyczyniać się do neurodysfunkcji. Krętki mogą również indukować komórki gospodarza do wydzielania kwasu chinolinowego , który stymuluje receptor NMDA na komórkach nerwowych, co może odpowiadać za zmęczenie i złe samopoczucie obserwowane w przypadku encefalopatii z Lyme . Ponadto rozproszona patologia istoty białej podczas encefalopatii z Lyme może zaburzać istotę szarą połączeń i może odpowiadać za deficyty uwagi, pamięci, zdolności wzrokowo-przestrzennych, złożonego poznania i stanu emocjonalnego. Choroba istoty białej może mieć większy potencjał wyzdrowienia niż choroba istoty szarej, być może dlatego, że utrata neuronów jest mniej powszechna. Obserwowano ustąpienie hiperintensywności istoty białej w badaniu MRI po leczeniu antybiotykami.
Tryptofan , prekursor serotoniny , wydaje się być zmniejszony w ośrodkowym układzie nerwowym w wielu chorobach zakaźnych, które wpływają na mózg, w tym na boreliozę. Naukowcy badają, czy to wydzielanie neurohormonu jest przyczyną neuropsychiatrycznych rozwijających się u niektórych osób z boreliozą.
Badania immunologiczne
Ekspozycja na bakterię Borrelia podczas boreliozy prawdopodobnie powoduje długotrwałą i szkodliwą odpowiedź zapalną , formę choroby autoimmunologicznej wywołanej patogenem. Wytwarzanie tej reakcji może być spowodowane formą mimikry molekularnej , w której Borrelia unika zabicia przez układ odpornościowy, przypominając normalne części tkanek ciała.
Przewlekłe objawy reakcji autoimmunologicznej mogą wyjaśniać, dlaczego niektóre objawy utrzymują się nawet po wyeliminowaniu krętków z organizmu. Ta hipoteza może wyjaśniać, dlaczego przewlekłe zapalenie stawów utrzymuje się po antybiotykoterapii, podobnie jak gorączka reumatyczna , ale jej szersze zastosowanie jest kontrowersyjne.
Diagnoza
Chorobę z Lyme rozpoznaje się na podstawie objawów, obiektywnych objawów fizycznych (takich jak rumień wędrujący (EM), porażenie nerwu twarzowego lub zapalenie stawów ), historii możliwej ekspozycji na zakażone kleszcze i ewentualnie badań laboratoryjnych . Osoby z objawami wczesnej boreliozy powinny poddać się badaniu skóry całego ciała w kierunku wysypki EM i zapytać, czy wysypka typu EM ujawniła się w ciągu ostatnich 1–2 miesięcy. Obecność wysypki EM i niedawna ekspozycja na kleszcza (tj. przebywanie na zewnątrz w prawdopodobnym środowisku kleszczy, gdzie borelioza jest powszechna , w ciągu 30 dni od pojawienia się wysypki) są wystarczające do rozpoznania boreliozy; żadne potwierdzenie laboratoryjne nie jest potrzebne ani zalecane. Większość osób zarażonych nie pamięta kleszcza ani ugryzienia, a wysypka EM nie musi wyglądać jak strzał w dziesiątkę (większość wysypek EM w USA nie) ani nie muszą jej towarzyszyć żadne inne objawy. W Stanach Zjednoczonych borelioza występuje najczęściej w Nowej Anglii i stanach środkowoatlantyckich oraz w częściach Wisconsin i Minnesoty , ale rozszerza się na inne obszary. Kilka przygranicznych obszarów Kanady również charakteryzuje się wysokim ryzykiem boreliozy.
W przypadku braku wysypki EM lub historii ekspozycji na kleszcze, rozpoznanie boreliozy zależy od potwierdzenia laboratoryjnego. Bakterie wywołujące boreliozę są trudne do zaobserwowania bezpośrednio w tkankach organizmu, a także trudne i zbyt czasochłonne do wyhodowania w laboratorium. Najszerzej stosowane testy szukają zamiast tego obecności przeciwciał przeciwko tym bakteriom we krwi. Dodatni wynik testu na obecność przeciwciał sam w sobie nie dowodzi aktywnej infekcji, ale może potwierdzić infekcję, która jest podejrzewana na podstawie objawów, obiektywnych wyników i historii narażenia na kleszcze u danej osoby. Ponieważ aż 5–20% normalnej populacji ma przeciwciała przeciwko boreliozie, osoby bez wywiadu i objawów sugerujących boreliozę nie powinny być badane na obecność przeciwciał z Lyme: pozytywny wynik byłby prawdopodobnie fałszywy, prawdopodobnie powodując niepotrzebne leczenie.
W niektórych przypadkach, gdy historia, oznaki i objawy silnie sugerują wczesną rozsianą boreliozę, można rozpocząć leczenie empiryczne i ponownie ocenić, gdy dostępne będą wyniki badań laboratoryjnych.
Testowane laboratoryjnie
Testy na przeciwciała we krwi za pomocą testu ELISA i Western blot są najczęściej stosowaną metodą diagnozowania boreliozy. Centrum Kontroli i Zapobiegania Chorobom (CDC) zaleca dwupoziomowy protokół : najpierw przeprowadzany jest czuły test ELISA, a jeśli wynik jest pozytywny lub niejednoznaczny, przeprowadza się bardziej specyficzny test Western blot. Układ odpornościowy potrzebuje trochę czasu, aby wytworzyć przeciwciała w odpowiedniej ilości. Po wystąpieniu infekcji z Lyme przeciwciała typu IgM i IgG zwykle można je wykryć po raz pierwszy odpowiednio po 2–4 tygodniach i 4–6 tygodniach, a szczyt po 6–8 tygodniach. Kiedy po raz pierwszy pojawia się wysypka EM, wykrywalne przeciwciała mogą nie być obecne. Dlatego zaleca się, aby nie przeprowadzać testów i opierać diagnozę na obecności wysypki EM. Do 30 dni po wystąpieniu podejrzenia zakażenia boreliozą zakażenie można potwierdzić wykrywając przeciwciała IgM lub IgG; po tym zaleca się, aby brać pod uwagę tylko przeciwciała IgG. Dodatni wynik testu IgM i ujemny IgG po pierwszym miesiącu infekcji generalnie wskazuje na wynik fałszywie dodatni. Liczba przeciwciał IgM zwykle spada po 4–6 miesiącach od zakażenia, podczas gdy przeciwciała IgG mogą pozostać wykrywalne przez lata.
Inne testy mogą być stosowane w przypadkach neuroboreliozy. W Europie neuroborelioza jest zwykle wywoływana przez Borrelia garinii i prawie zawsze wiąże się z pleocytozą limfocytarną , tj. gęstość limfocytów (komórek zwalczających infekcje) i białka w płynie mózgowo-rdzeniowym zazwyczaj wzrasta do charakterystycznie nieprawidłowego poziomu, podczas gdy poziom glukozy pozostaje prawidłowy. Dodatkowo układ odpornościowy wytwarza przeciwciała przeciwko boreliozie w przestrzeni wewnątrzoponowej, która zawiera płyn mózgowo-rdzeniowy. Demonstracja przez nakłucie lędźwiowe oraz analiza płynu mózgowo-rdzeniowego pod kątem pleocytozy i produkcji przeciwciał dooponowych są wymagane do ostatecznego rozpoznania neuroboreliozy w Europie (z wyjątkiem przypadków neuropatii obwodowej związanej z acrodermatitis chronica atrophicans , która jest zwykle wywoływana przez Borrelia afzelii i potwierdzona testami na obecność przeciwciał we krwi). W Ameryce Północnej neuroboreliozę wywołuje Borrelia burgdorferi i nie mogą im towarzyszyć te same objawy płynu mózgowo-rdzeniowego; potwierdzają diagnozę neuroboreliozy ośrodkowego układu nerwowego (OUN), jeśli są dodatnie, ale nie wykluczają jej, jeśli są ujemne. Amerykańskie wytyczne uznają analizę płynu mózgowo-rdzeniowego za opcjonalną, gdy objawy wydają się ograniczać do obwodowego układu nerwowego (PNS), np. porażenie nerwu twarzowego bez jawnych objawów zapalenia opon mózgowo-rdzeniowych. W przeciwieństwie do testów krwi i przeciwciał podoponowych, testy pleocytozy płynu mózgowo-rdzeniowego wracają do normy po zakończeniu infekcji i dlatego mogą być wykorzystywane jako obiektywne wskaźniki powodzenia leczenia i pomagają w podejmowaniu decyzji o wycofaniu się. W zakażeniach obejmujących badanie PUN, elektromiografii i przewodnictwa nerwowego można wykorzystać do obiektywnego monitorowania odpowiedzi na leczenie.
W zapaleniu serca z Lyme elektrokardiogramy są wykorzystywane do wykazania nieprawidłowości przewodzenia w sercu, podczas gdy echokardiografia może wykazać dysfunkcję mięśnia sercowego . Biopsja i potwierdzenie obecności komórek Borrelia w tkance mięśnia sercowego mogą być stosowane w szczególnych przypadkach, ale zwykle nie są wykonywane ze względu na ryzyko zabiegu.
reakcji łańcuchowej polimerazy (PCR) na boreliozę zostały również opracowane w celu wykrycia materiału genetycznego ( DNA ) krętka boreliozy. Hodowla lub PCR są obecnymi sposobami wykrywania obecności organizmu, ponieważ badania serologiczne wykrywają tylko przeciwciała Borrelia . PCR ma tę zaletę, że jest znacznie szybszy niż hodowla. Jednak testy PCR są podatne na fałszywie dodatnie wyniki wyników, np. poprzez wykrycie szczątków martwych komórek Borrelia lub zanieczyszczenia próbki. Nawet prawidłowo przeprowadzona reakcja PCR często daje wyniki fałszywie ujemne, ponieważ podczas infekcji we krwi i płynie mózgowo-rdzeniowym (CSF) można znaleźć niewiele komórek Borrelia . Dlatego testy PCR zalecane są tylko w szczególnych przypadkach, np. w diagnostyce boreliozy z Lyme, ponieważ jest to bardzo czuły sposób wykrywania DNA ospA w płynie maziowym. Chociaż czułość PCR w płynie mózgowo-rdzeniowym jest niska, można rozważyć jej zastosowanie w przypadku podejrzenia fałszywie ujemnego wyniku dooponowego testu wytwarzania przeciwciał, np. w bardzo wczesnej (< 6 tyg.) neuroboreliozie lub w z obniżoną odpornością .
Dostępnych jest kilka innych form testów laboratoryjnych na boreliozę, z których niektóre nie zostały odpowiednio zweryfikowane. Antygeny OspA wydalane przez żywe bakterie Borrelia do moczu to obiecująca technika, która jest obecnie badana. Badane jest wykorzystanie nanocząstek do ich wykrywania, a OspA powiązano z aktywnymi objawami boreliozy. Wysokie miana przeciwciał immunoglobulin G (IgG) lub immunoglobulin M (IgM) przeciwko antygenom Borrelia wskazują na chorobę, ale niższe miana mogą wprowadzać w błąd, ponieważ przeciwciała IgM mogą pozostać po początkowej infekcji, a przeciwciała IgG mogą pozostać przez lata.
B. burgdorferi z niedoborem ściany komórkowej oraz testów transformacji limfocytów.
Obrazowanie
Neuroobrazowanie jest kontrowersyjne, jeśli chodzi o to, czy dostarcza specyficznych wzorców charakterystycznych dla neuroboreliozy , ale może pomóc w diagnostyce różnicowej i zrozumieniu patofizjologii choroby. Choć kontrowersyjne, niektóre dowody wskazują, że niektóre testy neuroobrazowania mogą dostarczyć danych pomocnych w diagnozie danej osoby. Rezonans magnetyczny (MRI) i emisyjna tomografia komputerowa pojedynczych fotonów (SPECT) to dwa testy, które mogą zidentyfikować nieprawidłowości w mózgu osoby dotkniętej tą chorobą. Wyniki neuroobrazowania w MRI obejmują zmiany w istocie białej okołokomorowej, a także powiększone komory i zanik kory mózgowej. Odkrycia są uważane za dość nietypowe, ponieważ stwierdzono, że zmiany są odwracalne po leczeniu antybiotykami. Obrazy uzyskane za pomocą SPECT pokazują liczne obszary, w których do kory mózgowej i istoty białej podkorowej dostarczana jest niewystarczająca ilość krwi. Wiadomo jednak, że obrazy SPECT są niespecyficzne, ponieważ wykazują niejednorodny wzór w obrazowaniu. Nieprawidłowości widoczne na obrazach SPECT są bardzo podobne do tych obserwowanych u osób z zapaleniem naczyń mózgowych i Choroba Creutzfeldta-Jakoba , co czyni je wątpliwymi.
Diagnostyka różnicowa
Zgłoszono, że kliniki środowiskowe błędnie diagnozują 23–28% wysypek Erythema migrans (EM) i 83% innych obiektywnych objawów wczesnej boreliozy. Wysypki EM są często błędnie diagnozowane jako ukąszenia pająków , zapalenie tkanki łącznej lub półpasiec . Wiele błędnych diagnoz przypisuje się powszechnemu błędnemu przekonaniu, że wysypki EM powinny wyglądać jak strzał w dziesiątkę. W rzeczywistości kluczowymi cechami wyróżniającymi wysypkę EM jest szybkość i stopień jej rozszerzania się, odpowiednio do 2–3 cm/dobę i średnicy co najmniej 5 cm, a w 50% przypadków powyżej 16 cm. Wysypka rozszerza się od środka, który może, ale nie musi, wyglądać inaczej lub być oddzielony pierścieniowym prześwitem od reszty wysypki. W porównaniu z wysypkami EM, ukąszenia pająków są bardziej powszechne w kończynach, są bardziej bolesne i swędzą lub stają się opuchnięte, a niektóre mogą powodować martwicę (zapadanie ciemnoniebieskiej plamy martwej skóry). Zapalenie tkanki łącznej najczęściej rozwija się wokół rany lub owrzodzenia, rzadko jest okrągłe i jest bardziej prawdopodobne, że stanie się obrzęknięte i tkliwe. Wysypki EM często pojawiają się w miejscach nietypowych dla zapalenia tkanki łącznej, takich jak pachy, pachwiny, brzuch lub tył kolana. Jak Lyme, półpasiec często zaczyna się od bólu głowy, gorączki i zmęczenia, po których następuje ból lub drętwienie. Jednak w przeciwieństwie do boreliozy, w przypadku półpaśca po tych objawach zwykle pojawiają się wysypki składające się z wielu małych pęcherzy wraz z dermatomem nerwu , a półpasiec można również potwierdzić szybkimi testami laboratoryjnymi.
Porażenie twarzy spowodowane chorobą z Lyme (LDFP) jest często błędnie diagnozowane jako porażenie Bella . Chociaż porażenie Bella jest najczęstszym rodzajem jednostronnego porażenia twarzy (około 70% przypadków), LDFP może odpowiadać za około 25% przypadków porażenia twarzy na obszarach, gdzie borelioza jest powszechna. W porównaniu z LDFP porażenie Bella znacznie rzadziej dotyczy obu stron twarzy. Mimo że LDFP i porażenie Bella mają podobne objawy i ewoluują podobnie, jeśli nie są leczone, leczenie kortykosteroidami jest korzystne w przypadku porażenia Bella, a jednocześnie jest szkodliwe dla LDFP. Niedawna historia narażenia na prawdopodobne siedlisko kleszczy podczas cieplejszych miesięcy, wysypka EM, objawy wirusopodobne, takie jak ból głowy i gorączka i / lub porażenie po obu stronach twarzy, powinna zostać oceniona pod kątem prawdopodobieństwa wystąpienia LDFP; jeśli jest więcej niż minimalna, empiryczną terapię antybiotykami należy rozpocząć bez kortykosteroidów i ponownie ocenić po zakończeniu badań laboratoryjnych w kierunku boreliozy.
W przeciwieństwie do wirusowego zapalenia opon mózgowo-rdzeniowych , limfocytowe zapalenie opon mózgowo-rdzeniowych z Lyme zwykle nie powoduje gorączki, trwa dłużej i nawraca. Limfocytowe zapalenie opon mózgowo-rdzeniowych charakteryzuje się również możliwym współwystępowaniem wysypki EM , porażeniem twarzy lub częściową niedrożnością widzenia oraz znacznie mniejszym odsetkiem leukocytów wielojądrzastych w płynie mózgowo-rdzeniowym .
Radikulopatia z Lyme atakująca kończyny jest często błędnie diagnozowana jako radikulopatia spowodowana uciskiem na korzenie nerwowe, taka jak rwa kulszowa . Chociaż większość przypadków radikulopatii ma charakter uciskowy i ustępuje po leczeniu zachowawczym (np. odpoczynkiem) w ciągu 4–6 tygodni, wytyczne dotyczące leczenia radikulopatii zalecają najpierw ocenę ryzyka innych możliwych przyczyn, które choć występują rzadziej, wymagają natychmiastowej diagnozy i leczenia, w tym infekcji, takich jak jak borelioza i półpasiec. Historia aktywności na świeżym powietrzu w prawdopodobnych siedliskach kleszczy w ciągu ostatnich 3 miesięcy, po której może wystąpić wysypka lub objawy wirusopodobne, a obecny ból głowy, inne objawy limfocytowego zapalenia opon mózgowych lub porażenie nerwu twarzowego prowadzi do podejrzenia boreliozy i zalecenia badań serologicznych i nakłucie lędźwiowe testy na potwierdzenie.
Radikulopatia z Lyme atakująca tułów może być błędnie diagnozowana jako niezliczona ilość innych schorzeń, takich jak zapalenie uchyłków i ostry zespół wieńcowy . Rozpoznanie późnej postaci boreliozy jest często komplikowane przez wieloaspektowy wygląd i niespecyficzne objawy, co skłoniło jednego z recenzentów do nazwania boreliozy nowym „wielkim naśladowcą”. Ponieważ wszystkie osoby z późniejszą infekcją będą miały pozytywny wynik testu na obecność przeciwciał, proste badania krwi mogą wykluczyć boreliozę jako możliwą przyczynę objawów u danej osoby.
Zapobieganie
Ukąszeniom kleszczy można zapobiegać, unikając lub skracając czas przebywania w prawdopodobnych siedliskach kleszczy oraz podejmując środki ostrożności podczas przebywania w jednym z nich i wychodzenia z niego.
Większość infekcji u ludzi z Lyme jest spowodowana ukąszeniami nimfy Ixodes między kwietniem a wrześniem. Kleszcze preferują wilgotne, zacienione miejsca w lasach , krzewach, wysokich trawach i ściółce lub stosach drewna. Zagęszczenie kleszczy jest zwykle najwyższe na terenach leśnych, następnie nieutrzymywane krawędzie między lasami i trawnikami (mniej więcej o połowę mniejsze), rośliny ozdobne i byliny okrywowe (około jedna czwarta) oraz trawniki (około 30 razy mniej). Larwy i nimfy Ixodes są zwykle liczne również tam, gdzie gniazdują myszy, na przykład na kamiennych ścianach i kłody drewna. Larwy i nimfy Ixodes zazwyczaj czekają na potencjalnych żywicieli („poszukiwanie”) na liściach lub trawach blisko ziemi z wyciągniętymi przednimi łapami; kiedy żywiciel ociera się o jego kończyny, kleszcz szybko przylega i wspina się na żywiciela, szukając miejsca na skórze do ugryzienia. Szacuje się, że w północno-wschodnich Stanach Zjednoczonych 69% ukąszeń kleszczy ma miejsce w domach, 11% w szkołach lub na obozach, 9% w parkach lub na terenach rekreacyjnych, 4% w pracy, 3% podczas polowań i 4% na innych obszarach. Czynności związane z ukąszeniami kleszczy w pobliżu rezydencji obejmują prace na podwórku, oczyszczanie krzaków, prace w ogrodzie, zabawę na podwórku i wpuszczanie do domu psów lub kotów, które wędrują na zewnątrz po obszarach leśnych lub trawiastych. W parkach ukąszenia kleszczy często zdarzają się podczas wędrówek lub biwakowania. Chodzenie po skoszonym trawniku lub środku ścieżki bez dotykania sąsiedniej roślinności jest mniej ryzykowne niż czołganie się lub siadanie na kłodzie lub kamiennej ścianie. Zwierzęta nie powinny mieć możliwości swobodnego poruszania się po prawdopodobnych siedliskach kleszczy.
Jako środek ostrożności CDC zaleca namaczanie lub spryskiwanie odzieży, butów i sprzętu kempingowego, takiego jak namioty, plecaki i śpiwory, 0,5% permetryną roztworu i powiesić do wyschnięcia przed użyciem. Permetryna jest bezwonna i bezpieczna dla ludzi, ale wysoce toksyczna dla kleszczy. Po pełzaniu po tkaninie nasączonej permetryną przez zaledwie 10–20 sekund nimfy kleszczy stają się podrażnione i odpadają lub umierają. Buty i skarpetki z zamkniętymi palcami poddane działaniu permetryny zmniejszają 74-krotnie liczbę ukąszeń przez nimfy, które po raz pierwszy stykają się z butem osoby noszącej również leczone szorty (ponieważ nimfy zwykle szukają blisko ziemi, jest to typowy scenariusz kontaktu). Lepszą ochronę można osiągnąć, wkładając spodnie nasączone permetryną (spodnie) do poddanych obróbce skarpet, a poddaną obróbce koszulę z długimi rękawami do spodni, tak aby zminimalizować szczeliny, przez które kleszcz może dostać się do skóry użytkownika. Jasna odzież może ułatwić dostrzeżenie kleszczy i usunięcie ich, zanim ukąszą. Stwierdzono, że mundury wojskowe i pracowników zewnętrznych potraktowane permetryną zmniejszają liczbę przypadków ukąszeń o 80–95%. Ochrona permetryny wystarcza na kilka tygodni noszenia i prania w przypadku artykułów traktowanych przez klienta i do 70 prań w przypadku artykułów traktowanych fabrycznie. Permetryny nie należy stosować na ludzką skórę, bieliznę lub koty.
EPA zaleca kilka środków odstraszających kleszcze do stosowania na odsłoniętej skórze, w tym DEET , pikarydyna , IR3535 (pochodna aminokwasu beta-alaniny), olejek z eukaliptusa cytrynowego (OLE, związek naturalny) i aktywny składnik OLE, para-mentan-diol ( PMD) . W przeciwieństwie do permetryny, repelenty odstraszają, ale nie zabijają kleszczy, chronią tylko przez kilka godzin po aplikacji i mogą być zmyte przez pot lub wodę. Najpopularniejszym repelentem jest DEET w USA i pikarydyna w Europie. W przeciwieństwie do DEET, pikarydyna jest bezwonna i rzadziej podrażnia skórę lub uszkadza tkaniny lub tworzywa sztuczne. Repelenty o wyższym stężeniu mogą działać dłużej, ale nie są bardziej skuteczne; przeciwko kleszczom 20% pikarydyna może działać przez 8 godzin vs. 55–98,11% DEET przez 5–6 godzin lub 30–40% OLE przez 6 godzin. Repelentów nie należy stosować pod ubraniem, na oczy, usta, rany lub skaleczenia ani u niemowląt w wieku poniżej 2 miesięcy (3 lata w przypadku OLE lub PMD). Jeśli filtr przeciwsłoneczny jest używany, należy nałożyć na niego środek odstraszający. Repelentów nie należy rozpylać bezpośrednio na twarz, lecz rozpylać na dłoni, a następnie wcierać w twarz.
Po wejściu do domu ubrania, sprzęt i zwierzęta domowe należy sprawdzić pod kątem obecności kleszczy. Ubrania można włożyć do gorącej suszarki na 10 minut, aby zabić kleszcze (samo pranie lub ciepła suszarka nie wystarczą). Prysznic tak szybko, jak to możliwe, szukanie kleszczy na całym ciele i usuwanie ich zmniejszają ryzyko infekcji. Niekarmione nimfy kleszczy są wielkości ziarenka maku, ale dzień lub dwa po ukąszeniu i przyczepieniu się do osoby wyglądają jak mały pęcherz krwi . Szczególnie dokładnie należy sprawdzić okolice: pachy, między nogami, tył kolana, pępek, tułów, a u dzieci uszy, szyję i włosy.
Usuwanie kleszczy
Dołączone kleszcze należy niezwłocznie usunąć. Ryzyko infekcji wzrasta wraz z czasem przyczepu, ale w Ameryce Północnej ryzyko boreliozy jest niewielkie, jeśli kleszcz zostanie usunięty w ciągu 36 godzin. CDC zaleca wprowadzenie pęsety z cienką końcówką między skórę a kleszcza, bardzo mocne chwycenie i wyciągnięcie zamkniętej pęsety ze skóry bez skręcania, szarpania, ściskania lub miażdżenia kleszcza. Po usunięciu kleszcza należy w miarę możliwości usunąć pozostałe części kleszcza w skórze czystą pęsetą. Następnie ranę i ręce należy umyć alkoholem lub wodą z mydłem. Kleszcza można pozbyć się umieszczając go w pojemniku z alkoholem, szczelnie zamykaną torebką, taśmą lub spłukując w toalecie. Osoba ukąszona powinna zapisać, gdzie i kiedy doszło do ugryzienia, aby można było o tym poinformować lekarza, jeśli w ciągu następnych kilku tygodni wystąpi u niej wysypka lub objawy grypopodobne. CDC zaleca, aby nie używać palców, lakieru do paznokci, wazeliny ani ciepła na kleszczu, aby spróbować go usunąć.
W Australii, gdzie australijski kleszcz paraliżujący jest powszechny, Australasian Society of Clinical Immunology and Allergy odradza używanie pęsety do usuwania kleszczy, ponieważ jeśli osoba jest uczulona, może dojść do wstrząsu anafilaktycznego może wyniknąć. Zamiast tego produkt należy spryskać kleszcza, aby spowodować jego zamrożenie, a następnie odpaść. Lekarz użyłby ciekłego azotu, ale zamiast tego można użyć produktów dostępnych w aptece do zamrażania brodawek. Inna metoda pochodząca z Australii polega na użyciu ok. 20 cm nici dentystycznej lub żyłki wędkarskiej do powolnego zawiązania węzła między skórą a kleszczem, a następnie odciągnięcia go od skóry.
Profilaktyczne antybiotyki
Ryzyko przeniesienia zakażenia wzrasta wraz z długością przyczepiania się kleszcza. Wymaga od 36 do 48 godzin przylegania bakterii, które powodują, że borelioza przemieszcza się z wnętrza kleszcza do jego śliny. Jeśli kleszcz jelenia, który z wystarczającym prawdopodobieństwem jest nosicielem Borrelii zostanie znaleziony przyczepiony do osoby i usunięty, a jeśli kleszcz był przyczepiony przez 36 godzin lub jest obrzęknięty, pojedyncza dawka doksycykliny podana w ciągu 72 godzin po usunięciu może zmniejszyć ryzyko boreliozy. Ogólnie nie jest zalecane dla wszystkich osób pogryzionych, ponieważ rozwój infekcji jest rzadki: około 50 osób pogryzionych musiałoby być leczonych w ten sposób, aby zapobiec jednemu przypadkowi rumienia wędrującego (tj. typowej wysypki występującej u około 70–80% osób zakażonych) ).
Architektura krajobrazu
Kilka praktyk związanych z kształtowaniem krajobrazu może zmniejszyć ryzyko ukąszeń kleszczy na podwórkach mieszkalnych. Obejmują one koszenie trawników, usuwanie ściółki i chwastów oraz unikanie stosowania okrywy gruntowej. lasów , kamiennych ścian i krzewów zaleca się zastosowanie bariery z kamieni lub wiórów drzewnych o szerokości 3 stóp . Bez roślinności na barierze kleszcze raczej jej nie przekroczą; akarycydy można go również spryskać w celu zabicia kleszczy. Wystawiona na słońce strefa bezpieczna dla kleszczy, znajdująca się co najmniej 9 stóp od bariery, powinna koncentrować działalność człowieka na podwórku, w tym na wszelkich patio, placach zabaw i ogrodnictwie. Materiały takie jak drewniane deski tarasowe, beton, cegły, żwir lub zrębki drewniane stosowane na ziemi pod tarasami i placami zabaw zniechęciłyby tam kleszcze. Można dodać ogrodzenie o wysokości 8 stóp, aby trzymać jelenie z dala od strefy bezpiecznej dla kleszczy.
Narażenie zawodowe
Pracownicy na zewnątrz są narażeni na boreliozę, jeśli pracują w miejscach z zakażonymi kleszczami. Obejmuje to budownictwo, kształtowanie krajobrazu, leśnictwo, wycinanie krzaków, geodezję, rolnictwo, prace kolejowe, prace na polach naftowych, prace przy liniach użyteczności publicznej, zarządzanie parkami lub dziką przyrodą. Pracownicy amerykańscy w północno-wschodnich i północno-środkowych stanach są najbardziej narażeni na kontakt z zakażonymi kleszczami. Kleszcze mogą również przenosić inne choroby przenoszone przez kleszcze na pracowników w tych i innych regionach kraju. Miejsca pracy z lasami, krzewami, wysoką trawą lub ściółką mogą mieć więcej kleszczy. Pracownicy na zewnątrz powinni zachować szczególną ostrożność późną wiosną i latem, kiedy młode kleszcze są najbardziej aktywne.
Zwierzęta żywicielskie
Kleszcze mogą żywić się krwią wielu możliwych gatunków żywicieli, w tym jaszczurek , ptaków , myszy , kotów , psów , jeleni , bydła i ludzi . Zakres, w jakim kleszcz może się żerować, rozmnażać i rozprzestrzeniać, będzie zależał od rodzaju i dostępności jego żywicieli. To, czy będzie rozprzestrzeniać choroby, zależy również od dostępnych żywicieli. Niektóre gatunki, takie jak jaszczurki, są określane jako „żywiciele rozcieńczenia”, ponieważ nie mają tendencji do wspierania patogenów boreliozy, a tym samym zmniejszają prawdopodobieństwo przeniesienia choroby przez żerujące na nich kleszcze. Jeleń bielik jest zarówno źródłem pożywienia, jak i „żywicielem reprodukcyjnym”, w którym kleszcze mają tendencję do łączenia się w pary. Mysz białonoga jest żywicielem rezerwuarowym w których patogen boreliozy może przetrwać. Dostępność gospodarzy może mieć znaczący wpływ na przenoszenie boreliozy. Większa różnorodność żywicieli lub tych, którzy nie wspierają patogenu, zwykle zmniejsza prawdopodobieństwo przeniesienia choroby.
W Stanach Zjednoczonych jednym ze sposobów zmniejszenia częstości występowania boreliozy i innych chorób przenoszonych przez kleszcze jeleniowatych było znaczne zmniejszenie populacji jeleniowatych, od których uzależnione są dorosłe kleszcze w zakresie karmienia i rozmnażania. Liczba przypadków boreliozy spadła po wytępieniu jeleni na wyspie Monhegan w stanie Maine oraz po zwalczaniu jeleni w Mumford Cove w Connecticut. Zwolennicy sugerowali zmniejszenie populacji jeleni do poziomu 8 do 10 jeleni na milę kwadratową, w porównaniu do poziomu 60 lub więcej jeleni na milę kwadratową na obszarach kraju o najwyższych wskaźnikach boreliozy.
Inni zauważyli, że chociaż jelenie są żywicielami reprodukcyjnymi, nie są rezerwuarami Borrelia burgdorferi . Naukowcy zasugerowali, że mniejsze, mniej widoczne rezerwuary boreliozy, takie jak myszy białonogie i wiewiórki wschodnie , może silniej wpływać na występowanie boreliozy. Badania ekosystemów w stanie Nowy Jork sugerują, że myszy białonogie rozwijają się, gdy lasy są podzielone na mniejsze, odizolowane fragmenty lasu z mniejszą liczbą drapieżników gryzoni. Im więcej gryzoni jest nosicielami choroby, tym większe jest prawdopodobieństwo, że kleszcz pożywi się gryzoniem przenoszącym chorobę i że ktoś złapie kleszcza przenoszącego chorobę w swoim ogrodzie lub spacerując po lesie. Dane wskazują, że im mniejszy obszar zalesiony, tym więcej będzie na nim kleszczy i prawdopodobnie będą one nosicielami boreliozy, co potwierdza tezę, że wylesianie i fragmentacja siedlisk wpływają na kleszcze, żywicieli i przenoszenie chorób.
Szacuje się, że choroby przenoszone przez kleszcze dotykają około 80% bydła na całym świecie. Wpływają również na koty, psy i inne zwierzęta domowe. Rutynowa kontrola weterynaryjna kleszczy zwierząt domowych za pomocą akarycydów została zasugerowana jako sposób na zmniejszenie narażenia ludzi na kleszcze. Jednak zwalczanie chemiczne za pomocą akarycydów jest obecnie krytykowane z wielu powodów. Wydaje się, że kleszcze rozwijają odporność na akarycydy; akarycydy są kosztowne; istnieją również obawy co do ich toksyczności i potencjalnego wpływu pozostałości chemicznych na żywność i środowisko.
W Europie znanymi rezerwuarami Borrelia burgdorferi było 9 ssaków małych, 7 ssaków średnich i 16 gatunków ptaków (w tym wróblowatych, morskich i bażantów). Wydaje się, że zwierzęta te przenoszą krętki na kleszcze, a tym samym uczestniczą w naturalnym krążeniu B. burgdorferi w Europie. mysz domową , a także inne gatunki małych gryzoni, zwłaszcza w Europie Wschodniej i Rosji. „Gatunkami rezerwuarowymi zawierającymi najwięcej patogenów jest sarna europejska Capreolus capreolus ”; nie wydaje się, aby służyła jako główny rezerwuar B. burgdorferi " uważali Jaenson i wsp. (1992) (niekompetentny żywiciel dla B. burgdorferi i wirusa KZM), ale jest ważny dla karmienia kleszczy, takich jak jelenie i dziki ( Sus scrofa ), u których zidentyfikowano jeden gatunek Rickettsia i trzy gatunki Borrelia ", z wysokim ryzykiem koinfekcji u saren. Niemniej jednak w 2000 roku u saren w Europie „ zidentyfikowano dwa gatunki Rickettsia i dwa gatunki Borrelia ”.
Szczepionka
Obecnie nie są dostępne żadne szczepionki dla ludzi przeciwko chorobie z Lyme. Jedyną szczepionką dla ludzi, która trafiła na rynek, była LYMErix, która była dostępna od 1998 r., zanim została wycofana z rynku w 2002 r. Kandydat na szczepionkę VLA15 miał rozpocząć fazę 3 badań w trzecim kwartale 2022 r., a inne badania są w toku . Dostępnych jest wiele szczepionek do zapobiegania chorobie z Lyme u psów.
LYMERix
Szczepionka LYMErix była dostępna od 1998 do 2002 roku. Rekombinowana szczepionka przeciwko chorobie z Lyme, oparta na białku zewnętrznej powierzchni A (OspA) B. burgdorferi z wodorotlenkiem glinu jako adiuwantem, została opracowana przez SmithKline Beecham . W badaniach klinicznych z udziałem ponad 10 000 osób stwierdzono, że szczepionka nadaje ochronną odporność na boreliozę u 76% dorosłych po trzech dawkach z jedynie łagodnymi lub umiarkowanymi i przejściowymi działaniami niepożądanymi . W dniu 21 grudnia 1998 r. Agencja ds. Żywności i Leków (FDA) zatwierdziła LYMErix na podstawie tych badań dla osób w wieku od 15 do 70 lat.
Po zatwierdzeniu szczepionki jej wejście do praktyki klinicznej było powolne z różnych powodów, w tym z jej kosztu, który często nie był refundowany przez firmy ubezpieczeniowe. Następnie setki biorców szczepionek zgłosiło, że rozwinęły się u nich autoimmunologiczne i inne skutki uboczne. Wspierane przez niektóre grupy rzeczników, wniesiono szereg pozwów zbiorowych przeciwko firmie GlaxoSmithKline , twierdząc, że szczepionka spowodowała te problemy zdrowotne. Twierdzenia te zostały zbadane przez FDA i Centers for Disease Control, które nie znalazły związku między szczepionką a dolegliwościami autoimmunologicznymi.
Pomimo braku dowodów na to, że skargi były spowodowane przez szczepionkę, sprzedaż gwałtownie spadła, a LYMErix został wycofany z rynku amerykańskiego przez firmę GlaxoSmithKline w lutym 2002 r., w związku z negatywnymi relacjami w mediach i obawami przed skutkami ubocznymi szczepionek. Los LYMErix został opisany w literaturze medycznej jako „przestroga”; artykuł redakcyjny w Nature przytoczył wycofanie LYMErix jako przykład, w którym „nieuzasadnione obawy opinii publicznej wywierają presję na twórców szczepionek, wykraczającą poza rozsądne względy bezpieczeństwa”. Powiedział pierwotny twórca szczepionki OspA w Instytucie Maxa Plancka Natura : „To tylko pokazuje, jak irracjonalny może być świat… Nie było naukowego uzasadnienia dla wycofania pierwszej szczepionki OspA LYMErix”.
VLA15
Sześciowartościowy (OspA) kandydat na szczepionkę opartą na podjednostce białka VLA15 został opracowany przez firmę Valneva . W lipcu 2017 r. Amerykańska Agencja ds. Żywności i Leków przyznała jej oznaczenie szybkiej ścieżki . W kwietniu 2020 r . Pfizer zapłacił 130 mln USD za prawa do szczepionki, a firmy wspólnie ją opracowują, przeprowadzając wiele badań fazy 2.
Próba VLA15 fazy 3 została zaplanowana na koniec 2022 r., rekrutacja ochotników w ośrodkach testowych zlokalizowanych w północno-wschodnich Stanach Zjednoczonych i Europie. Uczestnicy mieli otrzymać początkową serię trzech dawek szczepionek w ciągu pięciu do dziewięciu miesięcy, a następnie dawkę przypominającą po dwunastu miesiącach, przy czym zarówno początkowa seria, jak i dawka przypominająca miały zostać zakończone przed szczytem boreliozy w roku pora roku.
Inne badania
Szczepionka mRNA zaprojektowana w celu wywołania silnej, szybkiej odpowiedzi immunologicznej na ślinę kleszcza umożliwiła układowi odpornościowemu wykrycie i usunięcie kleszczy ze zwierząt testowych, zanim były one w stanie przenosić zakaźne bakterie. Szczepionka zawiera mRNA potrzebne organizmowi do budowy 19 białek w ślinie kleszczy, które poprzez umożliwienie szybkiego powstania rumienia (swędzącego zaczerwienienia) w miejscu ukąszenia chronią świnki morskie przed boreliozą. Chroniło to również zwierzęta testowe, jeśli kleszcz nie został usunięty, jeśli tylko jeden kleszcz, a nie trzy, pozostaje przyczepiony.
Szczepionki dla psów
Szczepionki dla psów zostały opracowane i zatwierdzone do zapobiegania chorobie z Lyme u psów. Obecnie dostępne są trzy szczepionki przeciwko boreliozie. LymeVax, opracowany przez Fort Dodge Laboratories, zawiera nienaruszone martwe krętki, które narażają żywiciela na działanie organizmu. szczepionka firmy Intervet- Schering-Plough , celuje w białka OspC i OspA . Przeciwciała OspC zabijają wszystkie bakterie, które nie zostały zabite przez przeciwciała OspA. Canine Recombinant Lyme, opracowany przez Merial , wytwarza przeciwciała przeciwko białku OspA, więc kleszcz żerujący na zaszczepionym psie wciąga krew pełną przeciwciał anty-OspA, które zabijają krętki w jelicie kleszcza, zanim zostaną one przeniesione na psa.
Leczenie
Podstawowym leczeniem są antybiotyki . Konkretne podejście do ich stosowania jest uzależnione od osoby dotkniętej chorobą i stopnia zaawansowania choroby. W przypadku większości osób z wczesną miejscową infekcją powszechnie zaleca się doustne podanie doksycykliny jako pierwszego wyboru, ponieważ jest ona skuteczna nie tylko przeciwko bakteriom Borrelia , ale także wielu innym chorobom przenoszonym przez kleszcze. Osoby przyjmujące doksycyklinę powinny unikać ekspozycji na słońce ze względu na zwiększone ryzyko oparzeń słonecznych . Doksycyklina jest przeciwwskazana u dzieci poniżej ósmego roku życia oraz kobiet w ciąży lub karmiących piersią; alternatywami dla doksycykliny są amoksycylina , aksetyl cefuroksymu i azytromycyna . Azytromycyna jest zalecana tylko w przypadku nietolerancji innych antybiotyków. Standardowe leczenie zapalenia tkanki łącznej , cefaleksyna , nie jest przydatne w przypadku boreliozy. Jeśli nie jest jasne, czy wysypka jest spowodowana boreliozą czy zapaleniem tkanki łącznej, IDSA zaleca leczenie cefuroksymem lub amoksycyliną/kwasem klawulanowym , ponieważ są one skuteczne przeciwko obu infekcjom. Osoby z wczesną rozsianą lub późną infekcją z Lyme mogą mieć objawową chorobę serca, zapalenie stawów z Lyme lub objawy neurologiczne, takie jak porażenie twarzy , radikulopatia , zapalenie opon mózgowych lub neuropatia obwodowa . W takich przypadkach zaleca się dożylne podanie ceftriaksonu jako pierwszego wyboru; jako alternatywy dostępne są cefotaksym i doksycyklina.
Schematy leczenia boreliozy wahają się od 14 dni we wczesnej zlokalizowanej chorobie, przez 14-21 dni we wczesnej chorobie rozsianej do 14-28 dni w późnej chorobie rozsianej. Neurologiczne powikłania boreliozy można leczyć doksycykliną , ponieważ można ją przyjmować doustnie i ma niższy koszt, chociaż w Ameryce Północnej dowody na skuteczność są tylko pośrednie. W przypadku niepowodzenia wytyczne zalecają ponowne podanie ceftriaksonu we wstrzyknięciach . Kilka miesięcy po leczeniu zapalenia stawów z Lyme, jeśli obrzęk stawów utrzymuje się lub powraca, można rozważyć drugą serię antybiotyków; antybiotyki dożylne są preferowane w przypadku ponownego leczenia w przypadku słabej odpowiedzi na antybiotyki doustne. Poza tym nie zaleca się przedłużonego schematu antybiotykoterapii trwającego dłużej niż 28 dni, ponieważ żadne dowody nie wskazują na jego skuteczność. Poziomy przeciwciał IgM i IgG mogą być podwyższone przez lata, nawet po skutecznym leczeniu antybiotykami. Ponieważ poziomy przeciwciał nie wskazują na powodzenie leczenia, nie zaleca się ich oznaczania.
Porażenie twarzy może ustąpić bez leczenia; jednak zaleca się leczenie antybiotykami, aby zatrzymać inne powikłania z Lyme. Kortykosteroidy nie są zalecane, gdy porażenie nerwu twarzowego jest spowodowane boreliozą. U osób z porażeniem twarzy zaleca się częste stosowanie sztucznych łez podczas czuwania, wraz z maścią i plastrem lub zaklejaniem oka podczas snu.
Około jedna trzecia osób z zapaleniem serca z Lyme potrzebuje tymczasowego rozrusznika serca do czasu ustąpienia nieprawidłowości przewodzenia serca, a 21% wymaga hospitalizacji. Zapalenia serca z Lyme nie należy leczyć kortykosteroidami.
Osoby z boreliozą powinny ograniczyć aktywność fizyczną, aby nie uszkodzić dotkniętych stawów, aw przypadku utykania powinny korzystać z kul. Ból związany z boreliozą można leczyć niesteroidowymi lekami przeciwzapalnymi (NLPZ). Zastrzyki z kortykosteroidów do stawów nie są zalecane w leczeniu zapalenia stawów z Lyme, które jest leczone antybiotykami. Osoby z zapaleniem stawów z Lyme leczone antybiotykami dożylnymi lub przez dwa miesiące antybiotykami doustnymi, u których obrzęk stawów utrzymuje się po dwóch miesiącach od leczenia i mają ujemny wynik testu PCR na obecność DNA Borrelii w płynie maziowym mają poantybiotykowe zapalenie stawów z Lyme; jest to bardziej powszechne po zakażeniu niektórymi szczepami Borrelia u osób z pewnymi cechami genetycznymi i immunologicznymi. Postantybiotykowe zapalenie stawów z Lyme można leczyć objawowo za pomocą NLPZ, leków przeciwreumatycznych modyfikujących przebieg choroby (DMARD), artroskopowej synowektomii lub fizykoterapii.
Osoby leczone powinny być poinformowane o możliwości reinfekcji i sposobach jej zapobiegania .
Rokowanie
Typowy pierwszy objaw boreliozy, rumień wędrujący (EM), ustępuje w ciągu kilku tygodni, nawet bez leczenia. Jednak u osób nieleczonych infekcja często rozprzestrzenia się do układu nerwowego, serca lub stawów, prawdopodobnie powodując trwałe uszkodzenie tkanek ciała.
Najlepsze perspektywy mają osoby, które otrzymają zaleconą antybiotykoterapię w ciągu kilku dni od pojawienia się początkowej wysypki EM. Powrót do zdrowia może nie być całkowity lub natychmiastowy. Odsetek osób osiągających pełne wyzdrowienie w Stanach Zjednoczonych wzrasta z około 64–71% pod koniec leczenia wysypki EM do około 84–90% po 30 miesiącach; wyższe wartości procentowe odnotowano w Europie. Niepowodzenie leczenia, czyli utrzymywanie się pierwotnych lub pojawienie się nowych objawów choroby, występuje tylko u nielicznych osób. Pozostałe osoby są uważane za wyleczone, ale nadal odczuwają subiektywne objawy, np. bóle stawów lub mięśni czy zmęczenie . Objawy te są zwykle łagodne i nie powodują niesprawności.
Osoby leczone dopiero po objawach ze strony układu nerwowego, oprócz objawów subiektywnych, mogą skończyć się obiektywnymi deficytami neurologicznymi. W Europie średnio po 32–33 miesiącach od wystąpienia pierwszych objawów boreliozy u osób leczonych głównie doksycykliną 200 mg przez 14–21 dni odsetek osób z utrzymującymi się objawami był znacznie wyższy wśród osób z rozpoznaniem neuroboreliozy (50%) niż wśród osób tylko z wysypką EM (16%). W innym badaniu europejskim, 5 lat po leczeniu neuroboreliozy, utrzymujące się objawy występowały rzadziej u dzieci (15%) niż u dorosłych (30%), a w tym drugim przypadku były one mniej powszechne u osób leczonych w ciągu 30 dni od wystąpienia pierwszego objawu (16% ) niż wśród leczonych później (39%); wśród osób z utrzymującymi się objawami 54% miało ograniczone codzienne czynności, a 19% przebywało na zwolnieniu lekarskim lub było niezdolnych do pracy.
Niektóre dane sugerują, że około 90% porażenia nerwu twarzowego z Lyme leczonego antybiotykami w pełni wraca do zdrowia średnio po 24 dniach od pojawienia się, a większość pozostałych wraca do zdrowia z jedynie łagodną nieprawidłowością. Jednak w Europie 41% osób leczonych z powodu porażenia nerwu twarzowego miało inne utrzymujące się objawy podczas wizyty kontrolnej do 6 miesięcy później, w tym 28% drętwienie lub zaburzenia czucia , a 14% zmęczenie lub koncentrację problemy. Porażenia po obu stronach twarzy wiążą się z gorszym i dłuższym czasem powrotu do zdrowia. Dane historyczne sugerują, że nieleczone osoby z porażeniem twarzy wracają do zdrowia w prawie takim samym tempie, ale 88% później cierpi na zapalenie stawów z Lyme. Inne badania pokazują, że synkineza (mimowolny ruch mięśnia twarzy, gdy inny jest dobrowolnie poruszany) może stać się widoczna dopiero po 6–12 miesiącach od ustąpienia porażenia nerwu twarzowego, ponieważ uszkodzone nerwy odrastają i czasami łączą się z nieprawidłowymi mięśniami. Synkineza jest związana ze kortykosteroidów . W dłuższej obserwacji 16–23% porażenia twarzy z Lyme nie wraca do pełnej sprawności.
W Europie około jedna czwarta osób z zespołem Bannwartha ( radikulopatia z Lyme i limfocytarne zapalenie opon mózgowo-rdzeniowych ) leczonych dożylnie ceftriaksonem przez 14 dni, średnio 30 dni po wystąpieniu pierwszych objawów, musiała zostać ponownie poddana leczeniu 3–6 miesięcy później z powodu niezadowalającej odpowiedzi klinicznej lub utrzymującego się celu markery infekcji w płynie mózgowo-rdzeniowym ; po 12 miesiącach 64% całkowicie wyzdrowiało, 31% miało łagodne lub rzadkie objawy nie powodujące niepełnosprawności, które nie wymagały regularnego stosowania środków przeciwbólowych, a 5% miało objawy, które powodowały niepełnosprawność lub wymagały znacznego stosowania środków przeciwbólowych. Najczęstszymi utrzymującymi się objawami niepowodującymi niesprawności były: ból głowy, zmęczenie , zaburzenia czucia , bóle stawów , zaburzenia pamięci , złe samopoczucie , ból korzeni , zaburzenia snu , bóle mięśni i koncentracja zakłócenia. Utrzymujące się objawy powodujące niepełnosprawność obejmowały porażenie nerwu twarzowego i inne zaburzenia ruchowe .
Wyzdrowienie z późnej neuroboreliozy zwykle trwa dłużej i jest mniej kompletne niż z wczesnej neuroboreliozy, prawdopodobnie z powodu nieodwracalnych uszkodzeń neurologicznych.
Około połowa osób z zapaleniem serca z Lyme przechodzi do całkowitego bloku serca , ale zwykle ustępuje on w ciągu tygodnia. Inne nieprawidłowości przewodzenia w sercu z Lyme ustępują zwykle w ciągu 6 tygodni. Około 94% osób w pełni wyzdrowiało, ale 5% potrzebuje stałego rozrusznika serca, a 1% kończy się uporczywym blokiem serca (rzeczywisty odsetek może być wyższy z powodu nierozpoznanych przypadków). Powikłania mięśnia sercowego z Lyme są zwykle łagodne i samoograniczające się. Jednak w niektórych przypadkach zapalenie serca z Lyme może być śmiertelne.
Zalecane leczenie antybiotykami jest skuteczne w około 90% przypadków zapalenia stawów z Lyme, chociaż ustąpienie stanu zapalnego może zająć kilka miesięcy i często konieczna jest druga runda antybiotyków. Oporne na antybiotyki zapalenie stawów z Lyme również ostatecznie ustępuje, zwykle w ciągu 9–14 miesięcy (zakres 4 miesiące – 4 lata); DMARDs lub synowektomia mogą przyspieszyć powrót do zdrowia.
Ponowna infekcja nie jest rzadkością. W amerykańskim badaniu 6–11% osób leczonych z powodu wysypki EM miało kolejną wysypkę EM w ciągu 30 miesięcy. Druga wysypka jest zwykle spowodowana zakażeniem innym Borrelia .
Mówi się, że osoby, które mają niespecyficzne, subiektywne objawy, takie jak zmęczenie, bóle stawów i mięśni lub trudności poznawcze przez ponad sześć miesięcy po zalecanym leczeniu boreliozy, mają zespół boreliozy po leczeniu (PTLDS). Od 2016 roku przyczyna utrzymujących się objawów nie była znana; stan ten jest ogólnie zarządzany podobnie jak fibromialgia lub zespół chronicznego zmęczenia .
Epidemiologia
Borelioza występuje regularnie w umiarkowanych regionach półkuli północnej . Szacuje się, że rocznie w Stanach Zjednoczonych diagnozuje się i leczy tę chorobę u 476 000 osób. Liczba ta jest prawdopodobnie zawyżona z powodu nadmiernej diagnozy i nadmiernego leczenia. W Europie diagnozuje się i leczy ponad 200 000 osób rocznie. Istnieje sugestia, że populacje kleszczy i występowanie boreliozy wzrastają i rozprzestrzeniają się na nowe obszary, częściowo z powodu ocieplenia temperatur spowodowanego zmianami klimatycznymi . Jednak systemy chorób przenoszonych przez kleszcze są złożone, a ustalenie, czy zmiany są spowodowane zmianami klimatycznymi, czy też innymi czynnikami, może być trudne.
Afryka
W północnej Afryce B. burgdorferi sensu lato została zidentyfikowana w Maroku , Algierii , Egipcie i Tunezji .
Choroba z Lyme w Afryce Subsaharyjskiej jest obecnie nieznana, ale dowody wskazują, że może wystąpić u ludzi w tym regionie. Obfitość żywicieli i wektorów kleszczy sprzyjałaby zakażeniu boreliozą w Afryce. Kenii odnotowano dwa przypadki boreliozy .
Azja
B. burgdorferi sensu lato są częściej spotykane w Japonii, a także w północno-zachodnich Chinach, Nepalu , Tajlandii i dalekowschodniej Rosji. Borrelia została również wyizolowana w Mongolii .
Europa
W Europie boreliozę wywołuje infekcja jednym lub więcej patogennymi europejskimi genogatunkami krętka B. burgdorferi sensu lato , przenoszonymi głównie przez kleszcza Ixodes ricinus . Przypadki B. burgdorferi sensu lato występują głównie w Europie Środkowej, zwłaszcza w Słowenii i Austrii, ale zostały odizolowane w prawie każdym kraju na kontynencie. Liczba zachorowań na południu Europy, takich jak Włochy i Portugalia, jest znacznie niższa. Liczba zdiagnozowanych przypadków w niektórych krajach zachodnich, takich jak Islandia, rośnie. Borelioza jest rzadkością na Islandii. Każdego roku diagnozuje się średnio około 6 do 7 przypadków, głównie miejscowych infekcji objawiających się rumieniem wędrującym. Żadna ze spraw nie miała definitywnego pochodzenia islandzkiego, a roczna liczba spraw nie wzrasta.
Zjednoczone Królestwo
W Wielkiej Brytanii liczba potwierdzonych laboratoryjnie przypadków boreliozy stale rośnie od czasu wprowadzenia dobrowolnego zgłaszania w 1986 r., kiedy to w Wielkiej Brytanii i Irlandii zarejestrowano łącznie 68 przypadków. W Wielkiej Brytanii odnotowano 23 potwierdzone przypadki w 1988 r. i 19 w 1990 r., ale 973 w 2009 r. i 953 w 2010 r. Wstępne dane za pierwsze 3 kwartały 2011 r. wskazują na 26% wzrost w porównaniu z tym samym okresem w 2010 r.
Uważa się jednak, że rzeczywista liczba przypadków jest znacznie wyższa niż sugerowały powyższe dane, a brytyjska Agencja Ochrony Zdrowia szacuje, że występuje od 2000 do 3000 przypadków rocznie (przy średniej około 15% zakażenia nabyte za granicą), natomiast dr Darrel Ho-Yen, dyrektor Scottish Toxoplasma Reference Laboratory and National Lyme Disease Testing Service uważa, że liczbę potwierdzonych przypadków należy pomnożyć przez 10 „aby uwzględnić błędnie zdiagnozowane przypadki, testy dające fałszywe wyniki, osoby cierpiące, które nie zostały przetestowane, osoby zarażone, ale nie wykazujące objawów, brak powiadomienia i osoby zarażone, które nie skonsultowały się z lekarzem”.
Pomimo tego, że borelioza (zakażenie Borrelia burgdorferi) jest chorobą podlegającą obowiązkowi zgłoszenia w Szkocji od stycznia 1990 r. i dlatego należy ją zgłaszać na podstawie podejrzenia klinicznego, uważa się, że wielu lekarzy pierwszego kontaktu nie jest świadomych tego wymogu. Obowiązkowe raportowanie, ograniczone tylko do wyników badań laboratoryjnych, zostało wprowadzone w całej Wielkiej Brytanii w październiku 2010 r. na mocy przepisów dotyczących ochrony zdrowia (powiadomień) z 2010 r.
Chociaż istnieje większa liczba przypadków boreliozy w New Forest , Salisbury Plain , Exmoor , South Downs , częściach Wiltshire i Berkshire , Thetford Forest i zachodnim wybrzeżu oraz na wyspach Szkocji, zarażone kleszcze są szeroko rozpowszechnione i mogą nawet można znaleźć w parkach Londynu. Raport z 1989 roku wykazał, że 25% pracowników leśnych w New Forest było seropozytywnych , podobnie jak od 2% do 4–5% ogólnej populacji lokalnej na tym obszarze.
Testy przeprowadzone na psach domowych w całym kraju w 2009 roku wykazały, że około 2,5% kleszczy w Wielkiej Brytanii może być zakażonych, znacznie więcej niż wcześniej sądzono. Spekuluje się, że globalne ocieplenie może w przyszłości doprowadzić do wzrostu aktywności kleszczy, a także wydłużenia czasu spędzanego przez ludzi w parkach publicznych, zwiększając tym samym ryzyko infekcji. Jednak żadne opublikowane badania tego nie potwierdziły.
Ameryka północna
Wiele badań w Ameryce Północnej dotyczyło ekologicznych i środowiskowych korelatów liczby osób dotkniętych boreliozą. Badanie przeprowadzone w 2005 r. Przy użyciu modelowania I. scapularis przydatności klimatu przewidywało, że zmiana klimatu spowoduje ogólny wzrost liczby odpowiednich siedlisk-wektorów o 213% do 2080 r. wraz z ekspansją w kierunku północnym w Kanadzie, zwiększoną przydatnością w środkowych Stanach Zjednoczonych i zmniejszoną retrakcją odpowiednich siedlisk i wektorów w południowych Stanach Zjednoczonych Przegląd opublikowanych badań z 2008 r. wykazał, że obecność lasów lub obszary były jedyną zmienną, która konsekwentnie zwiększała ryzyko boreliozy, podczas gdy inne zmienne środowiskowe wykazywały niewielką lub żadną zgodność między badaniami. Autorzy argumentowali, że czynniki wpływające na zagęszczenie kleszczy i ryzyko dla ludzi między miejscami są nadal słabo poznane i że przyszłe badania powinny być prowadzone w dłuższych okresach czasu, bardziej ujednolicone w różnych regionach i uwzględniać istniejącą wiedzę na temat regionalnej boreliozy ekologia choroby .
Kanada
Zakres kleszczy zdolnych do przenoszenia boreliozy rozszerzył się z ograniczonego obszaru Ontario na obszary południowego Quebecu, Manitoby, północnego Ontario, południowego Nowego Brunszwiku, południowo-zachodniej Nowej Szkocji i ograniczonych części Saskatchewan i Alberty, a także Kolumbii Brytyjskiej. Przypadki zostały zgłoszone tak daleko na wschód, jak wyspa Nowa Fundlandia. Oparta na modelu prognoza Leightona i in. (2012) sugerują, że zasięg kleszcza I. scapularis rozszerzy się na Kanadę o 46 km/rok w ciągu następnej dekady, a ocieplenie klimatu będzie głównym czynnikiem napędzającym szybsze rozprzestrzenianie się.
Meksyk
Badanie z 2007 roku sugeruje, że infekcje Borrelia burgdorferi są endemiczne w Meksyku, na podstawie czterech przypadków zgłoszonych w latach 1999-2000.
Stany Zjednoczone
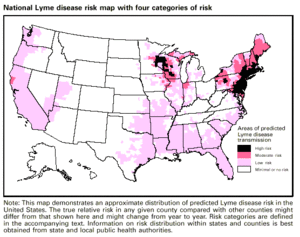
Borelioza jest najczęstszą chorobą przenoszoną przez kleszcze w Ameryce Północnej i Europie oraz jedną z najszybciej rozwijających się chorób zakaźnych w Stanach Zjednoczonych. Spośród przypadków zgłoszonych do CDC w Stanach Zjednoczonych, wskaźnik zakażenia boreliozą wynosi 7,9 przypadków na każde 100 000 osób. W dziesięciu stanach, w których borelioza występuje najczęściej, średnia wynosiła 31,6 przypadków na każde 100 000 osób w 2005 roku.
Chociaż boreliozę zgłaszano we wszystkich stanach z powodu infekcji związanych z podróżowaniem, około 99% wszystkich zgłoszonych przypadków ogranicza się do zaledwie pięciu obszarów geograficznych (Nowa Anglia, środkowoatlantycki, wschodnio-północno-środkowy, południowy Atlantyk i zachodnio-północno-zachodni Centralny). CDC wdrożyło krajowy nadzór przypadków boreliozy w 1991 roku. Od tego czasu kryteria zgłaszania były wielokrotnie modyfikowane. Definicja przypadku nadzoru z 2022 r. klasyfikuje przypadki jako potwierdzone, prawdopodobne i podejrzane.
CDC podkreśla, że chociaż dane z nadzoru mają ograniczenia, są przydatne ze względu na „jednolitość, prostotę i aktualność”. Podczas gdy liczba przypadków jest niedostatecznie zgłaszana na obszarach o wysokiej zachorowalności, prawdopodobne jest zawyżanie liczby zgłoszeń na obszarach o niskiej zachorowalności. Ponadto przypadki nadzoru są zgłaszane według hrabstwa zamieszkania, a nie miejsca, w którym doszło do zakażenia.
Liczba zgłoszonych przypadków choroby rośnie, podobnie jak regiony endemiczne w Ameryce Północnej. Na przykład wcześniej uważano, że B. burgdorferi sensu lato ma trudności z utrzymaniem się w cyklu enzootycznym w Kalifornii, ponieważ zakładano, że duża populacja jaszczurek osłabi liczbę osób dotkniętych przez B. burgdorferi w lokalnych populacjach kleszczy ; od tego czasu zostało to zakwestionowane, ponieważ niektóre dowody sugerują, że jaszczurki mogą się zarazić.
Z wyjątkiem jednego badania w Europie, wiele danych dotyczących jaszczurek opiera się na wykrywaniu DNA krętka i nie wykazało, że jaszczurki są w stanie zarażać żywiące się nimi kleszcze. Ponieważ niektóre eksperymenty sugerują, że jaszczurki są oporne na zakażenie Borrelią , wydaje się prawdopodobne, że ich udział w cyklu enzootycznym jest bardziej złożony i specyficzny dla gatunku.
Podczas gdy B. burgdorferi jest najczęściej kojarzona z kleszczami, których żywicielami są jelenie bieliki i myszy białonogie , Borrelia afzelii jest najczęściej wykrywana u kleszczy-wektorów żywiących się gryzoniami, a Borrelia garinii i Borrelia valaisiana wydają się być związane z ptakami. Zarówno gryzonie, jak i ptaki są kompetentnymi żywicielami rezerwuarowymi dla B. burgdorferi sensu stricto . Odporność genogatunków krętków boreliozy na działanie bakteriolityczne alternatywnego szlaku dopełniacza różnych gatunków żywicieli może determinować ich asocjację rezerwuarową. [ potrzebne źródło ]
Może istnieć kilka podobnych, ale najwyraźniej różnych warunków, spowodowanych przez różne gatunki lub podgatunki Borrelii w Ameryce Północnej. Ograniczonym regionalnie schorzeniem, które może być związane z Borrelią , jest południowa choroba wysypkowa związana z kleszczami (STARI), znana również jako choroba Mastersa. Amblyomma americanum , znany powszechnie jako kleszcz samotnej gwiazdy, jest uznawany za głównego wektora STARI. W niektórych częściach geograficznego rozmieszczenia STARI borelioza jest dość rzadka (np. Arkansas), więc ludzie w tych regionach doświadczający objawów podobnych do boreliozy – zwłaszcza jeśli są po ukąszeniu przez samotnego kleszcza – powinni rozważyć STARI jako możliwość. Jest to na ogół łagodniejszy stan niż borelioza i zwykle dobrze reaguje na leczenie antybiotykami.
W ostatnich latach w Montanie odnotowuje się od 5 do 10 przypadków choroby podobnej do boreliozy rocznie. Występuje głównie w kieszeniach wzdłuż rzeki Yellowstone w środkowej Montanie. Ludzie rozwinęli czerwoną wysypkę wokół ukąszenia kleszcza, po której następują tygodnie zmęczenia i gorączka.
Skutki boreliozy są porównywalne u mężczyzn i kobiet. Dotyczy to wielu grup wiekowych, chociaż liczba przypadków jest najwyższa wśród osób w wieku od 10 do 19 lat. Z nieznanych przyczyn borelioza występuje siedmiokrotnie częściej wśród Azjatów.
Ameryka Południowa
W Ameryce Południowej rozpoznawanie i występowanie chorób przenoszonych przez kleszcze rośnie. W Brazylii zidentyfikowano chorobę podobną do boreliozy, znaną jako zespół Baggio-Yoshinari , wywoływaną przez mikroorganizmy, które nie należą do kompleksu B. burgdorferi sensu lato i przenoszoną przez kleszcze z rodzajów Amblyomma i Rhipicephalus . Pierwszy zgłoszony przypadek BYS w Brazylii odnotowano w 1992 roku w Cotia w São Paulo.
Historia
Ewolucyjna historia genetyki Borrelia burgdorferi była przedmiotem ostatnich badań. Jedno z badań wykazało, że przed ponownym zalesianiem , które towarzyszyło porzucaniu farm postkolonialnych w Nowej Anglii i hurtową migracją na środkowy zachód , która miała miejsce na początku XIX wieku, borelioza była obecna w Ameryce przez tysiące lat i rozprzestrzeniła się wzdłuż z żywicielami kleszczy od północnego wschodu do środkowego zachodu.
John Josselyn, który odwiedził Nową Anglię w 1638 i ponownie w latach 1663-1670, napisał: „W lecie na krzakach wisi nieskończona liczba kleszczy, które przyczepiają się do szat człowieka i wpełzają do jego spodni, wgryzając się w krótkim czasie w bardzo ludzkie ciało. Widziałem pończochy tych, którzy przeszli przez lasy nimi pokryte”.
Potwierdzają to również pisma Petera Kalma , szwedzkiego botanika, który został wysłany do Ameryki przez Linneusza i który podczas swojej wizyty w 1749 roku stwierdził, że lasy Nowego Jorku „obfitują” w kleszcze. Kiedy podróż Kalma została odtworzona 100 lat później, lasy zniknęły, a borelioza prawdopodobnie wyizolowała się z kilku obszarów wzdłuż północno-wschodniego wybrzeża, Wisconsin i Minnesoty.
Być może pierwszy szczegółowy opis tego, co jest obecnie znane jako borelioza, pojawił się w pismach Johna Walkera po wizycie na wyspie Jura (Deer Island) u zachodniego wybrzeża Szkocji w 1764 r. Daje on dobry opis obu objawów boreliozy (z „doskonałym bólem [w] wewnętrznych częściach kończyn”) i samego kleszcza-wektora, którego opisuje jako „robaka” z ciałem „czerwonego koloru i ściśniętego kształtu z rząd stóp z każdej strony”, który „penetruje skórę”. Wiele osób z tego obszaru Wielkiej Brytanii wyemigrowało do Ameryki Północnej między 1717 a końcem XVIII wieku. [ potrzebne źródło ]
Badanie zachowanych okazów muzealnych wykazało obecność DNA Borrelii w zainfekowanym kleszczu Ixodes ricinus z Niemiec, którego historia sięga 1884 r., oraz zakażonej myszy z Cape Cod, która zmarła w 1894 r . starej mumii , ujawnił obecność sekwencji DNA Borrelia burgdorferi, czyniąc go najwcześniejszym znanym człowiekiem z boreliozą.
Wczesne europejskie badania tego, co jest obecnie znane jako borelioza, opisywały jej objawy skórne. Pierwsze badanie pochodzi z 1883 roku we Wrocławiu , w Niemczech (obecnie Wrocław , Polska), gdzie lekarz Alfred Buchwald opisał mężczyznę, który od 16 lat cierpiał na zwyrodnieniową chorobę skóry , znaną obecnie jako acrodermatitis chronica atrophicans .
Na konferencji naukowej w 1909 r. szwedzki dermatolog Arvid Afzelius przedstawił badanie dotyczące rozszerzającej się, podobnej do pierścienia zmiany, którą zaobserwował u starszej kobiety po ukąszeniu kleszcza przez owcę. Nazwał zmianę rumieniem wędrującym . Choroba skóry znana obecnie jako chłoniak borelialny została po raz pierwszy opisana w 1911 roku.
Współczesna historia medycznego zrozumienia choroby, w tym jej przyczyny, diagnozy i leczenia, była trudna.
Problemy neurologiczne po ukąszeniach kleszczy rozpoznawano od lat dwudziestych XX wieku. Francuscy lekarze Garin i Bujadoux opisali rolnika z bolesnym zapaleniem korzonków czuciowych , któremu towarzyszyło łagodne zapalenie opon mózgowych po ukąszeniu przez kleszcza. Odnotowano również dużą wysypkę w kształcie pierścienia, chociaż lekarze nie wiązali jej z zapaleniem opon mózgowo-rdzeniowych. W 1930 roku szwedzki dermatolog Sven Hellerström jako pierwszy zaproponował EM i objawy neurologiczne po ukąszeniu kleszcza były ze sobą powiązane. W latach czterdziestych XX wieku niemiecki neurolog Alfred Bannwarth opisali kilka przypadków przewlekłego limfocytowego zapalenia opon mózgowo-rdzeniowych i zapalenia wielokorzeniowego, z których niektórym towarzyszyły rumieniowe zmiany skórne.
Carl Lennhoff, który pracował w Instytucie Karolinska w Szwecji, uważał, że wiele chorób skóry jest spowodowanych przez krętki. W 1948 roku użył specjalnego barwnika do mikroskopowej obserwacji czegoś, co uważał za krętki w różnych typach zmian skórnych, w tym EM. Chociaż później okazało się, że jego wnioski były błędne, wzbudzono zainteresowanie badaniem krętków. W 1949 r. Nils Thyresson, który również pracował w Instytucie Karolinska, jako pierwszy leczył ACA penicyliną. W latach pięćdziesiątych XX wieku w całej Europie uznano związek między ukąszeniem kleszcza, chłoniakiem, EM i zespołem Bannwartha, co doprowadziło do powszechnego stosowania penicyliny do leczenia w Europie.
W 1970 r. Rudolph Scrimenti, dermatolog z Wisconsin , rozpoznał uszkodzenie EM u osoby po przypomnieniu sobie artykułu Hellerströma, który został przedrukowany w amerykańskim czasopiśmie naukowym w 1950 r. Był to pierwszy udokumentowany przypadek EM w Stanach Zjednoczonych. Opierając się na literaturze europejskiej, leczył osobę penicyliną.
Pełny zespół znany obecnie jako borelioza nie został rozpoznany, dopóki grupa przypadków pierwotnie uważanych za młodzieńcze reumatoidalne zapalenie stawów nie została zidentyfikowana w trzech miastach w południowo-wschodnim Connecticut w 1975 r., W tym w miastach Lyme i Old Lyme , które nadały chorobie popularną nazwę. Zostało to zbadane przez lekarzy Davida Snydmana i Allena Steere z Epidemic Intelligence Service oraz przez innych z Uniwersytetu Yale , w tym Stephena Malawistę , który jest uznawany za współodkrywcę choroby. Uznanie, że ludzie w Stanach Zjednoczonych cierpią na EM, doprowadziło do uznania, że „Boreliozowe zapalenie stawów” jest jednym z przejawów tej samej choroby przenoszonej przez kleszcze, znanej w Europie.
Przed 1976 r. elementy zakażenia B. burgdorferi sensu lato były nazywane lub znane jako kleszczowe zapalenie opon mózgowo-rdzeniowych, zespół Garina-Bujadoux, zespół Bannwartha, choroba Afzeliusa, kolano Montauk lub gorączka kleszczowa owiec. Od 1976 roku choroba ta jest najczęściej określana jako borelioza, borelioza z Lyme lub po prostu borelioza.
W 1980 Steere i in. , zaczął testować schematy antybiotyków u dorosłych z boreliozą. W tym samym roku epidemiolog z Departamentu Zdrowia stanu Nowy Jork, Jorge Benach , dostarczył Willy'emu Burgdorferowi , badaczowi z Rocky Mountain Biological Laboratory , kolekcję I. dammini [ scapularis ] z Shelter Island w stanie Nowy Jork, znanego obszaru endemicznego występowania boreliozy w ramach trwającego dochodzenia w sprawie gorączki plamistej Gór Skalistych. Badając kleszcze pod kątem riketsji, Burgdorfer zauważył „słabo wybarwione, raczej długie, nieregularnie zwinięte krętki”. Dalsze badania ujawniły krętki u 60% kleszczy. Burgdorfer przypisał swojej znajomości literatury europejskiej zrozumienie, że krętki mogą być „długo poszukiwaną przyczyną ECM i boreliozy”. Benach dostarczył mu więcej kleszczy z Shelter Island i sera od osób, u których zdiagnozowano boreliozę. Badacz University of Texas Health Science Center, Alan Barbour, „zaoferował swoją wiedzę na temat hodowli i immunochemicznego scharakteryzowania organizmu”. Burgdorfer następnie potwierdził swoje odkrycie, izolując od ludzi z boreliozą krętki identyczne z tymi znalezionymi w kleszczach. W czerwcu 1982 roku opublikował swoje odkrycia w Science i na jego cześć krętek nazwano Borrelia burgdorferi .
Po zidentyfikowaniu B. burgdorferi jako czynnika wywołującego boreliozę, do badań wybrano antybiotyki, kierując się wrażliwością na antybiotyki in vitro , w tym antybiotyki tetracyklinowe , amoksycylinę , aksetyl cefuroksymu , penicylinę dożylną i domięśniową oraz ceftriakson dożylny . Mechanizm przenoszenia kleszczy był również przedmiotem wielu dyskusji. B. burgdorferi krętki zidentyfikowano w ślinie kleszcza w 1987 roku, potwierdzając hipotezę, że przenoszenie odbywało się przez gruczoły ślinowe kleszcza.
Społeczeństwo, kultura i kontrowersje
Zmiany krajobrazu i urbanizacja
Urbanizacja i inne czynniki antropogeniczne mogą być zaangażowane w rozprzestrzenianie się boreliozy na ludzi. Na wielu obszarach ekspansja dzielnic podmiejskich doprowadziła do stopniowego wylesiania okolicznych obszarów leśnych i zwiększonego kontaktu granicznego między ludźmi a obszarami gęstymi od kleszczy. Ekspansja człowieka doprowadziła również do zmniejszenia liczby drapieżników polujących na jelenie, a także myszy, wiewiórki i inne małe gryzonie – główne rezerwuary boreliozy. W wyniku wzmożonego kontaktu człowieka z gospodarzem i nosicielem znacznie wzrosło prawdopodobieństwo przeniesienia choroby. Naukowcy badają możliwe powiązania między globalne ocieplenie i rozprzestrzenianie się chorób przenoszonych przez wektory, w tym boreliozy.
Efekt rozcieńczenia
Biorąc pod uwagę tę dynamikę siedlisko-gospodarza, niektórzy badacze zaczęli postulować, czy efekt rozcieńczenia może złagodzić rozprzestrzenianie się boreliozy. Efekt rozcieńczenia to hipoteza, która przewiduje, że wzrost bioróżnorodności żywiciela spowoduje spadek liczby wektorów zakażonych B. burgdorferi . Badania naukowe wykazały, że częstość występowania infekcji nimf (NIP) zmniejsza się wraz ze wzrostem liczby gatunków żywicieli, wspierając efekt rozcieńczenia. To powiedziawszy, wyników tych nie należy błędnie interpretować, sugerując, że istnieje bezpośredni związek między zmniejszonym NIP a zmniejszonym ryzykiem epidemiologicznym, ponieważ nie zostało to jeszcze udowodnione. Ponadto należy zauważyć, że jak dotąd efekt rozcieńczenia jest obsługiwany tylko w północno-wschodnich Stanach Zjednoczonych i został obalony w innych częściach świata, w których również występują wysokie wskaźniki zachorowalności na boreliozę
Przewlekła borelioza
Termin „przewlekła borelioza” jest kontrowersyjny i nie jest uznawany w literaturze medycznej, a większość autorytetów medycznych odradza długotrwałe leczenie antybiotykami boreliozy. Badania wykazały, że większość osób, u których zdiagnozowano „przewlekłą boreliozę”, albo nie ma obiektywnych dowodów na przebytą lub obecną infekcję B. burgdorferi , albo są to osoby, które należy sklasyfikować jako cierpiące na zespół boreliozy po leczeniu (PTLDS), który definiuje się jako utrzymujące się lub nawracające niespecyficzne objawy (takie jak zmęczenie, ból mięśniowo-szkieletowy i dolegliwości poznawcze) u osoby wcześniej leczonej z powodu boreliozy.
Film dokumentalny Under Our Skin z 2008 roku znany jest z promowania kontrowersyjnych i nierozpoznanych teorii na temat „przewlekłej boreliozy”.
Inne zwierzęta
Zwierzęta
Zapobieganie boreliozie jest ważnym krokiem w zapewnieniu psom bezpieczeństwa na obszarach endemicznych. Dostępna jest edukacja profilaktyczna i szereg działań zapobiegawczych. Po pierwsze, dla właścicieli psów, którzy mieszkają w pobliżu lub często odwiedzają obszary zaatakowane przez kleszcze, ważnym krokiem są rutynowe szczepienia ich psów.
Innym kluczowym środkiem zapobiegawczym jest stosowanie trwałych środków roztoczobójczych, takich jak miejscowe repelenty lub pestycydy zawierające triazapentadieny ( Amitraz ), fenylopirazole ( Fipronil ) lub permetryna ( piretroidy ). Te akarycydy działają przede wszystkim na dorosłe stadia kleszczy przenoszących boreliozę i zmniejszają liczbę kleszczy aktywnych reprodukcyjnie w środowisku. Preparaty tych składników są dostępne w różnych postaciach do stosowania miejscowego, w tym do nakrapiania, sprayów, proszków, impregnowanych obroży, roztworów i szamponów.
Badanie psa pod kątem kleszczy po przebywaniu na obszarze występowania kleszczy jest ważnym środkiem zapobiegawczym, który należy podjąć w zapobieganiu boreliozie. Kluczowe miejsca do zbadania to głowa, szyja i uszy.
U psów poważne długoterminowe rokowanie może skutkować chorobą kłębuszków nerkowych, która jest kategorią uszkodzenia nerek, które może powodować przewlekłą chorobę nerek. Psy mogą również doświadczać przewlekłej choroby stawów, jeśli choroba nie jest leczona. Jednak większość przypadków boreliozy u psów kończy się całkowitym wyzdrowieniem po leczeniu antybiotykami, a czasem bez. [ Konieczna weryfikacja ] W rzadkich przypadkach borelioza może być śmiertelna zarówno dla ludzi, jak i psów.
![]() Ten artykuł zawiera materiały należące do domeny publicznej dotyczące zespołu boreliozy po leczeniu . Centra Kontroli i Zapobiegania Chorób .
Ten artykuł zawiera materiały należące do domeny publicznej dotyczące zespołu boreliozy po leczeniu . Centra Kontroli i Zapobiegania Chorób .
Dalsza lektura
- Ostfeld R. (2012). Choroba z Lyme: ekologia złożonego systemu . Nowy Jork: Oxford University Press . ISBN 978-0-19-992847-7 .
- Barbour AG (2015). Choroba z Lyme: dlaczego się rozprzestrzenia, jak powoduje choroby i co z tym zrobić . Baltimore. ISBN 978-1-4214-1721-9 .
- Halperin JJ, wyd. (2018). Borelioza: podejście oparte na dowodach (wyd. 2). Wallingford, Oxfordshire, Wielka Brytania: CABI. ISBN 978-1-78639-207-7 .
- Radolf JD, Samuels DS, wyd. (2021). Borelioza i nawracające krętki gorączki: genomika, biologia molekularna, interakcje gospodarza i patogeneza choroby . Poole, Wielka Brytania: Caister. ISBN 978-1-913652-61-6 .
- Oaklander M (17 czerwca 2021). „Kiedyś mieliśmy szczepionkę przeciw boreliozie. Czy jesteśmy gotowi, aby ją przywrócić?” . Czas .
Linki zewnętrzne
- CDC – borelioza
- Przewodnik Association for Public Health Laboratories – Sugerowany język raportowania, interpretacja i wytyczne dotyczące wyników testów serologicznych boreliozy
- NIH – borelioza
- Wytyczne NICE – borelioza



