Nitrogliceryna

|
|
|
|
|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Trójazotan propanu-1,2,3-triylu |
|
Inne nazwy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 1802063 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Bank Leków | |
| Karta informacyjna ECHA | 100.000.219 |
| Numer WE |
|
| 165859 | |
| KEGG | |
| Siatka | Nitrogliceryna |
|
Identyfikator klienta PubChem
|
|
| UNII | |
| Numer ONZ | 0143, 0144, 1204, 3064, 3319 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C3H5N3O9 _ _ _ _ _ _ _ | |
| Masa cząsteczkowa | 227,085 g·mol -1 |
| Wygląd | Bezbarwna ciecz |
| Gęstość | 1,6 g⋅cm -3 (przy 15 ° C) |
| Temperatura topnienia | 14 ° C (57 ° F; 287 K) |
| Temperatura wrzenia | 50 ° C (122 ° F; 323 K) Wybucha |
| Nieznacznie | |
| Rozpuszczalność | Aceton, eter, benzen, alkohol |
| dziennik P | 2.154 |
| Struktura | |
|
|
|
|
| Wybuchowe dane | |
| Wrażliwość na wstrząsy | Wysoki |
| Wrażliwość na tarcie | Wysoki |
| Prędkość detonacji | 7700 m⋅s -1 |
| czynnik RE | 1,50 |
| Termochemia | |
|
Standardowa entalpia formowania (Δ f H ⦵ 298 ) |
−370 kJ⋅mol −1 |
|
Standardowa entalpia spalania (Δ c H ⦵ 298 ) |
−1,529 MJ⋅mol −1 |
| Farmakologia | |
| C01DA02 ( KTO ) C05AE01 ( KTO ) | |
| Dożylnie, doustnie, pod język, miejscowo | |
| Farmakokinetyka : | |
| <1% | |
| Wątroba | |
| 3 min | |
| Status prawny |
|
| Zagrożenia | |
| Bezpieczeństwo i higiena pracy (BHP): | |
|
Główne zagrożenia
|
Wybuchowy, toksyczny |
| Oznakowanie GHS : | |
   
|
|
| Niebezpieczeństwo | |
| H202 , H205 , H241 , H301 , H311 , H331 , H370 | |
| P210 , P243 , P250 , P260 , P264 , P270 , P271 , P280 , P302+P352 , P410 | |
| NFPA 704 (ognisty diament) | |
| NIOSH (limity ekspozycji na zdrowie w USA): | |
|
PEL (dopuszczalny)
|
C 0,2 ppm (2 mg/m 3 ) [skóra] |
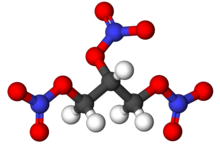
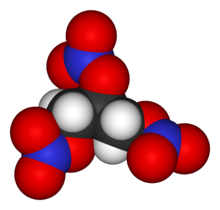
Nitrogliceryna ( NG ), (alternatywna pisownia nitrogliceryny), znana również jako trinitrogliceryna ( TNG ), nitro , triazotan glicerolu ( GTN ) lub 1,2,3-trinitroksypropan , jest gęstą, bezbarwną, oleistą, wybuchową cieczą najczęściej wytwarzaną przez nitrowanie glicerolu dymiącym na biało kwasem azotowym w warunkach odpowiednich do tworzenia estru kwasu azotowego . Chemicznie substancja jest organiczny związek azotanowy zamiast związku nitrowego , ale tradycyjna nazwa została zachowana. Wynaleziona w 1847 roku przez Ascanio Sobrero , nitrogliceryna była od tego czasu używana jako aktywny składnik do produkcji materiałów wybuchowych , a mianowicie dynamitu , i jako taka jest stosowana w przemyśle budowlanym , wyburzeniowym i górniczym . Od lat osiemdziesiątych XIX wieku jest używany przez wojsko jako składnik aktywny i żelatynizator nitrocelulozy w niektórych stałych propelentach takich jak kordyt i balistyt . Jest głównym składnikiem dwuskładnikowych bezdymnych propelentów używanych przez przeładowywacze . W połączeniu z nitrocelulozą setki kombinacji prochu są używane przez przeładowywacze karabinów, pistoletów i strzelb.
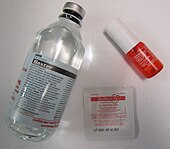
Nitrogliceryna jest stosowana w medycynie od ponad 130 lat jako silny środek rozszerzający naczynia krwionośne (rozszerzenie układu naczyniowego) w leczeniu chorób serca , takich jak dusznica bolesna i przewlekła niewydolność serca . Chociaż wcześniej było wiadomo, że te korzystne efekty wynikają z przekształcania nitrogliceryny w tlenek azotu , silny środek rozszerzający żyły, dopiero w 2002 r. odkryto, że enzymem odpowiedzialnym za tę konwersję jest mitochondrialna dehydrogenaza aldehydowa ( ALDH2 ). Nitrogliceryna jest dostępna w tabletki podjęzykowe , spraye, maści i plastry.
Historia
Nitrogliceryna była pierwszym wyprodukowanym praktycznym materiałem wybuchowym, który był silniejszy niż czarny proch . Po raz pierwszy został zsyntetyzowany przez włoskiego chemika Ascanio Sobrero w 1847 roku, pracującego pod kierunkiem Théophile'a-Julesa Pelouze'a na Uniwersytecie w Turynie . Sobrero początkowo nazwał swoje odkrycie pirogliceryną i stanowczo ostrzegał przed jej użyciem jako materiału wybuchowego.
Nitrogliceryna została później przyjęta jako komercyjnie użyteczny materiał wybuchowy przez Alfreda Nobla , który eksperymentował z bezpieczniejszymi sposobami obchodzenia się z niebezpiecznym związkiem po tym, jak jego młodszy brat Emil Oskar Nobel i kilku pracowników fabryki zginęło w eksplozji w fabryce zbrojeniowej Nobla w 1864 roku w Heleneborg , Szwecja.
Rok później Nobel założył Alfred Nobel and Company w Niemczech i zbudował odizolowaną fabrykę na wzgórzach Krümmel w Geesthacht niedaleko Hamburga . Ta firma eksportowała płynną kombinację nitrogliceryny i prochu strzelniczego zwaną „olejem wybuchowym”, ale była ona wyjątkowo niestabilna i trudna w obsłudze, o czym świadczą liczne katastrofy. Budynki fabryki Krümmel były dwukrotnie niszczone.
W kwietniu 1866 roku trzy skrzynie nitrogliceryny zostały wysłane do Kalifornii dla Central Pacific Railroad , która planowała eksperymentować z nią jako materiałem wybuchowym, aby przyspieszyć budowę tunelu Summit Tunnel o długości 1659 stóp (506 m) przez góry Sierra Nevada . Jedna ze skrzyń eksplodowała, niszcząc Wells Fargo w San Francisco i zabicie 15 osób. Doprowadziło to do całkowitego zakazu transportu płynnej nitrogliceryny w Kalifornii. wierceń i robót strzałowych w twardej skale wymaganych do ukończenia pierwszej transkontynentalnej linii kolejowej w Ameryce Północnej .
W Boże Narodzenie 1867 roku próba pozbycia się dziewięciu pojemników z olejem wybuchowym, które były nielegalnie przechowywane w White Swan Inn w centrum Newcastle Upon Tyne, doprowadziła do eksplozji na Town Moor, w której zginęło osiem osób. W czerwcu 1869 roku dwa jednotonowe wagony załadowane nitrogliceryną, znaną wówczas lokalnie jako Powder-Oil, eksplodowały na drodze w wiosce Cwm-y-glo w północnej Walii . Eksplozja doprowadziła do śmierci sześciu osób, wielu rannych i wielu zniszczeń w wiosce. Znaleziono niewiele śladów po dwóch koniach. Rząd Wielkiej Brytanii był tak zaniepokojony wyrządzonymi szkodami i tym, co mogło się wydarzyć w mieście (te dwie tony były częścią większego ładunku przybywającego z Niemiec przez Liverpool), że wkrótce uchwalił ustawę Nitro-Glycerine Act z 1869 r. Płynna nitrogliceryna była szeroko zakazane również gdzie indziej, a te ograniczenia prawne doprowadziły Alfreda Nobla i jego firmę do opracowania dynamitu w 1867 roku. Zostało to zrobione przez zmieszanie nitrogliceryny z ziemią okrzemkową („ Kieselguhr ” w języku niemieckim) znalezione na wzgórzach Krümmel. Podobne mieszaniny, takie jak „dualline” (1867), „litofracteur” (1869) i „ gelignite ” (1875), powstały przez zmieszanie nitrogliceryny z innymi obojętnymi absorbentami i wieloma kombinacjami były wypróbowywane przez inne firmy w próbach obejścia ściśle chronionych patentów Nobla na dynamit.
Mieszanki dynamitu zawierające nitrocelulozę , która zwiększa lepkość mieszanki, są powszechnie znane jako „żelatyny”.
Po odkryciu, że azotyn amylu pomaga złagodzić ból w klatce piersiowej, lekarz William Murrell eksperymentował z użyciem nitrogliceryny w celu złagodzenia dusznicy bolesnej i obniżenia ciśnienia krwi . Zaczął leczyć swoich pacjentów małymi rozcieńczonymi dawkami nitrogliceryny w 1878 roku, a leczenie to zostało wkrótce przyjęte do powszechnego użytku po tym, jak Murrell opublikował swoje wyniki w czasopiśmie The Lancet w 1879 roku. Kilka miesięcy przed śmiercią w 1896 roku Alfredowi Nobelowi przepisano nitroglicerynę na tę chorobę serca, pisząc do przyjaciela: „Czy to nie ironia losu, że przepisano mi nitroglicerynę, którą należy przyjmować wewnętrznie! Nazywają to Trinitrin, żeby nie straszyć chemika i opinii publicznej”. Z tego samego powodu placówka medyczna używała również nazwy „trójazotan glicerolu”.
Wskaźniki produkcji wojennej
Duże ilości nitrogliceryny zostały wyprodukowane podczas I i II wojny światowej do użytku jako paliwo wojskowe oraz w pracach inżynierii wojskowej . Podczas I wojny światowej, HM Factory, Gretna , największa fabryka paliwa w Wielkiej Brytanii , produkowała około 800 ton kordytu RDB tygodniowo. Ta ilość wymagała co najmniej 336 ton nitrogliceryny tygodniowo (zakładając brak strat w produkcji). Royal Navy miała własną fabrykę w Royal Navy Cordite Factory, Holton Heath , w Dorset , Anglia. Duża fabryka kordytu została również zbudowana w Kanadzie podczas I wojny światowej. Fabryka kordytu Canadian Explosives Limited w Nobel w Ontario została zaprojektowana do produkcji 1 500 000 funtów (680 ton) kordytu miesięcznie, co wymaga około 286 ton nitrogliceryny miesięcznie.
Niestabilność i desensytyzacja
W swojej nierozcieńczonej postaci nitrogliceryna jest kontaktowym materiałem wybuchowym , a wstrząs fizyczny powoduje jej eksplozję. Jeśli nie został odpowiednio oczyszczony podczas produkcji, może z czasem ulec degradacji do jeszcze bardziej niestabilnych postaci. To sprawia, że nitrogliceryna jest bardzo niebezpieczna w transporcie lub użytkowaniu. W swojej nierozcieńczonej postaci jest to jeden z najpotężniejszych materiałów wybuchowych na świecie, porównywalny z niedawno opracowanymi RDX i PETN .
Na początku swojej historii stwierdzono, że ciekła nitrogliceryna została „ znieczulona ” przez zamrożenie jej w temperaturze poniżej 45 do 55 ° F (7 do 13 ° C), w zależności od jej czystości. Jego wrażliwość na wstrząs, gdy jest zamrożona, jest nieco nieprzewidywalna: „Jest bardziej niewrażliwy na wstrząs spowodowany piorunującą czapką lub kula karabinowa w takim stanie, ale z drugiej strony wydaje się być bardziej podatna na eksplozję podczas łamania, zgniatania, ubijania itp. „Zamrożona nitrogliceryna jest znacznie mniej energetyczna niż płyn, dlatego przed użyciem należy ją rozmrozić. Rozmrażanie może być wyjątkowo uczulający, zwłaszcza jeśli obecne są zanieczyszczenia lub ogrzewanie jest zbyt szybkie.Diazotan glikolu etylenowego lub inny poliazotan można dodać w celu obniżenia temperatury topnienia, a tym samym uniknięcia konieczności rozmrażania zamrożonego materiału wybuchowego.
Chemiczne „odczulanie” nitrogliceryny jest możliwe do tego stopnia, że można ją uznać za „bezpieczną” jak nowoczesne materiały wybuchowe , takie jak dodanie etanolu , acetonu lub dinitrotoluenu . Może być konieczne wyekstrahowanie nitrogliceryny z chemicznego środka odczulającego w celu przywrócenia jego skuteczności przed użyciem, na przykład przez dodanie wody w celu usunięcia etanolu używanego jako środek odczulający.
Detonacja
Prędkość detonacji nitrogliceryny wynosi 7820 metrów na sekundę, co stanowi około 113% prędkości TNT . W związku z tym nitrogliceryna jest uważana za materiał wybuchowy o wysokim połysku , co oznacza, że ma doskonałą zdolność rozbijania. Ciepło uwalniane podczas detonacji podnosi temperaturę gazowych produktów ubocznych do około 5000 ° C (9000 ° F). Przy standardowej entalpii wybuchowego rozkładu -1414 kJ / mol i masie cząsteczkowej 227,0865 g / mol, nitrogliceryna ma gęstość energii wybuchu równą 1,488 kilokalorii na gram, czyli 6,23 kJ/g, dzięki czemu nitrogliceryna jest o 49% bardziej energetyczna w przeliczeniu na masę niż standardowa wartość definicyjna przypisana TNT (dokładnie 1 kcal/g).
Produkcja
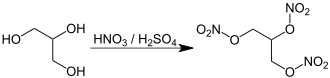
Nitroglicerynę można wytworzyć przez katalizowane kwasem nitrowanie glicerolu (gliceryny).
Przemysłowy proces produkcyjny często poddaje glicerol reakcji z prawie 1:1 mieszaniną stężonego kwasu siarkowego i stężonego kwasu azotowego . Można to wytworzyć przez zmieszanie dymiącego na biało kwasu azotowego — dość drogiego czystego kwasu azotowego , z którego usunięto tlenki azotu, w przeciwieństwie do dymiącego na czerwono kwasu azotowego , który zawiera tlenki azotu — i stężonego kwasu siarkowego . Częściej tę mieszaninę uzyskuje się tańszą metodą mieszania dymiącego kwasu siarkowego , znany również jako oleum — kwas siarkowy zawierający nadmiar trójtlenku siarki — i azeotropowy kwas azotowy (składający się z około 70% kwasu azotowego , a resztę stanowi woda).
Kwas siarkowy wytwarza protonowane formy kwasu azotowego , które są atakowane przez nukleofilowe atomy tlenu glicerolu . W ten sposób dodaje się grupę nitrową jako ester C-O-NO 2 i wytwarza się woda. Różni się to od elektrofilowej reakcji podstawienia aromatycznego, w której jony nitroniowe są elektrofilami .
Dodatek glicerolu powoduje reakcję egzotermiczną (tj. wydziela się ciepło), jak zwykle w przypadku nitrowania mieszanymi kwasami. Jeśli mieszanina stanie się zbyt gorąca, dochodzi do niekontrolowanej reakcji, stanu przyspieszonego nitrowania, któremu towarzyszy destrukcyjne utlenianie materiałów organicznych przez gorący kwas azotowy i wydzielanie się trującego dwutlenku azotu , co wiąże się z dużym ryzykiem wybuchu. W ten sposób gliceryna mieszaninę dodaje się powoli do naczynia reakcyjnego zawierającego mieszany kwas (nie kwas do gliceryny). Nitrator jest chłodzony zimną wodą lub inną mieszaniną chłodziwa i utrzymywany przez cały czas gliceryny w temperaturze około 22 ° C (72 ° F), wystarczająco gorącej, aby zaszła szybka estryfikacja, ale wystarczająco zimnej, aby uniknąć niekontrolowanej reakcji. Naczynie nitratora, często wykonane z żelaza lub ołowiu i generalnie mieszane ze sprężonym powietrzem , ma u podstawy klapę awaryjną, która wisi nad dużym basenem z bardzo zimną wodą i do której można wrzucić całą mieszaninę reakcyjną (zwaną ładunkiem), aby zapobiec eksplozji, procesowi określanemu jako utonięcie. Jeśli temperatura wsadu przekroczy około 30 °C (86 °F) (rzeczywista wartość różni się w zależności od kraju) lub w otworze wentylacyjnym nitratora widoczne są brązowe opary, oznacza to, że jest on natychmiast topiony.
Użyj jako materiał wybuchowy i propelent
Główne zastosowanie nitrogliceryny, pod względem tonażu, to materiały wybuchowe, takie jak dynamit i propelenty.
Nitrogliceryna jest oleistą cieczą, która może eksplodować pod wpływem ciepła, wstrząsu lub płomienia.
Alfred Nobel rozwinął zastosowanie nitrogliceryny jako wybuchowego materiału wybuchowego przez zmieszanie nitrogliceryny z obojętnymi absorbentami , zwłaszcza " Kieselgur ", czyli ziemią okrzemkową . Nazwał ten wybuchowy dynamit i opatentował go w 1867 roku. Dostarczany był gotowy do użycia w postaci lasek, owiniętych pojedynczo w natłuszczony wodoodporny papier. Dynamit i podobne materiały wybuchowe były powszechnie stosowane do inżynierii lądowej , takich jak wiercenie tuneli autostradowych i kolejowych , do górnictwa , do oczyszczania pól uprawnych z pniaków, w kamieniołomach i przy pracach rozbiórkowych . Podobnie inżynierowie wojskowi używali dynamitu do prac budowlanych i wyburzeniowych.
Nitrogliceryna była również stosowana jako składnik wojskowych materiałów pędnych do broni palnej .
Nitrogliceryna została wykorzystana w połączeniu ze szczelinowaniem hydraulicznym , procesem wykorzystywanym do odzyskiwania ropy i gazu z formacji łupkowych . Technika ta obejmuje przemieszczanie i detonowanie nitrogliceryny w systemach pęknięć naturalnych lub wywołanych hydraulicznie lub przemieszczanie i detonację nitrogliceryny w szczelinach wywołanych hydraulicznie, a następnie strzały z odwiertu przy użyciu granulowanego trotylu .
Nitrogliceryna ma tę przewagę nad niektórymi innymi materiałami wybuchowymi, że podczas detonacji praktycznie nie wytwarza widocznego dymu. Dlatego jest przydatny jako składnik receptury różnego rodzaju proszków bezdymnych .
Jego wrażliwość ograniczyła przydatność nitrogliceryny jako wojskowego materiału wybuchowego, a mniej wrażliwe materiały wybuchowe, takie jak TNT , RDX i HMX , w dużej mierze zastąpiły ją w amunicji. Pozostaje ważny w inżynierii wojskowej, a inżynierowie bojowi nadal używają dynamitu.
Następnie Alfred Nobel opracował balistyt , łącząc nitroglicerynę i bawełnę strzelniczą . Opatentował go w 1887 roku. Balistyt został przyjęty przez wiele rządów europejskich jako paliwo wojskowe. Jako pierwsze przyjęły go Włochy. rząd brytyjski i rządy Wspólnoty Narodów przyjęły kordyt , który został opracowany przez Sir Fredericka Abela i Sir Jamesa Dewara z Wielkiej Brytanii w 1889 r. Oryginalny Cordite Mk I składał się z 58% nitrogliceryny, 37% bawełny strzelniczej i 5,0% wazeliny . Balistyt i kordyt były wytwarzane w postaci „sznurków”.
Proszki bezdymne zostały pierwotnie opracowane przy użyciu nitrocelulozy jako jedynego składnika wybuchowego. Dlatego były znane jako propelenty jednozasadowe. Opracowano również gamę prochów bezdymnych, które zawierają zarówno nitrocelulozę, jak i nitroglicerynę, znanych jako propelenty dwuzasadowe. Proszki bezdymne były pierwotnie dostarczane tylko do celów wojskowych, ale wkrótce zostały również opracowane do użytku cywilnego i szybko zostały przyjęte do sportu. Niektóre są znane jako pudry sportowe. Propelenty trójzasadowe zawierają nitrocelulozę, nitroglicerynę i nitroguanidynę , ale są zarezerwowane głównie dla amunicji o bardzo dużym kalibrze, takiej jak ta używana w armatach czołgowych i artyleria morska . Żelatyna wybuchowa, znana również jako gelignite , została wynaleziona przez Nobla w 1875 roku przy użyciu nitrogliceryny, miazgi drzewnej oraz azotanu sodu lub potasu . Był to wczesny, tani i elastyczny materiał wybuchowy.
Zastosowanie medyczne
Nitrogliceryna należy do grupy leków zwanych azotanami, która obejmuje wiele innych azotanów, takich jak diazotan izosorbidu (Isordil) i monoazotan izosorbidu (Imdur, Ismo, Monoket). Wszystkie te czynniki wywierają swoje działanie, przekształcając się w tlenek azotu w organizmie przez mitochondrialną dehydrogenazę aldehydową ( ALDH2 ), a tlenek azotu jest silnym naturalnym środkiem rozszerzającym naczynia krwionośne.
W medycynie nitrogliceryna jest prawdopodobnie najczęściej przepisywana na dusznicę bolesną , bolesny objaw choroby niedokrwiennej serca, spowodowany niedostatecznym dopływem krwi i tlenu do serca oraz jako silny środek przeciwnadciśnieniowy. Nitrogliceryna koryguje brak równowagi między dopływem tlenu i krwi do serca a zapotrzebowaniem serca na energię. Na rynku dostępnych jest wiele preparatów w różnych dawkach. W niskich dawkach nitrogliceryna rozszerza żyły bardziej niż tętnice, zmniejszając w ten sposób napięcie wstępne (objętość krwi w sercu po wypełnieniu); uważa się, że jest to jego główny mechanizm działania. Zmniejszając obciążenie wstępne, serce ma mniej krwi do pompowania, co zmniejsza zapotrzebowanie na tlen, ponieważ serce nie musi tak ciężko pracować. Dodatkowo, posiadanie mniejszego obciążenia wstępnego zmniejsza ciśnienie przezścienne komory (nacisk wywierany na ściany serca), co zmniejsza kompresję tętnic serca, aby umożliwić przepływ większej ilości krwi przez serce. W wyższych dawkach rozszerza również tętnice, zmniejszając w ten sposób obciążenie następcze (zmniejszenie ciśnienia, z jakim serce musi pompować). Poprawa stosunku zapotrzebowania mięśnia sercowego na tlen do podaży prowadzi do następujących efektów terapeutycznych podczas epizodów dławicy piersiowej: ustąpienie bólu w klatce piersiowej, obniżenie ciśnienia krwi, przyspieszenie akcji serca, hipotonia ortostatyczna . Pacjenci cierpiący na dusznicę bolesną podczas wykonywania pewnych czynności fizycznych mogą często zapobiegać objawom, przyjmując nitroglicerynę 5 do 10 minut przed aktywnością. Przedawkowanie może wywołać methemoglobinemię .
Nitrogliceryna jest dostępna w postaci tabletek, maści, roztworu do podawania dożylnego , plastrów przezskórnych lub aerozoli podjęzykowych . Niektóre formy nitrogliceryny utrzymują się w organizmie znacznie dłużej niż inne. Nitrogliceryna oraz początek i czas działania każdej postaci jest inny. Podjęzykowy lub tabletkowy spray nitrogliceryny zaczyna działać po dwóch minutach i trwa dwadzieścia pięć minut. Doustna postać nitrogliceryny ma początek po trzydziestu pięciu minutach i czas działania 4-8 godzin. Plaster transdermalny zaczyna działać po trzydziestu minutach i trwa od dziesięciu do dwunastu godzin. Wykazano, że ciągła ekspozycja na azotany powoduje, że organizm przestaje normalnie reagować na ten lek. Eksperci zalecają, aby plastry usuwać na noc, dając organizmowi kilka godzin na przywrócenie reakcji na azotany. Krócej działające preparaty nitrogliceryny można stosować kilka razy dziennie z mniejszym ryzykiem rozwoju tolerancji. Nitrogliceryna została po raz pierwszy użyta przez Williama Murrella do leczenia ataków dusznicy bolesnej w 1878 roku, a odkrycie zostało opublikowane w tym samym roku.
Ekspozycja przemysłowa
Rzadkie narażenie na wysokie dawki nitrogliceryny może powodować silne bóle głowy znane jako „głowa NG” lub „głowa huku”. Te bóle głowy mogą być na tyle silne, że u niektórych osób powodują ubezwłasnowolnienie; jednak ludzie rozwijają tolerancję i zależność od nitrogliceryny po długotrwałym narażeniu. Chociaż rzadko, odstawienie może być śmiertelne. Objawy odstawienne obejmują ból w klatce piersiowej i inne problemy z sercem. Objawy te można złagodzić po ponownym narażeniu na nitroglicerynę lub inne odpowiednie azotany organiczne.
W przypadku pracowników zakładów produkujących nitroglicerynę (NTG) skutki odstawienia obejmują czasami „niedzielne zawały serca” u osób regularnie narażonych na nitroglicerynę w miejscu pracy, co prowadzi do rozwoju tolerancji na działanie rozszerzające żyły. W weekend pracownicy tracą tolerancję, a kiedy są ponownie narażeni w poniedziałek, drastyczne rozszerzenie naczyń powoduje przyspieszenie akcji serca , zawroty głowy i ból głowy. Nazywa się to „chorobą poniedziałkową”.
Ludzie mogą być narażeni na nitroglicerynę w miejscu pracy poprzez wdychanie jej, wchłanianie przez skórę, połykanie lub kontakt wzrokowy. Administracja ds. Bezpieczeństwa i Higieny Pracy ustaliła prawny limit ( dopuszczalny limit narażenia ) dla narażenia na nitroglicerynę w miejscu pracy na 0,2 ppm (2 mg/m 3 ) ekspozycji skóry w ciągu 8-godzinnego dnia pracy. Narodowy Instytut Bezpieczeństwa i Higieny Pracy ustalił zalecany limit narażenia skóry na 0,1 mg/m 3 w ciągu 8-godzinnego dnia pracy. Na poziomie 75 mg/m 3 nitrogliceryna jest bezpośrednio zagrażające życiu i zdrowiu .
Zobacz też
Linki zewnętrzne
- „Nitrogliceryna! Straszna eksplozja i ofiary śmiertelne w San Francisco” . Muzeum historii fotografii Central Pacific Railroad . Źródło 23 marca 2005 . – artykuł w gazecie z 1866 r
- Strona książki internetowej dla C 3 H 5 N 3 O 9
- CDC - Kieszonkowy przewodnik NIOSH dotyczący zagrożeń chemicznych
- Tales Tales of Destruction Szczegółowe i przerażające historie o historycznym użyciu torped wypełnionych nitrogliceryną do ponownego uruchomienia szybów naftowych.
- Dynamit i TNT w układzie okresowym filmów (University of Nottingham)