Wrodzona dystrofia mięśniowa Fukuyamy
| Wrodzona dystrofia mięśniowa Fukuyamy | |
|---|---|
| Inne nazwy | Wrodzona dystrofia mięśniowa typu Fukuyamy |
 | |
| Wrodzona dystrofia mięśniowa Fukuyamy ma autosomalny recesywny wzór dziedziczenia | |
| Objawy | drgawki |
| Powoduje | Mutacja genu FKTN |
| Metoda diagnostyczna | Stężenie kinazy kreatynowej w surowicy i biopsje mięśni |
| Leczenie | Fizykoterapia |
Wrodzona dystrofia mięśniowa Fukuyamy (FCMD) jest rzadką, autosomalną recesywną postacią dystrofii mięśniowej (osłabienie i rozpad tkanki mięśniowej), opisaną głównie w Japonii , ale zidentyfikowaną również u tureckich i aszkenazyjskich pacjentów pochodzenia żydowskiego; piętnaście przypadków zostało po raz pierwszy opisanych w 1960 roku przez dr Yukio Fukuyamę.
FCMD wpływa głównie na mózg , oczy i mięśnie , w szczególności zaburzenie wpływa na rozwój mięśni szkieletowych , prowadząc do osłabienia i zdeformowanego wyglądu, a rozwój mózgu jest stępiony, wpływając na funkcjonowanie poznawcze, a także umiejętności społeczne. W 1995 roku zaburzenie powiązano z mutacjami w genie kodującym białko fukutynę ( gen FCMD ). Wrodzona dystrofia mięśniowa Fukuyamy jest drugą najbardziej rozpowszechnioną postacią dystrofii mięśniowej w Japonii. Jedna na 90 osób w Japonii jest nosicielem heterozygotycznym. [ wymagany cytat medyczny ]
Objawy i oznaki
Pod względem objawów wrodzona dystrofia mięśniowa Fukuyamy charakteryzuje się obniżeniem napięcia mięśni szkieletowych oraz upośledzeniem rozwoju mózgu i oczu. Początkowe objawy FCMD występują we wczesnym okresie niemowlęcym w postaci obniżonej zdolności do pobierania pokarmu. Wyraźne różnice w wyglądzie twarzy występują z powodu zmniejszonego napięcia mięśniowego. Dalsze cechy obejmują:
- drgawki
- Opóźnienie w rozwoju
- Problemy z sercem
- Trudności w połykaniu
- Problemy neurologiczne
Wrodzona dystrofia mięśniowa Fukuyamy wpływa również na układ nerwowy i różne powiązane części. FCMD wpływa na prawidłowy rozwój mózgu, wytwarzając zasadniczo gładką, wyboistą korę zwaną lissencephaly brukowca, a także różne inne wady rozwojowe, zwłaszcza mikropolygyrię . Dzieci doświadczają również opóźnionej mielinizacji w mózgu.
Przyczyna
Przyczyna wrodzonej dystrofii mięśniowej Fukuyamy jest zakorzeniona w genie FKTN , zlokalizowanym na ludzkim chromosomie 9q31 , kodującym białko fukutynę . Mutacje w tym genie, a co za tym idzie w białku fukutyny, są przyczyną FCMD. Choroba dziedziczona jest w sposób autosomalny recesywny.
Oznacza to, że wadliwy gen odpowiedzialny za zaburzenie znajduje się na autosomie ( chromosom 9 jest autosomem), a dwie kopie wadliwego genu (po jednej odziedziczonej od każdego z rodziców) są potrzebne, aby urodzić się z zaburzeniem. Rodzice osoby z zaburzeniem dziedziczonym autosomalnie recesywnie oboje są nosicielami jednej kopii wadliwego genu, ale zwykle nie doświadczają żadnych oznak ani objawów tego zaburzenia.
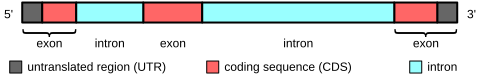
Zidentyfikowano dwie mutacje. Pierwszą i najbardziej powszechną jest retrotransposalna insercja SVA w regionie 3' nie podlegającym translacji. Druga to głęboka intronowa mutacja punktowa c.647+2084G>T. Ta druga mutacja została znaleziona do tej pory tylko w obecności pierwszej mutacji.
Patofizjologia
Mechanizm tego podtypu dystrofii mięśniowej polega na mutacji w genie FKTN, co skutkuje zniekształconym białkiem fukutyny. Uważa się, że fukutyna modyfikuje białko alfa-dystroglikanu , które jest ważne w zakotwiczaniu komórek do pewnych cząsteczek, w szczególności niektórych białek. Alfa-dystroglikan w mięśniach szkieletowych pomaga zapobiegać rozpadowi włókien mięśniowych poprzez stabilizację i ochronę. Alfa-dystroglikan pomaga również w rozwoju mózgu, pomagając w migracji neuronów. Najczęściej FKTN jest zmutowany w taki sposób, że powoduje niedobór fukutyny w komórce, co z kolei stwarza problemy podczas tworzenia alfa-dystroglikanu, prowadząc do mniejszej stabilizacji komórek mięśniowych. Używanie zdestabilizowanych włókien mięśniowych z czasem powoduje ich rozpad i stopniowy spadek napięcia mięśniowego oraz zanik włókien mięśniowych. Spadek mózgowej fukutyny powoduje, że komórki neuronalne kontynuują przemieszczanie się poza ich zamierzone miejsce. Ponadto stres oksydacyjny ma pewien wpływ na astrocyty (a także neurony ), gdy fukutyna jest osłabiona.
Diagnoza
Jeśli chodzi o diagnozę wrodzonej dystrofii mięśniowej Fukuyamy, można uzyskać stężenie kinazy kreatynowej w surowicy i biopsje mięśni, aby pomóc określić, czy dana osoba ma FMCD. Molekularne testy genetyczne FKTN są wykorzystywane do określenia mutacji w genie FKTN po tym, jak stężenie kinazy kreatynowej w surowicy, biopsje mięśni i/lub obrazowanie MRI wykazało nieprawidłowości wskazujące na FCMD, obecność objawów wskazuje na wrodzoną dystrofię mięśniową Fukuyamy. Dostępne testy genetyczne obejmują:
- Analiza powiązań
- Analiza usuwania
- Analiza sekwencji - egzony
- Analiza sekwencji - cały region kodujący
Leczenie
Obecnie ten podtyp dystrofii mięśniowej nie ma lekarstwa i nie istnieje żadne ostateczne leczenie. Leczenie oferuje taktykę zapobiegawczą, aby opóźnić rozpad mięśni i wydłużyć oczekiwaną długość życia. Rozciąganie i fizykoterapia mogą zwiększyć mobilność. Leczenie obejmuje również korygowanie nieprawidłowości szkieletowych poprzez chirurgię ortopedyczną i inne techniki ortopedyczne. Podaje się leki przeciwpadaczkowe, aby zapobiec napadom padaczkowym. Inhibitory ACE i beta-adrenolityki pomagają leczyć choroby serca, a wspomaganie oddychania jest bardziej niż prawdopodobne, że w pewnym momencie osoba dotknięta chorobą jest potrzebna.
Rokowanie
Wrodzona dystrofia mięśniowa Fukuyamy ma złe rokowanie. Większość dzieci z FCMD osiąga maksymalną mobilność w pozycji siedzącej i ślizgającej się. Ze względu na złożone skutki stale nasilających się problemów z sercem, upośledzony umysłowy , problemy z połykaniem i dodatkowe powikłania, dzieci z FCMD rzadko przeżywają okres dojrzewania, zaburzenie to kończy się śmiercią przed ukończeniem 20 roku życia.
Zobacz też
Dalsza lektura
- Aida, N.; Tamagawa, K.; Takada, K.; Yagishita, A.; Kobayashi, N.; Chikumaru, K.; Iwamoto, H. (1996-04-01). „Mózg MR w wrodzonej dystrofii mięśniowej Fukuyamy” . American Journal of Neuroradiology . 17 (4): 605–613. ISSN 0195-6108 . PMC 8337276 . PMID 8730178 .
- Saito, Fumiaki; Matsumura, Kiichiro (2011-01-01). „Wrodzona dystrofia mięśniowa typu Fukuyama i wadliwa glikozylacja α-dystroglikanu” . Mięsień szkieletowy . 1:22 . doi : 10.1186/2044-5040-1-22 . ISSN 2044-5040 . PMC 3156645 .
- Dystrofia mięśniowa typu Fukuyama w Biurze Chorób Rzadkich NIH