Inżynieria biomedyczna
Inżynieria biomedyczna ( BME ) lub inżynieria medyczna to zastosowanie zasad inżynierii i koncepcji projektowych w medycynie i biologii do celów opieki zdrowotnej (np. Diagnostyka lub terapia). BME jest również tradycyjnie nauką logiczną służącą postępowi w leczeniu opieki zdrowotnej, w tym diagnozie , monitorowaniu i terapii . W zakres inżyniera biomedycznego wchodzi również zarządzanie obecnym sprzętem medycznym w szpitalach przy jednoczesnym przestrzeganiu odpowiednich standardów branżowych. Obejmuje to zamówienia, rutynowe testy, konserwację zapobiegawczą i wydawanie zaleceń dotyczących sprzętu, rolę znaną również jako technik sprzętu biomedycznego (BMET) lub inżynieria kliniczna .
Inżynieria biomedyczna pojawiła się niedawno jako odrębna dziedzina nauki w porównaniu z wieloma innymi dziedzinami inżynierii. Taka ewolucja jest powszechna jako przejście nowej dziedziny od specjalizacji interdyscyplinarnej wśród już ustalonych dziedzin do uznania jej za dziedzinę samą w sobie. Wiele prac w inżynierii biomedycznej składa się z badań i rozwoju , obejmujących szeroki wachlarz poddziedzin (patrz poniżej). Wybitne zastosowania inżynierii biomedycznej obejmują rozwój biokompatybilnych protez , różnych diagnostycznych i terapeutycznych urządzeń medycznych , od sprzętu klinicznego po mikroimplanty, powszechny sprzęt do obrazowania, taki jak MRI i EKG / EKG, regeneracyjny wzrost tkanek, leki farmaceutyczne i biologiczne środki terapeutyczne.
Bioinformatyka

Bioinformatyka to interdyscyplinarna dziedzina, która rozwija metody i narzędzia programowe do zrozumienia danych biologicznych. Jako interdyscyplinarna dziedzina nauki, bioinformatyka łączy informatykę, statystykę, matematykę i inżynierię w celu analizy i interpretacji danych biologicznych.
Bioinformatyka jest uważana zarówno za ogólne określenie zbioru badań biologicznych, które wykorzystują programowanie komputerowe jako część swojej metodologii, jak i odniesienie do określonych „rurociągów” analitycznych, które są wielokrotnie używane, szczególnie w dziedzinie genomiki. Typowe zastosowania bioinformatyki obejmują identyfikację potencjalnych genów i nukleotydów (SNP). Często taka identyfikacja ma na celu lepsze zrozumienie genetycznych podstaw choroby, unikalnych adaptacji, pożądanych właściwości (zwłaszcza u gatunków rolniczych) lub różnic między populacjami. W mniej formalny sposób bioinformatyka próbuje również zrozumieć zasady organizacji sekwencji kwasów nukleinowych i białek.
Biomechanika
Biomechanika to badanie struktury i funkcji mechanicznych aspektów systemów biologicznych na każdym poziomie, od całych organizmów po narządy , komórki i organelle komórkowe , przy użyciu metod mechaniki .
Biomateriał
Biomateriał to dowolna materia, powierzchnia lub konstrukcja, która wchodzi w interakcję z systemami żywymi . Jako nauka biomateriały mają około pięćdziesięciu lat. Badanie biomateriałów nazywa się nauką o biomateriałach lub inżynierią biomateriałów . Odnotowuje stały i silny wzrost w swojej historii, a wiele firm inwestuje duże kwoty w rozwój nowych produktów. Nauka o biomateriałach obejmuje elementy medycyny, biologii, chemii, inżynierii tkankowej i materiałoznawstwa.
Optyka biomedyczna
Optyka biomedyczna łączy zasady fizyki, inżynierii i biologii w celu badania interakcji tkanki biologicznej i światła oraz tego, jak można to wykorzystać do wykrywania, obrazowania i leczenia. Ma szeroki zakres zastosowań, w tym obrazowanie optyczne, mikroskopię, oftalmoskopię, spektroskopię i terapię. Przykłady technik i technologii optyki biomedycznej obejmują optyczną tomografię koherencyjną (OCT), mikroskopię fluorescencyjną , mikroskopię konfokalną i terapię fotodynamiczną (PDT). Na przykład OCT wykorzystuje światło do tworzenia trójwymiarowych obrazów o wysokiej rozdzielczości struktur wewnętrznych, takich jak siatkówka w oku lub tętnice wieńcowe w sercu. Mikroskopia fluorescencyjna polega na znakowaniu określonych cząsteczek barwnikami fluorescencyjnymi i wizualizowaniu ich za pomocą światła, co zapewnia wgląd w procesy biologiczne i mechanizmy chorobowe. Niedawno optyka adaptatywna pomaga w obrazowaniu, korygując aberracje w tkance biologicznej, umożliwiając obrazowanie w wyższej rozdzielczości i lepszą dokładność w procedurach, takich jak chirurgia laserowa i obrazowanie siatkówki.
Inżynieria tkankowa
Inżynieria tkankowa, podobnie jak inżynieria genetyczna (patrz poniżej), jest głównym segmentem biotechnologii - który w znacznym stopniu pokrywa się z BME.
Jednym z celów inżynierii tkankowej jest tworzenie sztucznych narządów (za pomocą materiału biologicznego) dla pacjentów potrzebujących przeszczepów narządów. Inżynierowie biomedyczni badają obecnie metody tworzenia takich organów. W tym celu naukowcy wyhodowali solidne kości szczęki i tchawice z ludzkich komórek macierzystych. Kilka sztucznych pęcherzy moczowych wyhodowano w laboratoriach i z powodzeniem przeszczepiono ludziom. Biosztuczne narządy, które wykorzystują zarówno komponenty syntetyczne, jak i biologiczne, są również przedmiotem zainteresowania w badaniach, na przykład w przypadku urządzeń wspomagających wątrobę, które wykorzystują komórki wątroby w konstrukcie sztucznego bioreaktora.

Inżynieria genetyczna
Inżynieria genetyczna, technologia rekombinacji DNA, modyfikacja/manipulacja genetyczna (GM) i składanie genów to terminy odnoszące się do bezpośredniej manipulacji genami organizmu. W przeciwieństwie do tradycyjnej hodowli, pośredniej metody manipulacji genetycznej, inżynieria genetyczna wykorzystuje nowoczesne narzędzia, takie jak klonowanie i transformacja molekularna, aby bezpośrednio zmieniać strukturę i cechy docelowych genów. Techniki inżynierii genetycznej odniosły sukces w wielu zastosowaniach. Niektóre przykłady obejmują udoskonalenie technologii upraw ( nie zastosowania medyczne , ale inżynieria systemów biologicznych ), wytwarzanie syntetycznej insuliny ludzkiej przy użyciu zmodyfikowanych bakterii, wytwarzanie erytropoetyny w komórkach jajnika chomika oraz wytwarzanie nowych typów eksperymentalne myszy, takie jak oncomous (mysz rakowa) do badań. [ potrzebne źródło ]
Inżynieria neuronowa
Inżynieria neuronowa (znana również jako neuroinżynieria) to dyscyplina, która wykorzystuje techniki inżynieryjne do zrozumienia, naprawy, wymiany lub ulepszenia systemów neuronowych. Inżynierowie neuronowi mają wyjątkowe kwalifikacje do rozwiązywania problemów projektowych na styku żywej tkanki nerwowej i nieożywionych konstrukcji.
Inżynieria farmaceutyczna
Inżynieria farmaceutyczna to interdyscyplinarna nauka, która obejmuje inżynierię leków, dostarczanie i celowanie nowych leków, technologię farmaceutyczną, operacje jednostkowe inżynierii chemicznej i analizę farmaceutyczną. Można ją uznać za część farmacji ze względu na skupienie się na wykorzystaniu technologii środków chemicznych w zapewnieniu lepszego leczenia.
Urządzenia szpitalne i medyczne
Jest to niezwykle szeroka kategoria — zasadniczo obejmująca wszystkie produkty ochrony zdrowia, które nie osiągają zamierzonych rezultatów głównie środkami chemicznymi (np. farmaceutyki) lub biologicznymi (np. szczepionki) i nie wymagają metabolizmu.
Wyrób medyczny przeznaczony jest do stosowania w:
- rozpoznanie choroby lub innych stanów
- w leczeniu, łagodzeniu, leczeniu lub zapobieganiu chorobom.
Niektóre przykłady obejmują rozruszniki serca , pompy infuzyjne , płuco-serce , maszyny do dializy , sztuczne narządy , implanty , protezy kończyn , soczewki korekcyjne , implanty ślimakowe , protezy oka , protezy twarzy , protezy somatyczne i implanty dentystyczne .
Stereolitografia jest praktycznym przykładem wykorzystania modelowania medycznego do tworzenia obiektów fizycznych. Oprócz modelowania narządów i ludzkiego ciała, nowe techniki inżynieryjne są obecnie wykorzystywane w badaniach i rozwoju nowych urządzeń do innowacyjnych terapii, terapii, monitorowania pacjentów i złożonych chorób.
Urządzenia medyczne są regulowane i klasyfikowane (w USA) w następujący sposób (patrz także Rozporządzenie ):
- Urządzenia klasy I stwarzają minimalne zagrożenie dla użytkownika i często mają prostszą konstrukcję niż urządzenia klasy II lub klasy III. Urządzenia w tej kategorii obejmują szpatułki do języka, baseny, bandaże elastyczne, rękawiczki do badań i ręczne instrumenty chirurgiczne oraz inne podobne rodzaje powszechnego wyposażenia.
- Urządzenia klasy II podlegają specjalnym kontrolom oprócz ogólnych kontroli urządzeń klasy I. Specjalne kontrole mogą obejmować specjalne wymagania dotyczące etykietowania, obowiązkowe standardy wydajności i nadzór po wprowadzeniu do obrotu . Urządzenia w tej klasie są zazwyczaj nieinwazyjne i obejmują aparaty rentgenowskie, PACS, elektryczne wózki inwalidzkie, pompy infuzyjne i obłożenia chirurgiczne.
- Urządzenia klasy III na ogół wymagają zatwierdzenia przed wprowadzeniem na rynek (PMA) lub powiadomienia przed wprowadzeniem na rynek (510 tys.), przeglądu naukowego w celu zapewnienia bezpieczeństwa i skuteczności urządzenia, oprócz ogólnych kontroli klasy I. Przykłady obejmują wymianę zastawek serca, implanty stawu biodrowego i kolanowego , implanty piersi wypełnione żelem silikonowym, wszczepione stymulatory móżdżku, wszczepialne generatory impulsów rozrusznika serca i implanty śródkostne.
Obrazowanie medyczne
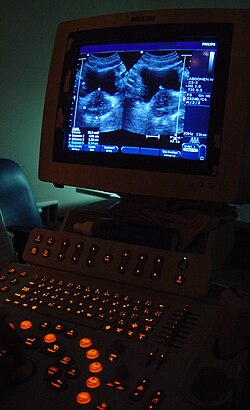
Obrazowanie medyczne/biomedyczne to główny segment urządzeń medycznych . Ten obszar dotyczy umożliwienia klinicystom bezpośredniego lub pośredniego „oglądania” rzeczy niewidocznych na pierwszy rzut oka (na przykład ze względu na ich rozmiar i / lub lokalizację). Może to obejmować wykorzystanie ultradźwięków, magnetyzmu, UV, radiologii i innych środków.
Alternatywnie, sprzęt nawigacyjny wykorzystuje technologię śledzenia elektromagnetycznego , taką jak umieszczanie cewnika w mózgu lub systemy umieszczania rurek żywieniowych . Na przykład ENvue firmy ENvizion Medical, elektromagnetyczny system nawigacji do umieszczania rurki do żywienia dojelitowego. System wykorzystuje zewnętrzny generator pola i kilka pasywnych czujników EM umożliwiających skalowanie wyświetlacza do konturów ciała pacjenta oraz podgląd w czasie rzeczywistym położenia i kierunku końcówki zgłębnika, co pomaga personelowi medycznemu zapewnić prawidłowe umieszczenie w przewodzie pokarmowym traktat .
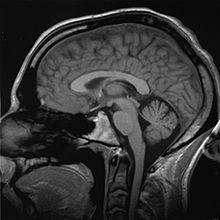
Technologie obrazowania są często niezbędne w diagnostyce medycznej i są zazwyczaj najbardziej złożonym sprzętem znajdującym się w szpitalu, w tym: fluoroskopia , obrazowanie metodą rezonansu magnetycznego (MRI), medycyna nuklearna , pozytonowa tomografia emisyjna (PET), skany PET-CT , radiografia projekcyjna, taka jak Rentgen i tomografia komputerowa , tomografia , ultradźwięki , mikroskopia optyczna i mikroskopia elektronowa .
Implanty
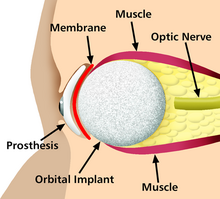
Implant jest rodzajem urządzenia medycznego, które zastępuje i pełni rolę brakującej struktury biologicznej (w porównaniu z przeszczepem, który wskazuje na przeszczepioną tkankę biomedyczną). Powierzchnia implantów stykająca się z ciałem może być wykonana z materiału biomedycznego, takiego jak tytan, silikon lub apatyt, w zależności od tego, co jest najbardziej funkcjonalne. W niektórych przypadkach implanty zawierają elektronikę, np. sztuczne rozruszniki serca i implanty ślimakowe. Niektóre implanty są bioaktywne, na przykład urządzenia do podskórnego podawania leków w postaci wszczepialnych pigułek lub stentów uwalniających lek .

Bionika
Sztuczne zamienniki części ciała to jedno z wielu zastosowań bioniki. Zainteresowana skomplikowanymi i dokładnymi badaniami właściwości i funkcji układów ludzkiego ciała, bionika może być stosowana do rozwiązywania niektórych problemów inżynierskich. Dokładne badanie różnych funkcji i procesów zachodzących w oczach, uszach i innych narządach utorowało drogę do ulepszonych aparatów fotograficznych, telewizorów, nadajników i odbiorników radiowych oraz wielu innych narzędzi.
Czujniki biomedyczne
W ostatnich latach coraz więcej uwagi poświęca się czujnikom biomedycznym opartym na technologii mikrofalowej. Można wytwarzać różne czujniki do określonych zastosowań zarówno w diagnozowaniu, jak i monitorowaniu stanów chorobowych, na przykład czujniki mikrofalowe mogą być stosowane jako technika uzupełniająca promieniowanie rentgenowskie do monitorowania urazów kończyn dolnych. Czujnik monitoruje właściwości dielektryczne, dzięki czemu może zauważyć zmiany w tkance (kości, mięśniach, tłuszczu itp.) pod skórą, więc podczas pomiaru w różnych momentach procesu gojenia reakcja czujnika będzie się zmieniać w miarę gojenia się urazu.
Inżynieria kliniczna
Inżynieria kliniczna to dziedzina inżynierii biomedycznej zajmująca się faktycznym wdrażaniem sprzętu i technologii medycznych w szpitalach lub innych placówkach klinicznych. Główne role inżynierów klinicznych obejmują szkolenie i nadzorowanie techników sprzętu biomedycznego (BMET) , wybieranie produktów/usług technologicznych i logistyczne zarządzanie ich wdrażaniem, współpracę z rządowymi organami regulacyjnymi w zakresie inspekcji/audytów oraz służenie jako konsultanci technologiczni dla innego personelu szpitala (np. , IT itp.). Inżynierowie kliniczni doradzają również i współpracują z producentami urządzeń medycznych w zakresie potencjalnych ulepszeń projektowych w oparciu o doświadczenia kliniczne, a także monitorują postęp stanu techniki, aby odpowiednio przekierować wzorce zamówień.
Ich nieodłączne skupienie na praktycznym wdrażaniu technologii sprawia, że są bardziej zorientowani na stopniowe przeprojektowywanie i rekonfiguracje, w przeciwieństwie do rewolucyjnych badań i rozwoju lub pomysłów, które miałyby wiele lat od przyjęcia klinicznego; jednak coraz częściej podejmuje się wysiłki, aby rozszerzyć ten horyzont czasowy, w którym inżynierowie kliniczni mogą wpływać na trajektorię innowacji biomedycznych. Pełniąc różne role, tworzą oni „pomost” między głównymi projektantami a użytkownikami końcowymi, łącząc perspektywę bycia blisko miejsca użycia, a jednocześnie przeszkoleni w zakresie inżynierii produktu i procesu. Działy inżynierii klinicznej czasami zatrudniają nie tylko inżynierów biomedycznych, ale także inżynierów przemysłowych / systemowych, aby pomogli w badaniach / optymalizacji operacyjnej, czynnikach ludzkich, analizie kosztów itp. Zobacz także inżynierię bezpieczeństwa, aby zapoznać się z omówieniem procedur stosowanych do projektowania bezpiecznych systemów . Dział inżynierii klinicznej składa się z kierownika, przełożonego, inżyniera i technika. Jeden inżynier na osiemdziesiąt łóżek w szpitalu to stosunek. Inżynierowie kliniczni są również upoważnieni do przeprowadzania audytów sklepów farmaceutycznych i powiązanych sklepów w celu monitorowania wycofywania przez FDA produktów inwazyjnych.
Inżynieria Rehabilitacji
Inżynieria rehabilitacyjna to systematyczne stosowanie nauk inżynieryjnych do projektowania, opracowywania, adaptacji, testowania, oceny, stosowania i dystrybucji rozwiązań technologicznych problemów, z którymi borykają się osoby niepełnosprawne. Obszary funkcjonalne, do których odnosi się inżynieria rehabilitacji, mogą obejmować mobilność, komunikację, słuch, wzrok i funkcje poznawcze oraz czynności związane z zatrudnieniem, niezależnym życiem, edukacją i integracją ze społecznością.
Podczas gdy niektórzy inżynierowie rehabilitacji mają tytuł magistra inżynierii rehabilitacji, zwykle specjalność inżynierii biomedycznej, większość inżynierów rehabilitacji ma tytuł licencjata lub magistra inżynierii biomedycznej, inżynierii mechanicznej lub elektrotechniki. Portugalski uniwersytet zapewnia tytuł licencjata i magistra inżynierii rehabilitacji i dostępności. Kwalifikacja do zostania inżynierem rehabilitacji w Wielkiej Brytanii jest możliwa poprzez uniwersytecki kurs licencjacki z wyróżnieniem, taki jak Health Design & Technology Institute, Coventry University.
Proces rehabilitacji osób niepełnosprawnych często obejmuje projektowanie urządzeń wspomagających, takich jak pomoce do chodzenia, które mają na celu promowanie włączenia ich użytkowników do głównego nurtu społeczeństwa, handlu i rekreacji.
Kwestie regulacyjne
Kwestie regulacyjne były stale zwiększane w ostatnich dziesięcioleciach, aby reagować na wiele incydentów powodowanych przez urządzenia dla pacjentów. Na przykład w latach 2008-2011 w Stanach Zjednoczonych wycofano 119 wyrobów medycznych sklasyfikowanych jako I klasa przez FDA. Według amerykańskiej Agencji ds. Żywności i Leków (FDA), wycofanie I klasy wiąże się z „ sytuacją, w której istnieje prawdopodobieństwo, że użycie lub narażenie na produkt spowoduje poważne niekorzystne skutki zdrowotne lub śmierć”
Niezależnie od przepisów krajowych, główne cele regulacyjne są zbieżne na całym świecie. Na przykład w przepisach dotyczących wyrobów medycznych wyrób musi być: 1) bezpieczny i 2) skuteczny oraz 3) dla wszystkich produkowanych wyrobów (dlaczego ta część została usunięta?)
Produkt jest bezpieczny, jeśli pacjenci, użytkownicy i osoby trzecie nie narażają się na niedopuszczalne ryzyko zagrożeń fizycznych (śmierć, urazy, ...) podczas jego zamierzonego użycia. Na urządzeniach należy wprowadzić środki ochronne, aby ograniczyć ryzyko szczątkowe do akceptowalnego poziomu w porównaniu z korzyściami płynącymi z ich użytkowania.
Produkt jest skuteczny, jeśli działa zgodnie z przeznaczeniem określonym przez producenta. Skuteczność osiąga się poprzez ocenę kliniczną, zgodność ze standardami wydajności lub wykazanie znacznej równoważności z wyrobem już wprowadzonym na rynek.
Powyższe cechy muszą być zapewnione dla wszystkich produkowanych elementów wyrobu medycznego. Wymaga to wdrożenia systemu jakości dla wszystkich odpowiednich podmiotów i procesów, które mogą mieć wpływ na bezpieczeństwo i skuteczność w całym cyklu życia wyrobu medycznego.
Dziedzina inżynierii urządzeń medycznych jest jedną z najbardziej regulowanych dziedzin inżynierii, a praktykujący inżynierowie biomedyczni muszą rutynowo konsultować się i współpracować z prawnikami regulacyjnymi i innymi ekspertami. Food and Drug Administration (FDA) jest głównym organem regulacyjnym opieki zdrowotnej w Stanach Zjednoczonych, mającym jurysdykcję nad urządzeniami medycznymi produktami złożonymi . Nadrzędnymi celami, na których opierają się decyzje polityczne FDA, są bezpieczeństwo i skuteczność produktów medycznych, które muszą być zapewnione poprzez wdrożony system jakości, zgodnie z rozporządzeniem 21 CFR 829 . Ponadto, ponieważ inżynierowie biomedyczni często opracowują urządzenia i technologie do użytku „konsumentów”, takie jak urządzenia do fizykoterapii (które są również urządzeniami „medycznymi”), mogą one również podlegać pod pewnymi względami Komisji ds. Bezpieczeństwa Produktów Konsumenckich . Największymi przeszkodami są zazwyczaj „pozwolenia” na 510 tys. (zwykle w przypadku urządzeń klasy 2) lub „zatwierdzenie” przed wprowadzeniem na rynek (zwykle w przypadku leków i urządzeń klasy 3).
W kontekście europejskim bezpieczeństwo, skuteczność i jakość są zapewnione poprzez „Ocenę zgodności”, która jest zdefiniowana jako „metoda, za pomocą której producent wykazuje, że jego urządzenie spełnia wymagania europejskiej dyrektywy dotyczącej wyrobów medycznych ” . Dyrektywa określa różne procedury w zależności od klasy urządzenia, od prostej deklaracji zgodności (załącznik VII) dla urządzeń klasy I po weryfikację WE (załącznik IV), zapewnienie jakości produkcji (załącznik V), zapewnienie jakości produktu (załącznik VI) oraz pełne zapewnienie jakości (załącznik II). Dyrektywa dotycząca urządzeń medycznych określa szczegółowe procedury certyfikacji. Ogólnie rzecz biorąc, procedury te obejmują testy i weryfikacje, które mają być zawarte w określonych dostawach, takich jak dokumentacja zarządzania ryzykiem, dokumentacja techniczna i dostawy systemu jakości. Plik zarządzania ryzykiem jest pierwszym elementem dostarczanym, który warunkuje następujące etapy projektowania i produkcji. Etap zarządzania ryzykiem prowadzi produkt w taki sposób, aby ryzyko związane z produktem zostało ograniczone do akceptowalnego poziomu w odniesieniu do korzyści oczekiwanych dla pacjentów w związku z używaniem wyrobu. Dokumentacja techniczna zawiera wszystkie dane dokumentacyjne i zapisy potwierdzające certyfikację wyrobu medycznego. Plik techniczny FDA ma podobną zawartość, chociaż ma inną strukturę. Wyniki Systemu Jakości zwykle obejmują procedury, które zapewniają jakość we wszystkich cyklach życia produktu. Ta sama norma (ISO EN 13485) jest zwykle stosowana w systemach zarządzania jakością w USA i na całym świecie.

W Unii Europejskiej istnieją jednostki certyfikujące zwane „ jednostkami notyfikowanymi ”, akredytowane przez państwa członkowskie UE. Jednostki Notyfikowane muszą zapewnić skuteczność procesu certyfikacji dla wszystkich wyrobów medycznych poza wyrobami klasy I, gdzie do wprowadzenia do obrotu wystarcza deklaracja zgodności wystawiona przez producenta. Po przejściu przez produkt wszystkich etapów wymaganych przez dyrektywę dotyczącą wyrobów medycznych, urządzenie może nosić oznakowanie CE wskazujące, że urządzenie jest uważane za bezpieczne i skuteczne, gdy jest używane zgodnie z przeznaczeniem, a zatem może być wprowadzane do obrotu w ramach obszarze Unii Europejskiej.
Różne rozwiązania regulacyjne czasami powodują, że określone technologie są opracowywane najpierw dla Stanów Zjednoczonych lub Europy, w zależności od korzystniejszej formy regulacji. Podczas gdy narody często dążą do merytorycznej harmonii, aby ułatwić międzynarodową dystrybucję, różnice filozoficzne dotyczące optymalnego zakresu regulacji mogą być przeszkodą; bardziej restrykcyjne przepisy wydają się atrakcyjne na poziomie intuicyjnym, ale krytycy potępiają koszt kompromisu w postaci spowolnienia dostępu do rozwiązań ratujących życie.
RoHS II
Dyrektywa 2011/65/UE, lepiej znana jako RoHS 2, to przekształcenie prawodawstwa pierwotnie wprowadzonego w 2002 r. Pierwotne prawodawstwo UE „Ograniczenia dotyczące niektórych niebezpiecznych substancji w urządzeniach elektrycznych i elektronicznych” (dyrektywa RoHS 2002/95/WE) zostało zastąpione i zastąpiona dyrektywą 2011/65/UE opublikowaną w lipcu 2011 r. i powszechnie znaną jako RoHS 2. RoHS ma na celu ograniczenie niebezpiecznych substancji znajdujących się w obiegu w produktach elektronicznych, w szczególności toksyn i metali ciężkich, które są następnie uwalniane do środowiska podczas recyklingu takich urządzeń .
Zakres dyrektywy RoHS 2 zostaje poszerzony o produkty wcześniej wyłączone, takie jak urządzenia medyczne i sprzęt przemysłowy. Ponadto producenci są teraz zobowiązani do dostarczania ocen ryzyka zgodności i raportów z badań – lub wyjaśnienia, dlaczego ich brakuje. Po raz pierwszy nie tylko producenci, ale także importerzy i dystrybutorzy są współodpowiedzialni za zapewnienie, że sprzęt elektryczny i elektroniczny objęty dyrektywą RoHS jest zgodny z limitami substancji niebezpiecznych i posiada znak CE na swoich produktach.
IEC60601
Nowa norma międzynarodowa IEC 60601 dotycząca urządzeń elektromedycznych do domowej opieki zdrowotnej, określająca wymagania dla urządzeń używanych w środowisku domowej opieki zdrowotnej. Norma IEC 60601-1-11 (2010) musi być teraz włączona do projektowania i weryfikacji szerokiej gamy urządzeń medycznych do użytku domowego iw punktach opieki wraz z innymi obowiązującymi normami z serii 3. edycji IEC 60601.
Obowiązkową datą wdrożenia europejskiej wersji normy EN jest 1 czerwca 2013 r. Amerykańska FDA wymaga stosowania normy 30 czerwca 2013 r., podczas gdy ostatnio Health Canada przedłużyła wymagany termin z czerwca 2012 r. na kwiecień 2013 r. Agencje północnoamerykańskie będą wymagać tych norm tylko w przypadku zgłaszania nowych urządzeń, podczas gdy UE zastosuje bardziej surowe podejście, wymagając, aby wszystkie mające zastosowanie urządzenia wprowadzane na rynek uwzględniały standard domowej opieki zdrowotnej.
AS/NZS 3551:2012
AS/ANS 3551:2012 to australijskie i nowozelandzkie standardy zarządzania wyrobami medycznymi. Norma określa procedury wymagane do utrzymania szerokiej gamy zasobów medycznych w warunkach klinicznych (np. Szpital). Normy oparte są na normach IEC 606101.
Norma obejmuje szeroki zakres elementów zarządzania sprzętem medycznym, w tym zaopatrzenie, testy akceptacyjne, konserwację (testy bezpieczeństwa elektrycznego i konserwacji zapobiegawczej) oraz wycofanie z eksploatacji.
Szkolenia i certyfikacja
Edukacja
Inżynierowie biomedyczni wymagają znacznej wiedzy zarówno z zakresu inżynierii, jak i biologii i zazwyczaj mają tytuł licencjata (licencjat, licencjat, licencjat lub inżynier BSE) lub magister (MS, mgr, MSE lub mgr inż.) lub stopień doktora (Ph.D. lub MD-PhD ) w BME (inżynieria biomedyczna) lub innej gałęzi inżynierii ze znacznym potencjałem nakładania się BME. Wraz ze wzrostem zainteresowania BME wiele uczelni inżynierskich ma obecnie wydział lub program inżynierii biomedycznej, z ofertami od poziomu licencjackiego (licencjat, licencjat, licencjat lub BSE) do poziomu doktoranckiego. Inżynieria biomedyczna dopiero niedawno pojawiła się jako odrębna dyscyplina, a nie interdyscyplinarna hybrydowa specjalizacja innych dyscyplin; a programy BME na wszystkich poziomach stają się coraz bardziej rozpowszechnione, w tym Bachelor of Science in Biomedical Engineering, który zawiera wystarczającą ilość treści z nauk biologicznych, aby wielu studentów używało go jako specjalizacji „ przedmedycznej ” w ramach przygotowań do szkoły medycznej . Oczekuje się, że liczba inżynierów biomedycznych wzrośnie zarówno jako przyczyna, jak i skutek ulepszeń technologii medycznej.
W Stanach Zjednoczonych coraz więcej programów studiów licencjackich jest również uznawanych przez ABET za akredytowane programy bioinżynierii / inżynierii biomedycznej. Od 2023 r. 155 programów jest obecnie akredytowanych przez ABET.
W Kanadzie i Australii powszechne są akredytowane programy dla absolwentów inżynierii biomedycznej. Na przykład McMaster University oferuje tytuł magistra, doktora medycyny i doktora inżynierii biomedycznej. Pierwszy kanadyjski studiów licencjackich BME był oferowany na Uniwersytecie Ryerson jako czteroletni licencjat. program. Politechnika w Montrealu oferuje również tytuł licencjata z inżynierii biomedycznej, podobnie jak Uniwersytet Flindersa.
Podobnie jak w przypadku wielu stopni, reputacja i ranking programu mogą mieć wpływ na to, czy posiadacz stopnia naukowego jest pożądany do zatrudnienia lub przyjęcia na studia. Reputacja wielu stopni licencjackich jest również powiązana z programami studiów podyplomowych lub badawczymi instytucji, które mają pewne namacalne czynniki oceny, takie jak finansowanie i wielkość badań, publikacje i cytowania. Szczególnie w przypadku BME ranking szpitala uniwersyteckiego i szkoły medycznej może być również istotnym czynnikiem wpływającym na postrzegany prestiż wydziału / programu BME.
Kształcenie absolwentów jest szczególnie ważnym aspektem w BME. Podczas gdy wiele dziedzin inżynierii (takich jak inżynieria mechaniczna lub elektryczna) nie wymaga szkolenia na poziomie magisterskim, aby uzyskać pracę na poziomie podstawowym w swojej dziedzinie, większość stanowisk BME preferuje je lub nawet wymaga. Ponieważ większość zawodów związanych z BME wiąże się z badaniami naukowymi, takimi jak farmaceutyków i urządzeń medycznych , wykształcenie wyższe jest niemal wymogiem (ponieważ stopnie licencjackie zazwyczaj nie wymagają wystarczającego przeszkolenia i doświadczenia badawczego). Może to być stopień magistra lub doktora; podczas gdy w niektórych specjalnościach dr. jest znacznie bardziej powszechny niż w innych, prawie nigdy nie stanowi większości (z wyjątkiem środowiska akademickiego). W rzeczywistości postrzegana potrzeba posiadania pewnego rodzaju dyplomu ukończenia studiów jest tak silna, że niektóre programy licencjackie BME będą aktywnie zniechęcać studentów do studiowania na kierunku BME bez wyraźnego zamiaru uzyskania tytułu magistra lub późniejszego ubiegania się o przyjęcie do szkoły medycznej.
Programy studiów podyplomowych w BME, podobnie jak w innych dziedzinach naukowych, są bardzo zróżnicowane, a poszczególne programy mogą podkreślać pewne aspekty w tej dziedzinie. Mogą również obejmować szeroko zakrojoną współpracę z programami z innych dziedzin (takich jak szkoła medyczna uniwersytetu lub inne wydziały inżynieryjne), ponownie ze względu na interdyscyplinarny charakter BME. MS i doktorat programy zazwyczaj wymagają od kandydatów posiadania tytułu licencjata w BME lub dyscyplinie inżynierskiej (plus niektóre zajęcia z nauk przyrodniczych) lub nauk przyrodniczych (plus niektóre zajęcia z inżynierii).
Edukacja w BME jest również bardzo zróżnicowana na całym świecie. Dzięki rozległemu sektorowi biotechnologii, licznym głównym uniwersytetom i stosunkowo niewielkiej liczbie barier wewnętrznych Stany Zjednoczone poczyniły znaczne postępy w rozwoju możliwości edukacyjnych i szkoleniowych BME. Europa, która ma również duży sektor biotechnologii i imponujący system edukacji, napotkała trudności w tworzeniu jednolitych standardów, ponieważ wspólnota europejska próbuje zastąpić niektóre z krajowych barier jurysdykcyjnych, które wciąż istnieją. Niedawno pojawiły się inicjatywy, takie jak BIOMEDEA, mające na celu opracowanie standardów edukacyjnych i zawodowych związanych z BME. Inne kraje, takie jak Australia, dostrzegają braki w edukacji BME i dążą do ich naprawienia. Ponadto, ponieważ dążenia do wysokich technologii są zwykle cechą krajów rozwiniętych, niektóre obszary świata mają tendencję do wolniejszego rozwoju edukacji, w tym BME.
Licencja/certyfikacja
Podobnie jak w przypadku innych zawodów wyuczonych, każdy stan ma pewne (dość podobne) wymagania, aby uzyskać licencję zarejestrowanego profesjonalnego inżyniera (PE), ale w USA w przemyśle taka licencja nie jest wymagana, aby być pracownikiem inżyniera w większości sytuacji (ze względu na wyjątek znany jako zwolnienie przemysłowe, które faktycznie dotyczy zdecydowanej większości amerykańskich inżynierów). Model amerykański na ogół wymagał od praktykujących inżynierów oferujących usługi inżynieryjne, które mają wpływ na dobro publiczne, bezpieczeństwo, ochronę życia, zdrowia lub mienia, posiadania licencji, podczas gdy inżynierowie pracujący w sektorze prywatnym bez bezpośredniego oferowania usług inżynieryjnych na rzecz publiczne lub inne przedsiębiorstwa, edukacja i rząd nie muszą mieć licencji. W szczególności nie ma to miejsca w wielu innych krajach, w których licencja jest prawnie niezbędna do wykonywania zawodu inżyniera, podobnie jak w przypadku prawa lub medycyny.
Inżynieria biomedyczna jest regulowana w niektórych krajach, takich jak Australia, ale rejestracja jest zwykle zalecana i nie jest wymagana.
W Wielkiej Brytanii inżynierowie mechanicy pracujący w obszarach inżynierii medycznej, bioinżynierii lub inżynierii biomedycznej mogą uzyskać status dyplomowanego inżyniera za pośrednictwem Institution of Mechanical Engineers . W Instytucie działa również Zakład Inżynierii w Medycynie i Zdrowiu. Instytut Fizyki i Inżynierii w Medycynie (IPEM) posiada panel do akredytacji kursów magisterskich z inżynierii biomedycznej, a status Chartered Engineering można również uzyskać za pośrednictwem IPEM.
Egzamin z podstaw inżynierii – pierwszy (i bardziej ogólny) z dwóch egzaminów licencyjnych w większości jurysdykcji w USA – obejmuje teraz biologię (chociaż technicznie nie BME). W przypadku drugiego egzaminu, zwanego Zasadami i praktykami, część 2 lub egzaminu z inżynierii zawodowej, kandydaci mogą wybrać treść określonej dyscypliny inżynierskiej, z której mają być testowani; obecnie nie ma takiej opcji dla BME, co oznacza, że każdy inżynier biomedyczny ubiegający się o licencję musi przygotować się do zdania tego egzaminu w innej kategorii (co nie ma wpływu na faktyczną licencję, ponieważ większość jurysdykcji i tak nie uznaje specjalizacji dyscyplinarnych). Jednak Towarzystwo Inżynierii Biomedycznej (BMES) od 2009 r. Bada możliwość wdrożenia wersji tego egzaminu specyficznej dla BME, aby ułatwić inżynierom biomedycznym uzyskanie licencji.
Poza rejestracją rządową niektóre organizacje zawodowe/przemysłowe sektora prywatnego oferują również certyfikaty o różnym stopniu ważności. Jednym z takich przykładów jest certyfikat Certified Clinical Engineer (CCE) dla inżynierów klinicznych.
Perspektywy rozwoju kariery
W 2012 r. W Stanach Zjednoczonych zatrudnionych było około 19 400 inżynierów biomedycznych, a przewidywano, że w latach 2012–2022 dziedzina ta wzrośnie o 5% (szybciej niż średnia). Inżynieria biomedyczna ma najwyższy odsetek kobiet inżynierów w porównaniu z innymi powszechnymi zawodami inżynierskimi.
Godne uwagi postacie
- Julia Tutelman Apter (nie żyje) - Jeden z pierwszych specjalistów w dziedzinie badań neurofizjologicznych i członek-założyciel Towarzystwa Inżynierii Biomedycznej
- Earl Bakken (nie żyje) – wynalazł pierwszy tranzystorowy rozrusznik serca, współzałożyciel firmy Medtronic .
- Forrest Bird (nie żyje) – lotnik i pionier w wynalezieniu wentylatorów mechanicznych
- YC Fung (nie żyje) – emerytowany profesor Uniwersytetu Kalifornijskiego w San Diego , przez wielu uważany za twórcę współczesnej biomechaniki
- Leslie Geddes (zmarły) – emerytowany profesor Uniwersytetu Purdue , inżynier elektryk, wynalazca i wychowawca ponad 2000 inżynierów biomedycznych, otrzymał w 2006 r . National Medal of Technology z rąk prezydenta George’a Busha za ponad 50 lat wkładu, który zaowocował innowacjami w zakresie od leczenia oparzeń po miniaturowe defibrylatory, naprawę więzadeł po małe ciśnieniomierze dla wcześniaków, a także nową metodę wykonywania resuscytacji krążeniowo-oddechowej (CPR).
- Willem Johan Kolff (nie żyje) – pionier hemodializy oraz w dziedzinie sztucznych narządów
- Robert Langer – profesor Instytutu MIT , prowadzi największe laboratorium BME na świecie, pionier w dostarczaniu leków i inżynierii tkankowej
- John Macleod (nie żyje) – jeden ze współodkrywców insuliny na Case Western Reserve University .
- Alfred E. Mann – Fizyk, przedsiębiorca i filantrop. Pionier w dziedzinie inżynierii biomedycznej.
- J. Thomas Mortimer – emerytowany profesor inżynierii biomedycznej na Uniwersytecie Case Western Reserve. Pionier funkcjonalnej stymulacji elektrycznej (FES)
- Robert M. Nerem – emerytowany profesor Georgia Institute of Technology . Pionier w dziedzinie tkanek regeneracyjnych, biomechaniki i autor ponad 300 opublikowanych prac. Jego prace były cytowane łącznie ponad 20 000 razy.
- P. Hunter Peckham – Donnell profesor inżynierii biomedycznej i ortopedii na Case Western Reserve University. Pionier funkcjonalnej stymulacji elektrycznej (FES)
- Nicholas A. Peppas – profesor inżynierii na University of Texas w Austin , pionier w dostarczaniu leków , biomateriałach , hydrożelach i nanobiotechnologii .
- Robert Plonsey – emerytowany profesor Duke University , pionier elektrofizjologii
- Otto Schmitt (nie żyje) - biofizyk ze znaczącym wkładem w BME, zajmujący się biomimetyką
- Ascher Shapiro (nie żyje) – profesor instytutu MIT, przyczynił się do rozwoju dziedziny BME, urządzeń medycznych (np. balonów wewnątrzaortalnych)
- Gordana Vunjak-Novakovic – profesor uniwersytecki na Uniwersytecie Columbia , pionier inżynierii tkankowej i projektowania bioreaktorów
- John G. Webster – emerytowany profesor na Uniwersytecie Wisconsin-Madison , pionier w dziedzinie wzmacniaczy oprzyrządowania do rejestracji sygnałów elektrofizjologicznych
- Fred Weibell , współautor książki Biomedical Instrumentation and Measurements
- UA Whitaker (zmarły) – fundator Fundacji Whitaker , która wspierała badania i edukację w BME, przekazując ponad 700 milionów dolarów różnym uniwersytetom, pomagając stworzyć 30 programów BME i pomagając sfinansować budowę 13 budynków
Zobacz też
- Biomedycyna — gałąź nauk medycznych, która stosuje zasady biologiczne i fizjologiczne w praktyce klinicznej
- Kardiofizyka – interdyscyplinarna nauka stojąca na styku kardiologii i fizyki medycznej
- Anatomia obliczeniowa – Interdyscyplinarna dziedzina biologii
- Fizyka medyczna - Zastosowanie koncepcji, teorii i metod fizycznych w medycynie lub opiece zdrowotnej
- Fizjom
- Program inżynierii biomedycznej i oprzyrządowania (BEIP)
Dalsza lektura
- Bronzino, Joseph D. (kwiecień 2006). Podręcznik inżynierii biomedycznej (wyd. Trzecie). [CRC Naciśnij]. ISBN 978-0-8493-2124-5 . Zarchiwizowane od oryginału w dniu 2015-02-24 . Źródło 2009-06-22 .
- Villafane, Carlos (czerwiec 2009). Biomed: z perspektywy studenta (wyd. Pierwsze). [przyjaciele techników.com]. ISBN 978-1-61539-663-4 .
Linki zewnętrzne
-
 Media związane z inżynierią biomedyczną w Wikimedia Commons
Media związane z inżynierią biomedyczną w Wikimedia Commons - Inżynierii Biomedycznej w Curlie