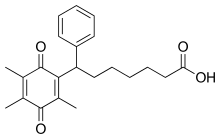
Seratrodast
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Bronica w Japonii, Changnuo, Mai Xu Jia, Quan Kang Nuo w Chinach oraz jako Seradair w Indiach. . |
| AHFS / Drugs.com | Międzynarodowe nazwy leków |
Drogi podawania |
Doustnie ( tabletki , granulki) |
| Kod ATC | |
| Status prawny | |
| Status prawny |
|
| Dane farmakokinetyczne | |
| Wiązanie białek | >96% |
| Okres półtrwania w fazie eliminacji | 22 godziny |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| ChemSpider | |
| UNII | |
| KEGG | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA | 100.220.176 |
| Dane chemiczne i fizyczne | |
| Formuła | C22H26O4 _ _ _ _ _ |
| Masa cząsteczkowa | 354,446 g · mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
Seratrodast (nazwa rozwojowa, AA-2414; pierwotnie sprzedawany jako Bronica ) jest antagonistą receptora tromboksanu A2 ( TXA2 ) (receptor TP) stosowanym głównie w leczeniu astmy . Był to pierwszy antagonista receptora TP, który został opracowany jako lek przeciwastmatyczny i został dopuszczony do obrotu w Japonii w 1997 roku. Od 2017 roku seratrodast był sprzedawany jako Bronica w Japonii oraz jako Changnuo, Mai Xu Jia, Quan Kang Nuo w Chinach.
W przeciwieństwie do inhibitorów syntazy tromboksanu, takich jak ozagrel , seratrodast nie wpływa na powstawanie skrzepliny , czas do okluzji i czas krwawienia . Seratrodast nie ma wpływu na czas protrombinowy i czas częściowej tromboplastyny po aktywacji , co wyklucza jakikolwiek wpływ na kaskadę krzepnięcia krwi .
Zastosowania medyczne
Seratrodast jest stosowany w leczeniu astmy.
Nie ma odpowiednich i dobrze kontrolowanych badań seratrodastu u kobiet w ciąży. Lek należy stosować w ciąży tylko wtedy, gdy potencjalne korzyści przewyższają ryzyko dla płodu. Seratrodastu nie należy stosować w okresie laktacji.
Nie ustalono bezpieczeństwa i skuteczności seratrodastu u dzieci (<18 lat).
Przeciwwskazania i interakcje
Seratrodastu nie należy stosować u osób z chorobami wątroby.
Stosowanie z paracetamolem lub antybiotykami cefemowymi zwiększa ryzyko uszkodzenia wątroby. Stosowanie z aspiryną zwiększa biodostępność seratrodastu.
Niekorzystne skutki
Do najczęściej obserwowanych działań niepożądanych (od 0,1 do 5%) należą podwyższona aktywność aminotransferaz , nudności, utrata apetytu, dyskomfort w żołądku, ból brzucha, biegunka, zaparcia, suchość w ustach, zaburzenia smaku, senność, ból głowy, zawroty głowy, kołatanie serca i złe samopoczucie. U mniej niż 0,1% pacjentów wystąpiły wymioty, małopłytkowość, krwawienie z nosa, skłonność do krwawień, bezsenność, drżenie, drętwienie, uderzenia gorąca i obrzęki. Wszystkie zgłaszane działania niepożądane miały nasilenie od łagodnego do umiarkowanego i ustępowały po odstawieniu leku.
Farmakologia
Tromboksan A2 (TXA 2 ) jest generowany w płucach osób chorych na astmę, a kiedy przekazuje sygnał przez receptor tromboksanu, powoduje skurcz oskrzeli , skurcz naczyń , wydzielanie śluzu i nadreaktywność dróg oddechowych . Seratrodast hamuje aktywność receptora tromboksanu , blokując działanie TXA 2 .
Farmakokinetyka
Farmakokinetykę seratrodastu badano u zdrowych ochotników z Japonii i rasy kaukaskiej, w tym z Indii. Stężenie seratrodastu w osoczu zwiększa się wraz ze wzrostem dawki. Wchłanianie seratrodastu jest stosunkowo szybkie, a maksymalne stężenie w osoczu wynosi 4,6–6 μg/ml i osiągane jest w ciągu 3 do 4 godzin. Stężenie seratrodastu w osoczu w stanie stacjonarnym jest osiągane w ciągu 4-5 dni. Seratrodast jest powoli usuwany, głównie w wyniku biotransformacji w wątrobie. Lek wykazuje dwuwykładniczy rozkład profili w osoczu ze średnim okresem półtrwania w fazie eliminacji wynoszącym 22 godziny. Około 20% podanej dawki jest wydalane z moczem, z czego 60% w postaci koniugatów
Chemia
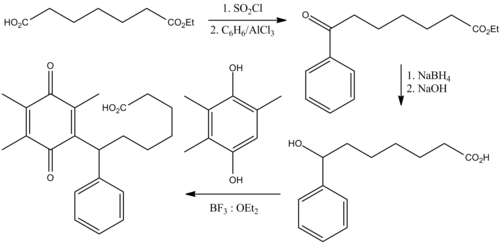
Seratrodast można przygotować w pięciu etapach, zaczynając od monoestru kwasu pimelinowego .
Historia
Seratrodast był pierwszym antagonistą receptora tromboksanu , który pojawił się na rynku jako lek na astmę; został zatwierdzony w Japonii w 1997 roku.
Społeczeństwo i kultura
Od 2017 roku seratrodast był sprzedawany jako Bronica w Japonii, Changnuo, Mai Xu Jia, Quan Kang Nuo w Chinach oraz jako Seretra & Seradair w Indiach.
Badania
Seratrodast badano w całorocznym alergicznym zapaleniu błony śluzowej nosa , przewlekłym zapaleniu oskrzeli i przewlekłej rozedmie płuc, ale około 2000 r. zaniechano wysiłków zmierzających do wprowadzenia leku na rynek w tych wskazaniach.