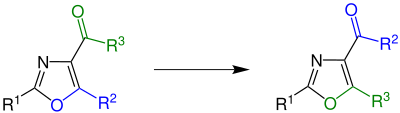
Przegrupowanie Cornfortha
W chemii organicznej przegrupowanie Cornfortha jest reakcją przegrupowania 4-acyloksazolu, w której grupa przyłączona do acylu w pozycji 4 i podstawnik w pozycji 5 pierścienia oksazolu zamieniają się miejscami. Po raz pierwszy został zgłoszony w 1949 roku i został nazwany na cześć Johna Cornfortha . Reakcja jest wykorzystywana w syntezie aminokwasów, gdzie jako związki pośrednie występują odpowiednie oksazole.
Przegląd
W oryginalnej pracy Cornforth użył 5-etoksy-2-fenylooksazolo-4-karboksyamidu (R1 = fenyl , R2 = etoksyl , R3 = amino ) .
Reakcja działa jednak również z dużą liczbą innych 1,3-oksazoli podstawionych karbonylem.
Michael Dewar dalej badał reakcję . Wykazano, że reakcja dawała dobre wydajności, powyżej 90%, gdy stosowano heterocykle zawierające azot w pozycji R3 .
Mechanizm
Mechanizm przegrupowania Cornfortha zaczyna się od termicznego pericyklicznego otwarcia pierścienia, które dostarcza nitrylowego związku pośredniego 1 , który następnie ulega przegrupowaniu do oksazolu, który jest izomerem w stosunku do związku wyjściowego.
Pośredni ylid ma kilka czynników rezonansowych, a stabilność wspomnianych struktur wpływa na wynik reakcji, ponieważ półprodukt powróci do materiału wyjściowego, jeśli trzecia struktura rezonansowa jest najbardziej stabilna. [ Potrzebne źródło ] To, czy reakcja zachodzi, zależy od różnicy energii między materiałem wyjściowym a produktem.