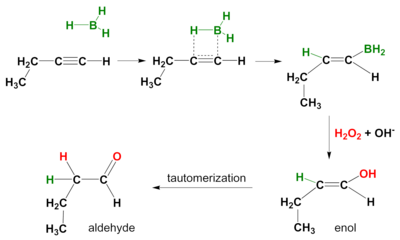
Reakcja hydroborowania – utleniania
Reakcja hydroborowania-utleniania jest dwuetapową reakcją hydratacji , która przekształca alken w alkohol . Proces ten prowadzi do syn addycji wodoru i grupy hydroksylowej w miejscu, w którym znajdowało się wiązanie podwójne . Hydroborowanie-utlenianie jest reakcją anty-Markownikowa , w której grupa hydroksylowa przyłącza się do mniej podstawionego węgla. W ten sposób reakcja zapewnia bardziej stereospecyficzny i komplementarny regiochemię alternatywa dla innych reakcji hydratacji, takich jak addycja katalizowana kwasem i proces oksyrtęciowo-redukcyjny . Reakcja została po raz pierwszy opisana przez Herberta C. Browna pod koniec lat pięćdziesiątych i została uznana za przyznanie mu Nagrody Nobla w dziedzinie chemii w 1979 roku.
Ogólna postać reakcji jest następująca:
Tetrahydrofuran (THF) jest archetypowym rozpuszczalnikiem stosowanym do hydroborowania.
Mechanizm i zakres
Etap hydroborowania
W pierwszym etapie boran (BH 3 ) przyłącza się do wiązania podwójnego , przenosząc jeden z atomów wodoru na atom węgla sąsiadujący z tym, który zostaje związany z borem . To hydroborowanie powtarza się jeszcze dwa razy, kolejno poddając reakcji każde wiązanie B–H, tak że do każdego BH 3 przyłączają się trzy alkeny . Powstały trialkiloboran traktuje się nadtlenkiem wodoru w drugim etapie. Proces ten zastępuje wiązania BC wiązaniami HO-C. Odczynnik borowy jest przekształcany w kwas borowy . Reakcja została pierwotnie opisana przez HC Brown w 1957 r. za przekształcenie 1-heksenu w 1-heksanol .
Wiedząc, że grupa zawierająca bor zostanie zastąpiona grupą hydroksylową, można zauważyć, że początkowy etap hydroborowania determinuje regioselektywność. Hydroborowanie przebiega w antymarkownikowski . Sekwencja reakcji jest również stereospecyficzna , dając dodatek syn (po tej samej stronie alkenu): hydroborowanie jest syn-selektywne, a utlenianie zastępuje bor grupą hydroksylową o tej samej pozycji geometrycznej. Zatem 1-metylocyklopenten reaguje z diboranem głównie z wytworzeniem trans -1-hydroksy-2-metylocyklopentanu - nowo dodany H i OH są cis do siebie.
Dopóki wszystkie atomy wodoru przyłączone do boru nie zostaną przeniesione, grupa borowa BH 2 będzie dodawać do kolejnych alkenów. Oznacza to, że jeden mol borowodoru przejdzie reakcję z trzema molami alkenu. Ponadto nie jest konieczne, aby wodoroboran zawierał więcej niż jeden wodór. Na przykład powszechnie stosuje się odczynniki typu R2BH , gdzie R może oznaczać pozostałą część cząsteczki. Takie zmodyfikowane reagenty hydroborujące obejmują 9-BBN , katecholoboran i disiamyloboran .
Etap utleniania
W drugim etapie sekwencji reakcji nukleofilowy anion wodoronadtlenkowy atakuje atom boru. Migracja alkilu do tlenu daje boran alkilowy z zachowaniem stereochemii (w rzeczywistości reakcja zachodzi poprzez boran trialkilu B(OR) 3 , a nie przez ester monoalkiloborowy BH 2 OR).
Atom „H” w reakcji pochodzi z B 2 H 6 , atom „O” pochodzi z nadtlenku wodoru (H 2 O 2 ), podczas gdy atom „H” związany z atomem O pochodzi z rozpuszczalnika (patrz mechanizm).
Hydroborowanie alkinów
Reakcja hydroborowania zachodzi również na alkinach . Ponownie sposób działania to syn , a produktami reakcji wtórnej są aldehydy z końcowych alkinów i ketony z wewnętrznych alkinów. Aby zapobiec hydroborowaniu w obu wiązaniach pi, stosuje się masywny boran, taki jak disiamylo (di-sec-izo-amylo) boran .
Alternatywne utlenianie
Zastosowanie innych utleniaczy zamiast nadtlenku wodoru może prowadzić do produktów karbonylowych, a nie alkoholi z alkenów. N -tlenek N - metylomorfoliny z katalitycznym nadrutenianem tetrapropyloamoniowym przekształca alkiloboran w karbonyl, a więc produkt ketonowy lub aldehydowy , w zależności od tego, jakie inne grupy były przyłączone do tego węgla w oryginalnym alkenie. Różne dichromiany lub pokrewne odczynniki chromu (VI) również dają ketony, ale dają kwasy karboksylowe zamiast aldehydów dla końcowych alkenów.
Linki zewnętrzne
- Portal chemii organicznej. Hydroborowanie (w tym najnowsza literatura). https://www.organic-chemistry.org/namedreactions/brown-hydroboration.shtm