Toksyna botulinowa
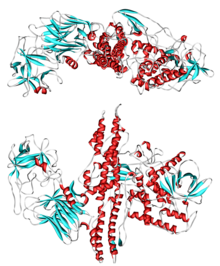
Diagram wstążkowy trzeciorzędowej struktury BotA (). wpis WPB .
| |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Botox, Myobloc, Jeuveau i inne |
| Inne nazwy | BoNT, abobotulinumtoxinA, daxibotulinumtoxinA, daxibotulinumtoxinA-lanm, evabotulinumtoxinA, incobotulinumtoxinA, letibotulinumtoxinA, onabotulinumtoxinA, prabotulinumtoxinA, relabotulinumtoxinA, rimabotulinumtoxinB |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a619021 |
| Dane licencyjne | |
| Kategoria ciąży |
|
Drogi podawania |
Domięśniowo , podskórnie , śródskórnie |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Identyfikatory | |
| Numer CAS | |
| Bank Leków | |
| ChemSpider |
|
| UNII |
|
| KEGG | |
| Karta informacyjna ECHA | 100.088.372 |
| Dane chemiczne i fizyczne | |
| Formuła | C 6760 H 10447 N 1743 O 2010 S 32 |
| Masa cząsteczkowa | 149 323,05 g ·mol -1 |
|
| |
| Identyfikatory | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| bontoksylizyny | |||||||||
| nr WE | 3.4.24.69 | ||||||||
| Bazy danych | |||||||||
| IntEnz | Widok IntEnz | ||||||||
| BRENDA | Wpis BRENDY | ||||||||
| ExPASy | Widok NiceZyme | ||||||||
| KEGG | Wpis KEGG | ||||||||
| MetaCyc | szlak metaboliczny | ||||||||
| PRYM | profil | ||||||||
| Struktury PDB | RCSB PDB PDBe PDB suma | ||||||||
| Ontologia genów | AmiGO / QuickGO | ||||||||
| |||||||||
Toksyna botulinowa lub neurotoksyna botulinowa ( BoNT ) to neurotoksyczne białko wytwarzane przez bakterie Clostridium botulinum i gatunki pokrewne. Zapobiega uwalnianiu neuroprzekaźnika acetylocholiny z zakończeń aksonów na złączu nerwowo-mięśniowym , powodując w ten sposób porażenie wiotkie . Toksyna powoduje chorobę zatrucia jadem kiełbasianym . Toksyna jest również wykorzystywana komercyjnie do celów medycznych i kosmetycznych.
Siedem głównych typów toksyny botulinowej to typy od A do G (A, B, C1, C2, D, E, F i G). Sporadycznie pojawiają się nowe typy. Typy A i B mogą powodować choroby u ludzi i są również wykorzystywane komercyjnie i medycznie. Typy C – G są mniej powszechne; typy E i F mogą powodować choroby u ludzi, podczas gdy inne typy powodują choroby u innych zwierząt.
Toksyny botulinowe należą do najsilniejszych znanych toksyn. Zatrucie może wystąpić naturalnie w wyniku infekcji rany lub jelit lub w wyniku spożycia utworzonej toksyny w pożywieniu. Szacunkowa śmiertelna dawka toksyny typu A dla człowieka wynosi 1,3-2,1 ng /kg dożylnie lub domięśniowo , 10-13 ng/kg przy inhalacji lub 1000 ng/kg przy podawaniu doustnym. Formy handlowe są sprzedawane pod markami Botox (onabotulinumtoxinA), Dysport / Azzalure (abobotulinumtoxinA), Letybo (letibotulinumtoxinA), Myobloc (rimabotulinumtoxinB), Xeomin / Bocouture (incobotulinumtoxinA) i Jeuveau (prabotulinumtoxinA).
Zastosowania medyczne
Toksyna botulinowa jest stosowana w leczeniu wielu wskazań terapeutycznych, z których wiele nie jest częścią zatwierdzonej etykiety leku.
Spastyczność mięśni
Toksyna botulinowa jest stosowana w leczeniu wielu zaburzeń charakteryzujących się nadmierną ruchomością mięśni, w tym mózgowym porażeniem dziecięcym , spastycznością poudarową, spastycznością po urazie rdzenia kręgowego, skurczami głowy i szyi, powiek , pochwy , kończyn, szczęki i strun głosowych . Podobnie toksyna botulinowa stosowana jest w celu rozluźnienia skurczu mięśni, w tym mięśni przełyku , szczęki , dolnych dróg moczowych i pęcherza moczowego, czy też skurczu odbytu, który może pogłębiać szczelinę odbytu . Wydaje się, że toksyna botulinowa jest skuteczna w leczeniu opornego na leczenie pęcherza nadreaktywnego .
Inne zaburzenia mięśni
Zez , inaczej znany jako nieprawidłowe ustawienie oczu, jest spowodowany brakiem równowagi w działaniu mięśni obracających oczy. Ten stan można czasami złagodzić poprzez osłabienie mięśnia, który ciągnie zbyt mocno lub pociąga za mięsień, który został osłabiony przez chorobę lub uraz. Mięśnie osłabione przez wstrzyknięcie toksyny regenerują się po paraliżu po kilku miesiącach, więc wydaje się, że zastrzyk trzeba powtórzyć, ale mięśnie dostosowują się do długości, przy której są chronicznie trzymane, więc jeśli sparaliżowany mięsień jest rozciągany przez swojego antagonistę, rośnie dłużej , podczas gdy antagonista skraca, dając trwały efekt. Jeśli widzenie obuoczne jest dobre, mózgowy mechanizm fuzji motorycznej, który ustawia oczy na celu widocznym dla obu oczu, może ustabilizować skorygowane ustawienie.
W styczniu 2014 roku toksyna botulinowa została zatwierdzona przez brytyjską Agencję Regulacyjną ds. Leków i Produktów Opieki Zdrowotnej do leczenia ograniczonego ruchu kostki spowodowanego spastycznością kończyn dolnych związaną z udarem u dorosłych.
W lipcu 2016 roku amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła abobotulinumtoxin A (Dysport) do wstrzykiwań w leczeniu spastyczności kończyn dolnych u dzieci w wieku od dwóch lat. AbobotulinumtoxinA to pierwsza i jedyna toksyna botulinowa zatwierdzona przez FDA do leczenia spastyczności kończyn dolnych u dzieci. W Stanach Zjednoczonych FDA zatwierdza tekst etykiet leków na receptę oraz warunki medyczne, które producent leku może sprzedawać. Jednak lekarze przepisujący leki mogą je swobodnie przepisywać na dowolne warunki, znane również jako stosowanie poza wskazaniami . Toksyny botulinowe były stosowane niezgodnie z zaleceniami w przypadku kilku schorzeń pediatrycznych, w tym esotropii dziecięcej .
Nadmierne pocenie
AbobotulinumtoxinA została zatwierdzona do leczenia nadmiernej potliwości pod pachami o nieznanej przyczynie , której nie można opanować środkami miejscowymi.
Migrena
W 2010 roku FDA zatwierdziła domięśniowe wstrzyknięcia toksyny botulinowej do profilaktycznego leczenia przewlekłego migrenowego bólu głowy .
Wskazania kosmetyczne
W zastosowaniach kosmetycznych toksyna botulinowa jest uważana za stosunkowo bezpieczną i skuteczną w redukcji zmarszczek na twarzy , zwłaszcza w górnej jednej trzeciej części twarzy. Formy handlowe są sprzedawane pod markami Botox Cosmetic/Vistabel firmy Allergan , Dysport/Azzalure firmy Galderma i Ipsen , Xeomin/Bocouture firmy Merz, Jeuveau/Nuceiva firmy Evolus, produkowane przez firmę Daewoong w Korei Południowej. Efekty wstrzyknięć toksyny botulinowej w przypadku zmarszczek gładzizny czoła („zmarszczek 11” między oczami) zwykle utrzymują się od dwóch do czterech miesięcy, aw niektórych przypadkach zależą od produktu, przy czym u niektórych pacjentów efekt utrzymuje się dłużej, do 6 miesięcy lub dłużej. Wstrzyknięcie toksyny botulinowej w mięśnie pod zmarszczkami mimicznym powoduje rozluźnienie tych mięśni, co skutkuje wygładzeniem pokrywającej je skóry. Wygładzenie zmarszczek jest zwykle widoczne od trzech do pięciu dni po wstrzyknięciu, z maksymalnym efektem typowo po tygodniu od wstrzyknięcia. Mięśnie można leczyć wielokrotnie, aby zachować wygładzony wygląd.
DaxibotulinumtoxinA (Daxxify) służy do tymczasowej poprawy wyglądu umiarkowanych do ciężkich zmarszczek gładzizny czoła (brwi). DaxibotulinumtoxinA jest inhibitorem uwalniania acetylocholiny i środkiem blokującym przewodnictwo nerwowo-mięśniowe.
Inny
Toksyna botulinowa jest również stosowana w leczeniu zaburzeń nerwów nadpobudliwych, w tym nadmiernej potliwości, bólu neuropatycznego i niektórych objawów alergii . Oprócz tych zastosowań toksyna botulinowa jest oceniana pod kątem zastosowania w leczeniu przewlekłego bólu . Badania pokazują, że toksyna botulinowa może być wstrzykiwana w artretyczne stawy barkowe w celu zmniejszenia przewlekłego bólu i poprawy zakresu ruchu. Stosowanie toksyny botulinowej typu A u dzieci z mózgowym porażeniem dziecięcym jest bezpieczne w mięśniach kończyn górnych i dolnych.
Skutki uboczne
Chociaż toksyna botulinowa jest ogólnie uważana za bezpieczną w warunkach klinicznych, mogą wystąpić poważne skutki uboczne jej stosowania. Najczęściej toksyna botulinowa może zostać wstrzyknięta w niewłaściwą grupę mięśniową lub rozłożona w czasie od miejsca wstrzyknięcia, powodując czasowy paraliż niezamierzonych mięśni.
Skutki uboczne stosowania kosmetyków zazwyczaj wynikają z niezamierzonego paraliżu mięśni twarzy. Należą do nich częściowy paraliż twarzy, osłabienie mięśni i problemy z połykaniem . Skutki uboczne nie ograniczają się jednak do bezpośredniego paraliżu i mogą również obejmować bóle głowy, objawy grypopodobne i reakcje alergiczne. Tak jak zabiegi kosmetyczne trwają tylko kilka miesięcy, skutki uboczne paraliżu mogą trwać tak samo. Przynajmniej w niektórych przypadkach efekty te ustępują w ciągu kilku tygodni po leczeniu. Zasinienie w miejscu wstrzyknięcia nie jest skutkiem ubocznym toksyny, ale raczej sposobem podania i zgłasza się, że można temu zapobiec, jeśli lekarz uciśnie miejsce wstrzyknięcia; kiedy to nastąpi, w określonych przypadkach podaje się, że trwa 7–11 dni. Podczas wstrzykiwania do mięśnia żwacza żuchwy utrata funkcji mięśnia może spowodować utratę lub zmniejszenie zdolności do żucia pokarmów stałych. Przy ciągłym stosowaniu wysokich dawek mięśnie mogą zanikać lub tracić siłę; badania wykazały, że te mięśnie odbudowują się po przerwie w botoksie.
Skutki uboczne stosowania terapeutycznego mogą być znacznie bardziej zróżnicowane w zależności od miejsca wstrzyknięcia i dawki wstrzykniętej toksyny. Ogólnie rzecz biorąc, skutki uboczne stosowania terapeutycznego mogą być poważniejsze niż te, które pojawiają się podczas stosowania kosmetycznego. Mogą one wynikać z paraliżu krytycznych grup mięśni i mogą obejmować arytmię , zawał serca , aw niektórych przypadkach drgawki, zatrzymanie oddechu i śmierć. Dodatkowo, skutki uboczne powszechne w kosmetykach są również powszechne w zastosowaniach terapeutycznych, w tym problemy z połykaniem, osłabienie mięśni, reakcje alergiczne i zespoły grypopodobne.
W odpowiedzi na pojawienie się tych skutków ubocznych, w 2008 roku FDA powiadomiła opinię publiczną o potencjalnych zagrożeniach toksyną botulinową jako środkiem terapeutycznym. Mianowicie, toksyna może rozprzestrzeniać się na obszary odległe od miejsca wstrzyknięcia i paraliżować niezamierzone grupy mięśni, zwłaszcza gdy jest stosowana w leczeniu spastyczności mięśni u dzieci leczonych z powodu mózgowego porażenia dziecięcego. W 2009 roku FDA ogłosiła, że do dostępnych produktów z toksyną botulinową zostaną dodane ostrzeżenia w pudełkach, ostrzegające o ich zdolności do rozprzestrzeniania się z miejsca wstrzyknięcia. Udowodniono jednak, że kliniczne zastosowanie toksyny botulinowej A u dzieci z mózgowym porażeniem dziecięcym jest bezpieczne przy minimalnych skutkach ubocznych. Ponadto FDA ogłosiła zmiany nazw kilku produktów z toksyną botulinową, aby podkreślić, że produkty te nie są wymienne i wymagają różnych dawek do prawidłowego stosowania. Botox i Botox Cosmetic otrzymały ogólną nazwę onabotulinumtoxinA, Myobloc jako rimabotulinumtoxinB, a Dysport zachował swoją ogólną nazwę abobotulinumtoxinA. W związku z tym FDA wydała komunikat dla pracowników służby zdrowia, w którym powtórzyła nazwy nowych leków i zatwierdzone zastosowania każdego z nich. Podobne ostrzeżenie zostało wydane przez Health Canada w 2009 roku, ostrzegając, że produkty zawierające toksynę botulinową mogą rozprzestrzeniać się na inne części ciała.
Rola w chorobie
Toksyna botulinowa wytwarzana przez Clostridium botulinum jest przyczyną zatrucia jadem kiełbasianym. Ludzie najczęściej spożywają toksynę z jedzenia niewłaściwie konserwowanej żywności, w której wyrosła C. botulinum . Jednak toksyna może również zostać wprowadzona przez zakażoną ranę. U niemowląt bakterie mogą czasami rosnąć w jelitach i wytwarzać toksynę botulinową w jelicie, co może powodować stan znany jako zespół wiotkiego dziecka . We wszystkich przypadkach toksyna może następnie rozprzestrzeniać się, blokując nerwy i funkcje mięśni. W ciężkich przypadkach toksyna może blokować nerwy kontrolujące układ oddechowy lub serce, powodując śmierć. Botulizm może być trudny do zdiagnozowania, ponieważ może wyglądać podobnie do chorób, takich jak zespół Guillain-Barré , myasthenia gravis i udar . Inne testy, takie jak skan mózgu i badanie płynu rdzeniowego, mogą pomóc wykluczyć inne przyczyny. Jeśli objawy zatrucia jadem kiełbasianym zostaną wcześnie wykryte, można zastosować różne metody leczenia. W celu usunięcia skażonej żywności, która pozostaje w jelitach, można zastosować lewatywy lub wywołać wymioty. W przypadku infekcji ran zakażony materiał można usunąć chirurgicznie. Antytoksyna botulinowa jest dostępna i może być stosowana w celu zapobiegania pogorszeniu się objawów, chociaż nie odwróci istniejącego uszkodzenia nerwów. W ciężkich przypadkach mechaniczne oddychanie może być stosowane w celu wspomagania pacjentów z niewydolnością oddechową. Uszkodzenie nerwów goi się z czasem, zwykle w ciągu tygodni lub miesięcy. [ nieudana weryfikacja ] Przy odpowiednim leczeniu śmiertelność w przypadku zatrucia jadem kiełbasianym można znacznie zmniejszyć.
Do leczenia zatrucia jadem kiełbasianym dostępne są dwa preparaty antytoksyn botulinowych. Trójwalentna (serotypy A, B, E) antytoksyna botulinowa pochodzi od koni przy użyciu całych przeciwciał . Drugą antytoksyną jest siedmiowartościowa antytoksyna botulinowa (serotypy A, B, C, D, E, F, G), która pochodzi z końskich przeciwciał, które zostały zmienione, aby uczynić je mniej immunogennymi. Ta antytoksyna jest skuteczna przeciwko wszystkim głównym szczepom jadu kiełbasianego.
Mechanizm akcji

Toksyna botulinowa wywiera swoje działanie poprzez rozszczepianie kluczowych białek niezbędnych do aktywacji nerwów. Po pierwsze, toksyna wiąże się specyficznie z presynaptyczną powierzchnią neuronów , które wykorzystują neuroprzekaźnik acetylocholinę . Po związaniu się z zakończeniem nerwowym neuron pobiera toksynę do pęcherzyka przez endocytozę za pośrednictwem receptora . W miarę jak pęcherzyk przemieszcza się dalej w głąb komórki, zakwasza się, aktywując część toksyny, która powoduje, że przechodzi ona przez błonę pęcherzyka do cytoplazmy komórki . Neurotoksyny botulinowe rozpoznają jednocześnie różne klasy receptorów ( gangliozydy , synaptotagminy i SV2 ). Po wejściu do cytoplazmy toksyna rozszczepia białka SNARE (białka pośredniczące w fuzji pęcherzyków z docelowymi przedziałami związanymi z błoną), co oznacza, że pęcherzyki acetylocholiny nie mogą wiązać się z błoną wewnątrzkomórkową, uniemożliwiając komórce uwalnianie pęcherzyków neuroprzekaźnika. To zatrzymuje sygnalizację nerwową, prowadząc do paraliżu.
Sama toksyna jest uwalniana z bakterii jako pojedynczy łańcuch, a następnie zostaje aktywowana po rozcięciu przez własne proteazy. Postać aktywna składa się z dwułańcuchowego białka złożonego z polipeptydu łańcucha ciężkiego o masie cząsteczkowej 100 kDa , połączonego wiązaniem dwusiarczkowym z polipeptydem łańcucha lekkiego o masie 50 kDa. Łańcuch ciężki zawiera domeny o kilku funkcjach; ma domenę odpowiedzialną za specyficzne wiązanie z presynaptycznymi zakończeniami nerwowymi, jak również domenę odpowiedzialną za pośredniczenie w translokacji łańcucha lekkiego do cytoplazmy komórki w miarę zakwaszania wakuoli. Łańcuch lekki jest metaloproteazą cynkową z rodziny M27 i jest aktywną częścią toksyny. Ulega translokacji do cytoplazmy komórki gospodarza, gdzie rozszczepia białko gospodarza SNAP-25 , należące do rodziny białek SNARE, odpowiedzialne za fuzję . Rozszczepiony SNAP-25 nie może pośredniczyć w fuzji pęcherzyków z błoną komórki gospodarza, zapobiegając w ten sposób uwalnianiu neuroprzekaźnika acetylocholiny z zakończeń aksonów. Ta blokada jest powoli odwracana, gdy toksyna traci aktywność, a białka SNARE są powoli regenerowane przez dotkniętą komórkę.
Siedem serotypów toksyn (A – G) jest tradycyjnie rozdzielonych na podstawie ich antygenowości. Mają różne struktury trzeciorzędowe i różnice w sekwencji. Podczas gdy różne typy toksyn atakują wszystkich członków rodziny SNARE, różne typy toksyn atakują różnych członków rodziny SNARE. Serotypy A, B i E powodują zatrucie jadem kiełbasianym u ludzi, przy czym aktywność typów A i B trwa najdłużej in vivo (od kilku tygodni do miesięcy). Istniejące typy toksyn mogą rekombinować, tworząc typy „hybrydowe” (mozaikowe, chimeryczne). Przykłady obejmują BoNT/CD, BoNT/DC i BoNT/FA, przy czym pierwsza litera wskazuje typ łańcucha lekkiego, a druga wskazuje typ łańcucha ciężkiego. BoNT/FA zyskało znaczną uwagę pod nazwą „BoNT/H”, ponieważ błędnie sądzono, że nie może zostać zneutralizowany przez żadną istniejącą antytoksynę.
Toksyny botulinowe są blisko spokrewnione z toksyną tężcową ; oba są wspólnie znane jako neurotoksyny Clostridium, a lekki łańcuch jest klasyfikowany przez MEROPS jako rodzina M27 . Typy nieklasyczne obejmują BoNT/X (), który jest toksyczny u myszy i prawdopodobnie u ludzi; a BoNT/J() znalezione w krowim Enterococcus ; oraz BoNT/Wo () znalezione w kolonizującej ryż Weissella oryzae .
Historia
Wstępne opisy i odkrycie Clostridium botulinum
Jedno z najwcześniej zarejestrowanych ognisk zatrucia jadem kiełbasianym miało miejsce w 1793 roku w wiosce Wildbad w dzisiejszej Badenii-Wirtembergii w Niemczech. Trzynaście osób zachorowało, a sześć zmarło po zjedzeniu żołądków wieprzowych wypełnionych kaszanką , lokalnym przysmakiem. Dodatkowe przypadki śmiertelnych zatruć pokarmowych w Wirtembergii skłoniły władze do wydania publicznego ostrzeżenia przed spożywaniem wędzonych kaszanek w 1802 r. I zebrania opisów przypadków „zatrucia kiełbasą”. W latach 1817-1822 niemiecki lekarz Justinus Kerner opublikował pierwszy pełny opis objawów zatrucia jadem kiełbasianym, oparty na szeroko zakrojonych obserwacjach klinicznych i doświadczeniach na zwierzętach. Doszedł do wniosku, że toksyna rozwija się w zepsutych kiełbasach w warunkach beztlenowych, jest substancją biologiczną, działa na układ nerwowy i już w niewielkich ilościach jest śmiertelna. Kerner postawił hipotezę, że ta „toksyna kiełbasiana” może być stosowana w leczeniu różnych chorób spowodowanych nadmierną aktywnością układu nerwowego, co czyni go pierwszym, który zasugerował, że można ją stosować terapeutycznie. W 1870 roku niemiecki lekarz Müller ukuł termin „zatrucie jadem kiełbasianym”, aby opisać chorobę spowodowaną zatruciem kiełbasą, od łacińskiego słowa botulus oznaczającego „kiełbasę”.
W 1895 roku belgijski mikrobiolog Émile van Ermengem odkrył to, co obecnie nazywa się Clostridium botulinum i potwierdził, że toksyna wytwarzana przez bakterie powoduje zatrucie jadem kiełbasianym. 14 grudnia 1895 r. W belgijskiej wiosce Ellezelles doszło do dużego wybuchu botulizmu, który miał miejsce podczas pogrzebu, na którym ludzie jedli marynowaną i wędzoną szynkę; trzech z nich zmarło. Badając zanieczyszczoną szynkę i przeprowadzając sekcje zwłok ludzi, którzy zmarli po jej zjedzeniu, van Ermengem wyizolował mikroorganizm beztlenowy, który nazwał Bacillus botulinus . Przeprowadzał również eksperymenty na zwierzętach z ekstraktami z szynki, izolowanymi kulturami bakteryjnymi i ekstraktami toksyn z bakterii. Na tej podstawie wywnioskował, że same bakterie nie powodują zatrucia jadem kiełbasianym przenoszonym przez żywność, ale raczej wytwarzają toksynę, która powoduje chorobę po spożyciu. W wyniku badań Kernera i van Ermengema uznano, że tylko zanieczyszczone mięso lub ryby mogą powodować zatrucie jadem kiełbasianym. Darmstadt w Niemczech wybuchła epidemia botulizmu z powodu białej fasoli w puszkach. W 1910 roku niemiecki mikrobiolog J. Leuchs opublikował artykuł wykazujący, że ogniska w Ellezelles i Darmstadt były spowodowane przez różne szczepy Bacillus botulinus i że toksyny były serologicznie różne. W 1917 Bacillus botulinus został przemianowany na Clostridium botulinum , ponieważ zdecydowano, że termin Bacillus powinien odnosić się tylko do grupy mikroorganizmów tlenowych, podczas gdy Clostridium będzie używany tylko do opisania grupy mikroorganizmów beztlenowych. W 1919 roku Georgina Burke wykorzystała reakcje toksyna-antytoksyna do zidentyfikowania dwóch szczepów Clostridium botulinum , które nazwała A i B.
Konserwowanie żywności
W ciągu następnych trzech dekad, 1895–1925, gdy konserwowanie żywności zbliżało się do przemysłu wartego miliardy dolarów rocznie, zatrucie jadem kiełbasianym stawało się zagrożeniem dla zdrowia publicznego. Karl Friedrich Meyer , szwajcarsko-amerykański naukowiec weterynaryjny, stworzył ośrodek w Fundacji Hoopera w San Francisco, gdzie opracował techniki hodowli organizmu i ekstrakcji toksyny i odwrotnie, zapobiegania wzrostowi organizmu i produkcji toksyny oraz inaktywacji toksyny przez ogrzewanie. W ten sposób zachowano kalifornijski przemysł konserwowy.
II wojna światowa
Wraz z wybuchem II wojny światowej w Fort Detrick w stanie Maryland badano wykorzystanie toksyny botulinowej jako broni. Carl Lamanna i James Duff opracowali techniki koncentracji i krystalizacji, których Edward J. Schantz użył do stworzenia pierwszego produktu klinicznego. Korpus Chemiczny Armii został rozwiązany, Schantz przeniósł się do Instytutu Badań Żywności w Wisconsin, gdzie produkował toksyny do użytku eksperymentalnego i dostarczał je społeczności akademickiej.
Mechanizm działania toksyny botulinowej – blokowania uwalniania neuroprzekaźnika acetylocholiny z zakończeń nerwowych – został wyjaśniony w połowie XX wieku i pozostaje ważnym tematem badawczym. Prawie wszystkie zabiegi toksynami opierają się na tym efekcie w różnych tkankach ciała.
zez
Okuliści specjalizujący się w zaburzeniach mięśni oka ( zez ) opracowali metodę wstrzykiwania pod kontrolą EMG (wykorzystując elektromiogram , sygnał elektryczny z aktywowanego mięśnia do kierowania wstrzyknięciem) środków miejscowo znieczulających jako technikę diagnostyczną do oceny wkładu poszczególnych mięśni w Ruch oczu. Ponieważ operacja zeza często wymagała powtarzania, podjęto poszukiwania niechirurgicznych zabiegów iniekcyjnych z użyciem różnych środków znieczulających, alkoholi, enzymów, blokerów enzymów i neurotoksyn węży. Wreszcie, zainspirowany pracą Daniela B. Drachmana z pisklętami w Johns Hopkins, Alan B. Scott i współpracownicy wstrzyknęli toksynę botulinową do mięśni zewnątrzgałkowych małpy. Wynik był niezwykły; kilka pikogramów wywołało paraliż ograniczony do mięśnia docelowego, długotrwały i bez skutków ubocznych.
Po opracowaniu technik liofilizacji, buforowaniu albuminą i zapewnieniu sterylności, mocy i bezpieczeństwa, Scott złożył wniosek do FDA o eksperymentalne użycie leku i rozpoczął produkcję neurotoksyny botulinowej typu A w swoim laboratorium w San Francisco. W 1977 roku wstrzyknął pierwszym pacjentom ze zezem, opisał jego użyteczność kliniczną w 1980 roku i wkrótce przeszkolił setki okulistów w zakresie wstrzykiwania leku pod kontrolą EMG, który nazwał Oculinum („wyrównywacz oczu”).
W 1986 roku firma Oculinum Inc, mikroproducent i dystrybutor toksyny botulinowej firmy Scott, nie była w stanie uzyskać ubezpieczenia od odpowiedzialności cywilnej za produkt i nie mogła już dostarczać leku. Gdy zapasy się wyczerpały, pacjenci, którzy polegali na okresowych zastrzykach, popadli w desperację. Przez cztery miesiące, gdy kwestie odpowiedzialności zostały rozwiązane, amerykańscy pacjenci z kurczem powiek podróżowali do kanadyjskich ośrodków okulistycznych w celu wykonania zastrzyków.
Na podstawie danych od tysięcy pacjentów zebranych przez 240 badaczy firma Oculinum Inc (która wkrótce została przejęta przez firmę Allergan) otrzymała w 1989 roku zgodę FDA na sprzedaż Oculinum do użytku klinicznego w Stanach Zjednoczonych w leczeniu zeza i kurczu powiek u dorosłych . Allergan zaczął wtedy używać znaku towarowego Botox. Ta pierwotna aprobata została przyznana na mocy amerykańskiej Ustawy o lekach sierocych z 1983 roku .
Kosmetyki
Wpływ toksyny botulinowej typu A na redukcję i likwidację zmarszczek na czole po raz pierwszy opisał i opublikował dr Richard Clark, chirurg plastyczny z Sacramento w Kalifornii. W 1987 roku Clark stanął przed wyzwaniem wyeliminowania oszpecenia spowodowanego funkcjonowaniem tylko prawej strony mięśni czoła po sparaliżowaniu lewej strony czoła podczas zabiegu liftingu twarzy. Ta pacjentka chciała wyglądać lepiej po liftingu, ale doświadczała dziwnego jednostronnego uniesienia brwi prawego czoła, podczas gdy lewa brew opadała, i stale wykazywała głębokie, wyraziste zmarszczki prawego czoła, podczas gdy lewa strona była idealnie gładka z powodu paraliżu. Clark był świadomy, że toksyna botulinowa jest bezpiecznie stosowana w leczeniu dzieci ze zezem i poprosił FDA o zgodę na eksperymentowanie z toksyną botulinową w celu sparaliżowania poruszających się i marszczących się normalnie funkcjonujących mięśni prawego czoła, aby obie strony czoła wyglądały tak samo. To badanie i opis przypadku kosmetycznego zastosowania toksyny botulinowej w leczeniu kosmetycznych komplikacji chirurgii plastycznej było pierwszym doniesieniem dotyczącym specyficznego leczenia zmarszczek i zostało opublikowane w czasopiśmie Chirurgia plastyczna i rekonstrukcyjna w 1989 roku . Amerykańskie Towarzystwo Chirurgów Plastycznych wyraźnie stwierdziło, że „pierwsze opisane użycie toksyny w warunkach estetycznych zostało dokonane przez Clarka i Berrisa w 1989 roku”.
Jean i Alastair Carruthers zaobserwowali, że pacjenci ze skurczem powiek, którzy otrzymali zastrzyki wokół oczu i górnej części twarzy, również cieszyli się zmniejszonymi zmarszczkami gładzizny twarzy („zmarszczkami” między brwiami). Alastair Carruthers poinformował, że inni w tamtym czasie również zauważyli te efekty i omówili kosmetyczny potencjał toksyny botulinowej. W przeciwieństwie do innych badaczy Carrutherowie nie tylko mówili o możliwości kosmetycznego zastosowania toksyny botulinowej. Przeprowadzili badanie kliniczne na normalnych osobach, których jedynym zmartwieniem była bruzda brwi. Przeprowadzili swoje badania w latach 1987-1989 i przedstawili swoje wyniki na dorocznym spotkaniu Amerykańskiego Towarzystwa Chirurgii Dermatologicznej w 1990 roku. Ich odkrycia zostały następnie opublikowane w 1992 roku.
Chroniczny ból
William J. Binder poinformował w 2000 r., że pacjenci, którzy otrzymali zastrzyki kosmetyczne wokół twarzy, zgłaszali ulgę w przewlekłym bólu głowy. Początkowo uważano, że jest to pośredni efekt zmniejszonego napięcia mięśni, ale obecnie wiadomo, że toksyna hamuje uwalnianie obwodowych neuroprzekaźników nocyceptywnych, hamując ośrodkowe systemy przetwarzania bólu odpowiedzialne za migrenowy ból głowy.
Społeczeństwo i kultura
Ekonomia
Według Amerykańskiego Towarzystwa Chirurgów Plastycznych od 2018 roku zastrzyki z toksyny botulinowej są najczęstszą operacją kosmetyczną, z 7,4 milionami zabiegów w Stanach Zjednoczonych . Kwalifikacje do wstrzykiwaczy botoksu różnią się w zależności od hrabstwa, stanu i kraju. Dostawcy kosmetyków Botox to dermatolodzy, chirurdzy plastyczni, lekarze medycyny estetycznej, dentyści, pielęgniarki, pielęgniarki i asystenci lekarzy.
Przewiduje się, że światowy rynek produktów z toksyną botulinową, napędzany ich zastosowaniami kosmetycznymi, osiągnie do 2018 r. ten sam przedział czasowy.
- Rynek USA
- W 2020 roku wykonano 4 401 536 zabiegów z użyciem toksyny botulinowej typu A. W 2019 r. rynek toksyny botulinowej zarobił 3,19 mld USD.
- Koszt botoksu Koszt
- botoksu jest zwykle określany na podstawie liczby podanych jednostek (śr. 10,00–30,00 USD za jednostkę) lub obszaru (200–1000 USD) i zależy od wiedzy lekarza, lokalizacji kliniki, liczby jednostek i złożoności leczenia. [ Potrzebne źródło ]
- Ubezpieczenie
- Botox do celów medycznych jest zwykle objęty ubezpieczeniem, jeśli lekarz uzna to za konieczne z medycznego punktu widzenia, i obejmuje mnóstwo problemów medycznych, w tym pęcherz nadreaktywny (OAB), nietrzymanie moczu z powodu schorzeń neurologicznych, bóle głowy i migreny, staw skroniowo-żuchwowy, spastyczność w dorosłych pacjentów, dystonia szyjna u dorosłych pacjentów, ciężka nadmierna potliwość pach (lub innych okolic ciała), kurcz powiek, spastyczność kończyn górnych lub dolnych.
- Migreny
- W przypadku migrenowych bólów głowy zalecana przez FDA dawka wynosi 155 jednostek i kosztuje od 300 do 600 USD za leczenie z własnej kieszeni, jeśli jest objęte ubezpieczeniem.
- Hyperhidrosis
- Botox na nadmierną potliwość jest zatwierdzony przez FDA.
- Kosmetyczne
- standardowe obszary do wstrzyknięć botoksu estetycznego obejmują twarz i inne obszary, które mogą tworzyć drobne linie i zmarszczki z powodu codziennych skurczów mięśni i / lub mimiki twarzy, takiej jak uśmiechanie się, marszczenie brwi, mrużenie oczu i unoszenie brwi. Obszary te obejmują obszar gładzizny między brwiami, poziome linie na czole, kurze łapki wokół oczu, a nawet okrągłe pasma, które tworzą się wokół szyi wtórnie do nadaktywności platysmy.
Bioterroryzm
Toksyna botulinowa została uznana za potencjalny środek do wykorzystania w bioterroryzmie . Może być wchłaniany przez oczy, błony śluzowe, drogi oddechowe i nieuszkodzoną skórę. Działanie toksyny botulinowej różni się od działania czynników nerwowych tym, że objawy zatrucia jadem kiełbasianym rozwijają się stosunkowo wolno (przez kilka dni), podczas gdy działanie środków nerwowych jest na ogół znacznie szybsze. Dowody sugerują, że ekspozycja nerwów (symulowana przez wstrzyknięcie atropiny i pralidoksymu ) zwiększy śmiertelność poprzez wzmocnienie mechanizmu toksyczności toksyny botulinowej. Jeśli chodzi o wykrywanie, protokoły wykorzystujące NBC (taki jak bibułka M-8 lub ICAM) nie wskażą „pozytywnego”, gdy badane są próbki zawierające toksynę botulinową. Aby potwierdzić diagnozę zatrucia toksyną botulinową, terapeutycznie lub w celu dostarczenia dowodów w dochodzeniach w sprawie śmierci, toksynę botulinową można oznaczyć ilościowo za pomocą testu immunologicznego ludzkich płynów biologicznych; u zatrutych pacjentów wykryto poziomy w surowicy 12–24 mysich jednostek LD50 na mililitr.
Japoński kult zagłady Aum Shinrikyo produkował toksynę botulinową i rozprowadzał ją w postaci aerozolu w centrum Tokio w latach 90., ale ataki nie spowodowały ofiar śmiertelnych.
Na początku lat 80. niemieckie i francuskie gazety donosiły, że policja dokonała nalotu na kryjówkę gangu Baader-Meinhof w Paryżu i znalazła prowizoryczne laboratorium, w którym znajdowały się kolby pełne bakterii Clostridium botulinum , która wytwarza toksynę botulinową. Ich raporty okazały się później błędne; nigdy nie znaleziono takiego laboratorium.
Nazwy marek
Toksyna botulinowa A jest sprzedawana pod markami Jeuveau, Botox i Xeomin. Toksyna botulinowa B jest sprzedawana pod marką Myobloc.
W Stanach Zjednoczonych produkty z toksyną botulinową są wytwarzane przez różne firmy, zarówno do użytku terapeutycznego, jak i kosmetycznego. Amerykański dostawca poinformował w swoich materiałach firmowych w 2011 r., Że może „zaspokajać światowe zapotrzebowanie na 25 wskazań zatwierdzonych przez agencje rządowe na całym świecie” mniej niż jeden gram surowej toksyny botulinowej. Myobloc lub Neurobloc, produkt z toksyną botulinową typu B, jest produkowany przez Solstice Neurosciences, spółkę zależną US WorldMeds. AbobotulinumtoxinA), preparat terapeutyczny toksyny typu A produkowany przez Galderma w Wielkiej Brytanii, jest licencjonowany do leczenia dystonii ogniskowych i niektórych zastosowań kosmetycznych w USA i innych krajach.
Oprócz trzech głównych producentów w USA, znanych jest wielu innych producentów toksyny botulinowej. Xeomin, wyprodukowany w Niemczech przez firmę Merz , jest również dostępny zarówno do użytku terapeutycznego, jak i kosmetycznego w Stanach Zjednoczonych. Instytut Produktów Biologicznych w Lanzhou w Chinach wytwarza produkt z toksyną botulinową typu A; od 2014 r. była to jedyna toksyna botulinowa typu A zatwierdzona w Chinach. Toksyna botulinowa typu A jest również sprzedawana na rynku światowym jako Lantox i Prosigne. Neuronox, produkt z toksyną botulinową typu A, został wprowadzony przez firmę Medy-Tox Inc. z Korei Południowej w 2009 roku.
Produkcja toksyn
Toksyny jadu kiełbasianego są wytwarzane przez bakterie z rodzaju Clostridium, mianowicie C. botulinum , C. butyricum , C. baratii i C. argentinense , które są szeroko rozpowszechnione, w tym w glebie i kurzu. Ponadto bakterie można znaleźć w domach na podłogach, dywanach i blatach, nawet po czyszczeniu. Zatrucie jadem kiełbasianym przenoszone przez żywność wynika pośrednio ze spożycia żywności zanieczyszczonej Clostridium , gdzie ekspozycja na środowisko beztlenowe umożliwia kiełkowanie zarodników, po czym bakterie mogą się namnażać i wytwarzać toksyny. Krytycznie rzecz biorąc, spożycie toksyny zamiast zarodników lub bakterii wegetatywnych powoduje zatrucie jadem kiełbasianym . Niemniej jednak wiadomo, że zatrucie jadem kiełbasianym jest przenoszone przez żywność w puszkach, która nie została odpowiednio ugotowana przed puszkowaniem lub po otwarciu puszki, więc można temu zapobiec. Botulizmowi niemowląt wynikającemu ze spożycia miodu lub innego pokarmu, który może przenosić te zarodniki, można zapobiegać poprzez wyeliminowanie tych pokarmów z diety dzieci w wieku poniżej 12 miesięcy.
Wrażliwość organizmu i toksyn
Właściwe chłodzenie w temperaturach poniżej 3 ° C (37 ° F) spowalnia wzrost C. botulinum . [ potrzebne źródło medyczne ] Organizm jest również podatny na wysokie stężenie soli, tlenu i niskie pH. [ nieudana weryfikacja ] Sama toksyna jest szybko niszczona przez ciepło, na przykład podczas dokładnego gotowania. Zarodniki wytwarzające toksynę są odporne na ciepło i przetrwają we wrzącej wodzie przez dłuższy czas.
Toksyna botulinowa jest denaturowana , a tym samym dezaktywowana w temperaturze powyżej 85°C (185°F) przez pięć minut. Jako metaloproteaza cynku (patrz poniżej), toksyna jest również podatna po ekspozycji na hamowanie przez inhibitory proteazy , np. hydroksamiany koordynujące cynk .
Badania
Kurcz powiek i zez
Uniwersyteccy okuliści z USA i Kanady udoskonalili zastosowanie toksyny botulinowej jako środka terapeutycznego. Do 1985 roku ustalono empirycznie protokół naukowy dotyczący miejsc wstrzyknięć i dawkowania w leczeniu kurczu powiek i zeza. Działania niepożądane w leczeniu tego schorzenia uznano za rzadkie, łagodne i uleczalne. Korzystne efekty iniekcji utrzymywały się tylko przez 4–6 miesięcy. Tak więc pacjenci z kurczem powiek wymagali ponownego wstrzyknięcia dwa lub trzy razy w roku.
W 1986 roku mikroproducent i dystrybutor Botoxu firmy Scott nie był już w stanie dostarczać leku z powodu niemożności uzyskania ubezpieczenia od odpowiedzialności cywilnej za produkt. Pacjenci byli zdesperowani, ponieważ zapasy botoksu były stopniowo zużywane, co zmusiło go do porzucenia pacjentów, którzy mieli otrzymać następny zastrzyk. Przez okres czterech miesięcy amerykańscy pacjenci z kurczem powiek musieli umawiać się na wykonywanie zastrzyków przez uczestniczących lekarzy w kanadyjskich ośrodkach okulistycznych do czasu rozwiązania kwestii odpowiedzialności.
W grudniu 1989 roku Botox został zatwierdzony przez amerykańską FDA do leczenia zeza, kurczu powiek i połowiczego skurczu twarzy u pacjentów w wieku powyżej 12 lat.
W przypadku leczenia esotropii dziecięcej u pacjentów w wieku poniżej 12 lat w kilku badaniach uzyskano odmienne wyniki. [ potrzebne lepsze źródło ]
Kosmetyk
Wpływ toksyny botulinowej typu A na redukcję i likwidację zmarszczek na czole po raz pierwszy opisał i opublikował dr Richard Clark, chirurg plastyczny z Sacramento w Kalifornii. W 1987 roku Clark stanął przed wyzwaniem wyeliminowania oszpecenia spowodowanego funkcjonowaniem tylko prawej strony mięśni czoła po sparaliżowaniu lewej strony czoła podczas zabiegu liftingu twarzy. Ta pacjentka chciała wyglądać lepiej po liftingu, ale doświadczała dziwnego jednostronnego uniesienia prawego czoła, podczas gdy lewa brew opadła, a ona odczuwała głębokie, wyraziste zmarszczki na prawym czole, podczas gdy lewa strona była idealnie gładka z powodu paraliżu. Clark był świadomy, że toksyna botulinowa jest bezpiecznie stosowana w leczeniu dzieci ze zezem i poprosił FDA o zgodę na eksperymentowanie z toksyną botulinową w celu sparaliżowania poruszających się i marszczących się normalnie funkcjonujących mięśni prawego czoła, aby obie strony czoła wyglądały tak samo. To badanie i opis przypadku kosmetycznego zastosowania toksyny botulinowej w leczeniu kosmetycznych komplikacji chirurgii plastycznej było pierwszym doniesieniem dotyczącym specyficznego leczenia zmarszczek i zostało opublikowane w czasopiśmie Chirurgia plastyczna i rekonstrukcyjna w 1989 roku . Amerykańskie Towarzystwo Chirurgów Plastycznych wyraźnie stwierdziło, że „pierwsze opisane użycie toksyny w warunkach estetycznych zostało dokonane przez Clarka i Berrisa w 1989 roku”.
JD i JA Carruthers również badali i opisali w 1992 roku zastosowanie toksyny botulinowej typu A jako zabiegu kosmetycznego. Przeprowadzili badanie pacjentów, których jedynym zmartwieniem była zmarszczka lub bruzda czoła gładzizny czoła. Poza tym uczestnicy badania byli normalni. Szesnastu z siedemnastu pacjentów dostępnych do obserwacji wykazało poprawę kosmetyczną. Badanie to zostało przedstawione na spotkaniu w 1991 roku. Badanie dotyczące leczenia zmarszczek gładzizny czoła zostało opublikowane w 1992 roku. Wynik ten został następnie potwierdzony przez inne grupy (Brin i grupa Columbia University pod Monte Keen). FDA ogłosiła rejestrację toksyny botulinowej typu A (Botox Cosmetic) w celu tymczasowej poprawy wyglądu umiarkowanych do ciężkich zmarszczek między brwiami (zmarszczek gładzizny czoła) w 2002 r. po szeroko zakrojonych badaniach klinicznych. Na długo przed tym rozpowszechniło się kosmetyczne zastosowanie toksyny botulinowej typu A. Rezultaty Botox Cosmetic mogą utrzymywać się do czterech miesięcy i mogą się różnić u każdego pacjenta. Amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła alternatywną metodę testowania bezpieczeństwa produktu w odpowiedzi na rosnące obawy opinii publicznej, że testowanie LD50 jest wymagane dla każdej partii sprzedawanej na rynku.
Toksyna botulinowa typu A znalazła również zastosowanie w leczeniu uśmiechu dziąsłowego , materiał wstrzykuje się w nadpobudliwe mięśnie górnej wargi, co powoduje zmniejszenie ruchu wargi ku górze, co skutkuje uśmiechem z mniejszą ekspozycją dziąseł . Botox jest zwykle wstrzykiwany w trzy mięśnie unoszące wargę, które zbiegają się po bocznej stronie ala nosa; dźwigacz labii superioris (LLS), mięsień dźwigacz labii superioris alaeque nasi (LLSAN) i zygomaticus minor (ZMi).
Zespół górnego neuronu ruchowego
Toksyna botulinowa typu A jest obecnie powszechną metodą leczenia mięśni dotkniętych zespołem górnego neuronu ruchowego (UMNS), takich jak mózgowe porażenie dziecięce , dla mięśni z upośledzoną zdolnością do efektywnego wydłużania . Mięśnie dotknięte UMNS często są ograniczone przez osłabienie , utratę wzajemnego hamowania , zmniejszoną kontrolę ruchu i hipertoniczność (w tym spastyczność ). W styczniu 2014 r. Toksyna botulinowa została zatwierdzona przez brytyjską Agencję Regulacyjną ds. Leków i Produktów Opieki Zdrowotnej (MHRA) do leczenia niepełnosprawności stawu skokowego spowodowanej spastycznością kończyn dolnych związaną z udarem u dorosłych. Ruchy w stawach mogą być ograniczone przez poważną nierównowagę mięśniową związaną z zespołem, kiedy niektóre mięśnie są wyraźnie hipertoniczne i brakuje im efektywnego aktywnego wydłużenia. Wstrzyknięcie nadmiernie aktywnego mięśnia w celu zmniejszenia jego poziomu skurczu może umożliwić poprawę ruchu posuwisto-zwrotnego, a więc poprawę zdolności poruszania się i ćwiczeń.
ślinotok
Sialorrhea to stan, w którym nie można wyeliminować wydzieliny z jamy ustnej, co powoduje gromadzenie się śliny w jamie ustnej. Ten stan może być spowodowany różnymi zespołami neurologicznymi, takimi jak porażenie Bella , niepełnosprawność intelektualna i porażenie mózgowe. Iniekcja toksyny botulinowej typu A do gruczołów ślinowych jest przydatna w zmniejszaniu wydzielania.
Dystonia szyjna
Toksyna botulinowa typu A jest stosowana w leczeniu dystonii szyjnej , ale po pewnym czasie może stać się nieskuteczna. Toksyna botulinowa typu B została zatwierdzona przez FDA do leczenia dystonii szyjnej w grudniu 2000 r. Nazwy handlowe toksyny botulinowej typu B to Myobloc w Stanach Zjednoczonych i Neurobloc w Unii Europejskiej.
Przewlekła migrena
Onabotulinumtoxin A (nazwa handlowa Botox) otrzymała aprobatę FDA do leczenia przewlekłych migren w dniu 15 października 2010 r. Toksyna jest wstrzykiwana w głowę i szyję w celu leczenia tych przewlekłych bólów głowy. Zatwierdzenie nastąpiło po dowodach przedstawionych agencji z dwóch badań finansowanych przez Allergan, wykazujących bardzo niewielką poprawę częstości występowania przewlekłych migren u osób z migreną poddawanych leczeniu botoksem.
Od tego czasu kilka randomizowanych badań kontrolnych wykazało, że toksyna botulinowa typu A poprawia objawy bólu głowy i poprawia jakość życia, gdy jest stosowana profilaktycznie u pacjentów z przewlekłą migreną , którzy wykazują cechy charakterystyczne bólu głowy zgodne z: uciskiem odczuwanym ze źródła zewnętrznego, krótszym całkowitym czasem trwania chronicznych migren (< 30 lat), „detoksykacji” pacjentów ze współistniejącym przewlekłym codziennym bólem głowy spowodowanym nadużywaniem leków i bez aktualnej historii innych leków zapobiegających bólowi głowy.
Depresja
Kilka małych badań wykazało korzyści u osób z depresją . Badania opierają się na hipotezie sprzężenia zwrotnego twarzy .
Przedwczesny wytrysk
Lek do leczenia przedwczesnego wytrysku jest opracowywany od 7 sierpnia 2013 roku i znajduje się w fazie II badań FDA.
Dalsza lektura
- Carruthers JD, Fagien S, Joseph JH, Humphrey SD, Biesman BS, Gallagher CJ i in. (styczeń 2020). „DaxibotulinumtoxinA do wstrzykiwań w leczeniu zmarszczek gładzizny czoła: wyniki każdego z dwóch wieloośrodkowych, randomizowanych, podwójnie ślepych, kontrolowanych placebo badań fazy 3 (SAKURA 1 i SAKURA 2)” . Chirurgia plastyczna i rekonstrukcyjna . 145 (1): 45–58. doi : 10.1097/PRS.0000000000006327 . PMC 6940025 . PMID 31609882 .
- Solish N, Carruthers J, Kaufman J, Rubio RG, Gross TM, Gallagher CJ (grudzień 2021). „Przegląd DaxibotulinumtoxinA do wstrzykiwań: nowy preparat toksyny botulinowej typu A” . Narkotyki . 81 (18): 2091–2101. doi : 10.1007/s40265-021-01631-w . PMC 8648634 . PMID 34787840 .
Linki zewnętrzne
- BotDB: obszerne zasoby na temat struktur BoNT, inhibitorów, kinetyki i literatury
- Przegląd wszystkich informacji strukturalnych dostępnych w PDB dla UniProt : P0DPI1 (neurotoksyna botulinowa typu A) w PDBe-KB .
- Przegląd wszystkich informacji strukturalnych dostępnych w PDB dla UniProt : P10844 (neurotoksyna botulinowa typu B) w PDBe-KB .
- Przegląd wszystkich informacji strukturalnych dostępnych w PDB dla UniProt : A0A0X1KH89 (Bontoksylizyna A) w PDBe-KB .
- „Onabotulinumtoxin A” . Portal informacyjny o lekach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „RimabotulinumtoxinB” . Portal informacyjny o lekach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Abobotulinumtoxin A” . Portal informacyjny o lekach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Zastrzyk z toksyny botulinowej A” . MedlinePlus .
- „Incobotulinumtoxin A Injection” . MedlinePlus .
- „Wstrzyknięcie toksyny botulinowej A” . MedlinePlus .
- „PrabotulinumtoxinA-xvfs Wstrzyknięcie” . MedlinePlus .
- „Wstrzyknięcie toksyny botulinowej B” . MedlinePlus .
- FDA OK Daxxify, przeciwzmarszczkowy lek i konkurent botoksu The New York Times