epibatydyna
 | |
 | |
| Identyfikatory | |
|---|---|
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| Bank Leków | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Karta informacyjna ECHA | 100.162.281 |
| Dane chemiczne i fizyczne | |
| Formuła | C11H13CIN2 _ _ _ _ _ _ |
| Masa cząsteczkowa | 208,69 g·mol -1 |
| Model 3D ( JSmol ) | |
| Gęstość | 1,2 ± 0,1 g/cm 3 |
| |
| |
|
| |
Epibatydyna jest chlorowanym alkaloidem wydzielanym przez ekwadorską żabę Epipedobates anthonyi i żabę trującą strzałkę z rodzaju Ameerega . Został odkryty przez Johna W. Daly'ego w 1974 r., Ale jego struktura została w pełni wyjaśniona dopiero w 1992 r. To, czy epibatydyna jest pierwszym zaobserwowanym przykładem chlorowanego alkaloidu, pozostaje kontrowersyjne ze względu na wyzwania związane z jednoznaczną identyfikacją związku z ograniczonych próbek zebranych przez Daly'ego . Do czasu zastosowania spektrometrii o wysokiej rozdzielczości w 1991 r. Pozostało mniej niż jeden miligram ekstraktu z próbek Daly'ego, co budzi obawy o możliwe zanieczyszczenie. Próbki z innych partii tego samego gatunku żaby nie dały epibatydyny.
Epibatydyna jest toksyczna. Jego toksyczność wynika z jego zdolności do interakcji z nikotynowymi i muskarynowymi receptorami acetylocholiny . Receptory te są zaangażowane między innymi w przekazywanie bolesnych odczuć i ruch. Epibatydyna powoduje następnie drętwienie, a ostatecznie paraliż. Dawki są śmiertelne, gdy paraliż powoduje zatrzymanie oddechu. Początkowo sądzono, że epibatydyna może być przydatna jako lek. Jednak ze względu na niedopuszczalny indeks terapeutyczny nie jest już badany pod kątem potencjalnych zastosowań terapeutycznych.
Historia
Epibatydyna została odkryta przez Johna W. Daly'ego w 1974 roku. Została wyizolowana ze skóry żab Epipedobates anthonyi zebranych przez Daly'ego i współpracownika Charlesa Myersa. W latach 1974-1979 Daly i Myers zebrali skóry prawie 3000 żab z różnych miejsc w Ekwadorze, po stwierdzeniu, że małe wstrzyknięcie preparatu z ich skóry wywołało u myszy działanie przeciwbólowe (przeciwbólowe), które przypominało działanie opioidu . Pomimo swojej potocznej nazwy - Anthony's Poison Arrow - sugerującej, że była używana przez tubylców podczas polowań, artykuł napisany przez Daly'ego w 2000 roku twierdził, że nie było lokalnego folkloru ani medycyny ludowej otaczającej żaby i że były one uważane przez miejscowych za mało ważne .
Struktura epibatydyny została wyjaśniona w 1992 r., co przeszkodziło uzyskaniu przez E. anthonyi statusu chronionego przez IUCN w 1984 r. Ponadto żaby te nie wytwarzają toksyny, gdy są hodowane i hodowane w niewoli, ponieważ same nie syntetyzują epibatydyny. Podobnie jak inne żaby z zatrutymi strzałkami, zamiast tego pozyskują je poprzez swoją dietę, a następnie sekwestrują na skórze. Prawdopodobnymi źródłami pokarmowymi są chrząszcze, mrówki, roztocza i muchy. Daly i Charles zauważyli, że epibatydyna została wyprodukowana z ich diety podczas ich podróży powrotnej do Ekwadoru w 1976 roku, kiedy odkryli, że w jednym miejscu żadna z obecnych żab nie wytwarzała alkaloidów, takich jak epibatydyna; odkryli, że tylko żaby w niektórych miejscach ze środkami dietetycznymi pozwalały tym żabom wytwarzać epibatydynę. Pokonując trudności, ostatecznie określono strukturę, a pierwszą syntezę epibatydyny zakończono w 1993 r. Od tego czasu opracowano wiele innych metod syntezy.
Ze względu na działanie przeciwbólowe epibatydyna cieszyła się dużym zainteresowaniem jako lek, ponieważ stwierdzono, że nie jest ona opioidem. Oznaczało to, że potencjalnie można go było używać bez obawy o uzależnienie. Szybko jednak okazało się, że nie można go stosować u ludzi, ponieważ dawka powodująca objawy toksyczne jest zbyt niska, aby była bezpieczna.
Synteza
Ze względu na względny niedobór epibatydyny w przyrodzie opracowano kilka dróg syntezy całkowitej.
Po odkryciu struktury epibatydyny opracowano ponad pięćdziesiąt sposobów jej syntezy w laboratorium. W pierwszym opisanym przykładzie dziewięcioetapowa procedura daje substancję w postaci racematu (w przeciwieństwie do naturalnie występującego związku to (+) -enancjomer; (-) -enancjomer nie występuje naturalnie). Później ustalono, że enancjomery (+) i (-) mają równoważne działanie przeciwbólowe i toksyczne. Proces okazał się dość produktywny, z wydajnością około 40%.
Enancjoselektywna synteza opisana przez EJ Coreya, wychodząca z aldehydu chloronikotynowego , została przedstawiona poniżej:
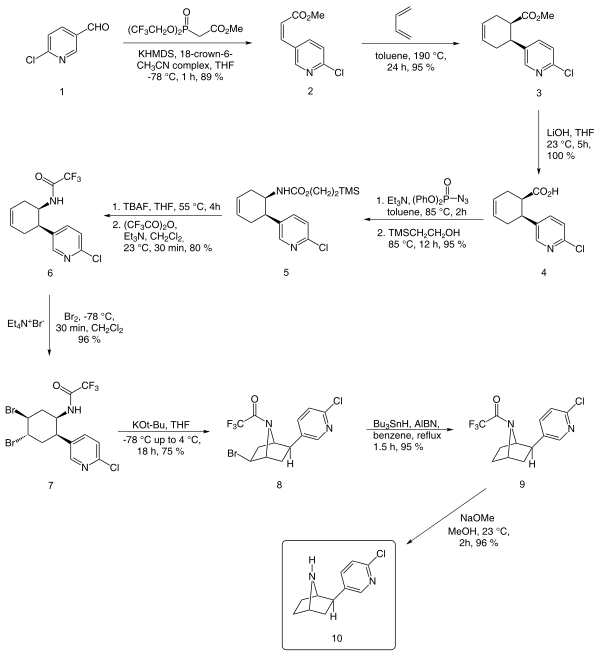
Oprócz metody Coreya, inne godne uwagi metody obejmują metody Broki, Huanga i Shena oraz Claytona i Regana.
Syntetyczne analogi
Podjęto szereg prób odkrycia strukturalnych analogów epibatyny, które zachowują działanie przeciwbólowe, ale bez toksyczności. Na przykład firma Abbott Laboratories wyprodukowała pochodne epibatydyny, w tym ABT-594 . ABT-594 zachowuje właściwości przeciwbólowe, jednocześnie unikając paraliżu, nadal wiążąc się z receptorami kontrolującymi odczuwanie bólu i wykazując niskie powinowactwo do nikotynowych receptorów acetylocholiny typu mięśniowego (nAChR), zmniejszając efekt paraliżu. Inne analogi epibatydyny obejmują ABT-418 , epiboksydynę i ich pochodne. Synteza epibatydyny, wykorzystująca mikrobiologiczną hydroksylację nieaktywowanego węgla w 7-azanorbornanie, została opublikowana w 1999 roku.
Struktura chemiczna
Epibatydyna jest piperydyno- pirydyną o strukturze podobnej do nikotyny . Jest to higroskopijna substancja oleista będąca bazą .
Efekty biologiczne
Mechanizm akcji
Epibatydyna ma dwa mechanizmy działania: może wiązać się z nikotynowymi receptorami acetylocholiny (nAChR) lub muskarynowymi receptorami acetylocholiny (mAChR). W szczególności uważa się, że przeciwbólowe epibatydyny wynikają z jej wiązania z podtypem α4/β2 receptorów nikotynowych. Epibatydyna wiąże się również z α3/β4 iw znacznie mniejszym stopniu z receptorami α7 (powinowactwo 300-krotnie mniejsze niż z receptorami α4/β2 ). Kolejność powinowactwa do mięśniowych receptorów nikotynowych jest następująca: αε > αγ > αδ.
Receptory nikotynowe dla acetylocholiny znajdują się w błonach postsynaptycznych komórek nerwowych. Receptory te są przykładem kanałów bramkowanych jonami, w których wiązanie przez ligand powoduje zmianę konformacyjną umożliwiającą jonom przejście przez błonę do komórki. Propagują neuroprzekaźnictwo w ośrodkowym i obwodowym układzie nerwowym . Kiedy neuroprzekaźniki wiążą się z tymi receptorami, kanały jonowe otwierają się, umożliwiając jonom Na + i Ca 2+ przemieszczanie się przez błonę. To depolaryzuje błonę postsynaptyczną, indukując potencjał czynnościowy, który propaguje sygnał. Sygnał ten ostatecznie indukuje uwalnianie dopaminy i norepinefryny , co skutkuje działaniem antynocyceptywnym na organizm. Typowym neuroprzekaźnikiem dla nAChR jest acetylocholina. Jednak inne substancje (takie jak epibatydyna i nikotyna ) są również zdolne do wiązania się z receptorem i indukowania podobnej, jeśli nie identycznej, odpowiedzi. Epibatydyna ma niezwykle wysokie powinowactwo do nAChR, w zależności od podtypu receptora, od 0,05 nM w podtypie α4β2 do 22 nM w podtypie α7. Powinowactwo jak i skuteczność (a co za tym idzie również siła działania ) są znacznie wyższe niż w przypadku nikotyny.
Działanie paralityczne epibatydyny następuje po jej związaniu z mięśniowymi receptorami nikotynowymi .
Niskie dawki epibatydyny będą miały wpływ tylko na nAChR, ze względu na większe powinowactwo do nAChR niż do mAChR. Wyższe dawki spowodują jednak, że epibatydyna zwiąże się z mAChR.
enancjomery (+) i (-) epibatydyny są biologicznie aktywne i oba mają podobne powinowactwo wiązania z nAChR. Tylko enancjomer (+) nie indukuje tolerancji. Chociaż może to stanowić potencjalną przewagę terapeutyczną nad morfiną, epibatydyna nie weszła do badań klinicznych, ponieważ nawet bardzo małe dawki są śmiertelne dla gryzoni.
Objawy
Epibatydyna ma kilka toksycznych konsekwencji. Efekty potwierdzone empirycznie obejmują współczulnego trzewnego i zwiększone ciśnienie tętnicze. Skutki wyładowania nerwowego mogą powodować antynocycepcję, częściowo za pośrednictwem agonizmu ośrodkowych nikotynowych receptorów acetylocholiny przy niskich dawkach epibatydyny; 5 µg/kg. Jednak w wyższych dawkach epibatydyna spowoduje paraliż i utratę przytomności, śpiączkę i ostatecznie śmierć. Średnia dawka śmiertelna (LD50 ) epibatydyny wynosi od 1,46 µg/kg do 13,98 µg/kg. To sprawia, że epibatydyna jest nieco bardziej toksyczna niż dioksyny (ze średnią LD50 22,8 µg/kg). [ potrzebne źródło ] Ze względu na niewielką różnicę między jego stężeniem toksycznym a stężeniem antynocyceptywnym, jego zastosowania terapeutyczne są bardzo ograniczone.
W badaniach na myszach podanie dawek epibatydyny większych niż 5 μg/kg powodowało zależne od dawki działanie paraliżujące na organizm. Przy dawkach powyżej 5 μg/kg objawy obejmowały nadciśnienie (podwyższone ciśnienie krwi), porażenie układu oddechowego , drgawki i ostatecznie śmierć. Objawy zmieniają się jednak drastycznie po podaniu niższych dawek. Myszy stały się odporne na ból i ciepło bez żadnych negatywnych skutków wyższych dawek.
Farmakologia
Epibatydyna najskuteczniej dostaje się do organizmu poprzez wstrzyknięcie. Badania in vitro wydają się sugerować, że epibatydyna nie jest prawie wcale metabolizowana w organizmie człowieka.
Również obecnie niewiele jest informacji na temat drogi klirensu z organizmu. Maksymalne stężenie w mózgu osiągane jest po około 30 minutach od wejścia do organizmu.
Potencjalne zastosowania medyczne
Jak stwierdzono powyżej, epibatydyna ma wysoką siłę działania przeciwbólowego. Badania pokazują, że ma moc co najmniej 200 razy większą niż morfina . Ponieważ związek nie uzależniał ani nie powodował przyzwyczajenia [ potrzebne źródło ] , początkowo uważano, że zastąpienie morfiny jako środka przeciwbólowego jest bardzo obiecujące . Jednak stężenie terapeutyczne jest bardzo zbliżone do stężenia toksycznego. Oznacza to, że nawet w dawce terapeutycznej (5 µg/kg) część epibatydyny może wiązać się z muskarynowymi receptorami acetylocholiny i powodować działania niepożądane, takie jak nadciśnienie , bradykardia i niedowład mięśni .
W porównaniu ze złotym standardem w leczeniu bólu, morfina i epibatydyna potrzebowały tylko 2,5 μg/kg, aby zainicjować działanie przeciwbólowe, podczas gdy ten sam efekt wymagał około 10 mg/kg morfiny (4000 razy większa skuteczność). Obecnie prowadzone są jedynie podstawowe badania nad efekty epibatydyny zostały jeszcze przeprowadzone; lek był w tej chwili podawany tylko gryzoniom do analizy.
Antidotum
Antidotum na epibatydynę jest mekamylamina , nikotynowy antagonista receptora acetylocholiny, który jest nieselektywny i niekompetycyjny. Zarówno (+), jak i (-) enancjomery mekamylaminy okazały się skuteczne i oba mają takie samo powinowactwo do nikotynowych receptorów acetylocholiny.
Zobacz też
- 6-Chloronikotyna
- Trucizna strzały
- Batrachotoksyna (i blisko spokrewniona homobatrachotoksyna )
- Nemertellina , neurotoksyna blisko spokrewniona z nikotelliną
- fantasmidyna
- tetrodotoksyna
